
在一密閉容器中發生如下反應:
aA(g)![]() bB(g)
bB(g)
達平衡后,保持溫度不變,將容器容積增加一倍,新平衡建立時,cB 是原來的 60%,則( )
A.平衡向正反應方向發生了移動 B.A 物質的轉化率變小了
C.B 物質的質量分數增大了 D.a>b
科目:高中化學 來源: 題型:閱讀理解
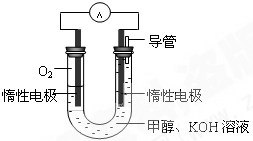 甲醇是重要的化工原料,在日常生活中有著廣泛的應用.
甲醇是重要的化工原料,在日常生活中有著廣泛的應用. CH3OH(g)△H1
CH3OH(g)△H1 CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 已知A、B、C、D、E五種元素的原子序數依次遞增,A、B、C、D位于前三周期.A位于周期表的s區,其原子中電子層數和未成對電子數相同;B的基態原子中電子占據三種能量不同的原子軌道,且每種軌道中的電子總數相同;D原子的核外成對電子數是未成對電子數的3倍.A、B、D三種元素組成的一種化合物M是新裝修居室中常含有的一種有害氣體,E是過渡元素且為地殼中含量較多的金屬元素之一.請回答下列問題:
已知A、B、C、D、E五種元素的原子序數依次遞增,A、B、C、D位于前三周期.A位于周期表的s區,其原子中電子層數和未成對電子數相同;B的基態原子中電子占據三種能量不同的原子軌道,且每種軌道中的電子總數相同;D原子的核外成對電子數是未成對電子數的3倍.A、B、D三種元素組成的一種化合物M是新裝修居室中常含有的一種有害氣體,E是過渡元素且為地殼中含量較多的金屬元素之一.請回答下列問題:
| ||
| ||

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
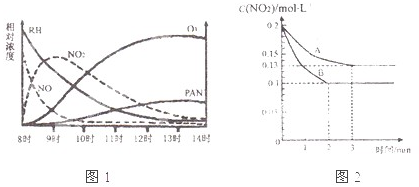
| C4(NO2)C(O2) |
| C2(N2O5) |
| C4(NO2)C(O2) |
| C2(N2O5) |
查看答案和解析>>
科目:高中化學 來源: 題型:
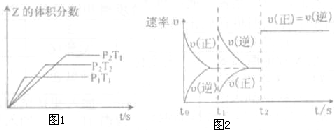 在一密閉容器中發生反應:2X(g)+Y(g)?aZ(g)△H=QkJ?mol-1,開始按體積 比2:1將X、Y充入反應器中,一定條件下發生反應.如圖1和圖2是根據反應繪制的圖象,下列有關說法正確的是( )
在一密閉容器中發生反應:2X(g)+Y(g)?aZ(g)△H=QkJ?mol-1,開始按體積 比2:1將X、Y充入反應器中,一定條件下發生反應.如圖1和圖2是根據反應繪制的圖象,下列有關說法正確的是( )| A、圖1,P1>P2,a<3 | B、圖1,T1<T2,Q>0 | C、圖2,t1時表示恒溫、恒壓條件下,向平衡體系中充入一定量的Z氣體 | D、圖2,如果α=3,t2時表示可能向體系中加入了催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:
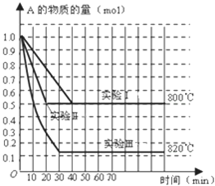 在一密閉容器中發生化學反應:2A(g)?B(g)+C(g);在幾種不同條件下進行,其中B、C的起始物質的量為0,反應物A的物質的量隨時間變化如圖所示,下列說法正確的是( )
在一密閉容器中發生化學反應:2A(g)?B(g)+C(g);在幾種不同條件下進行,其中B、C的起始物質的量為0,反應物A的物質的量隨時間變化如圖所示,下列說法正確的是( )| A、該反應正反應為放熱反應 | B、實驗Ⅱ和實驗Ⅰ比較,實驗Ⅱ一定使用了催化劑 | C、在實驗Ⅰ中,若容器的體積為0.5L,則從開始到達平衡時間內B的平均反應速率為0.025mol/(L?min) | D、在800℃時,增大壓強,若反應重新達平衡時混合氣體對氫氣的相對密度為64.5,則A的相對分子質量為129 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com