
【題目】部分弱酸的電離平衡常數如下表:
弱酸 | HCOOH | HCN | H2CO3 |
電離平衡常數 (25℃) | Ka=1.77×104 | Ka=4.9×1010 | Ka1=4.3×107 Ka2=5.6×1011 |
下列選項正確的是
A.NaCN溶液中通入少量CO2氣體:c(Na+) > c(![]() ) >c(
) >c(![]() )
)
B.稀釋等體積、等濃度的HCOOH和HCN至相同pH,加水的體積前者小于后者
C.物質的量濃度相等的HCOONa和KCN溶液中:c(Na+)c(HCOO) >c(K+)c(CN)
D.等體積、等濃度的HCOOH和NaCN混合溶液中:c(H+)+c(HCN) =c(HCOO)+c(OH)
【答案】AD
【解析】
試題分析:A、氫氰酸的電離平衡常數小于碳酸而大于碳酸氫根離子,所以氫氰酸酸性弱于碳酸而強于碳酸氫根離子,根據強酸制取弱酸知碳酸和氰化物的鹽反應生成氫氰酸和碳酸氫鹽,![]() 電離產生
電離產生![]() ,正確;B、因為HCOOH的電離平衡常數大于HCN的電離平衡常數,濃度相同,HCOOH的pH更低,稀釋到相同的pH需要水的量更多,錯誤;C、根據物料守恒可得兩溶液分別存在:c(Na+)c(HCOO)=c(HCOOH),c(K+)c(CN)=c(HCN),根據越弱越水解的規律,c(HCOOH)<c(HCN),則c(Na+)c(HCOO)<c(K+)c(CN),錯誤;D、存在的電荷守恒為c(Na+)+c(H+)=c(CN) +c(HCOO)+c(OH),物料守恒為c(Na+)=c(CN) +c(HCN ),相減得到c(H+)+c(HCN) =c(HCOO)+c(OH),正確。
,正確;B、因為HCOOH的電離平衡常數大于HCN的電離平衡常數,濃度相同,HCOOH的pH更低,稀釋到相同的pH需要水的量更多,錯誤;C、根據物料守恒可得兩溶液分別存在:c(Na+)c(HCOO)=c(HCOOH),c(K+)c(CN)=c(HCN),根據越弱越水解的規律,c(HCOOH)<c(HCN),則c(Na+)c(HCOO)<c(K+)c(CN),錯誤;D、存在的電荷守恒為c(Na+)+c(H+)=c(CN) +c(HCOO)+c(OH),物料守恒為c(Na+)=c(CN) +c(HCN ),相減得到c(H+)+c(HCN) =c(HCOO)+c(OH),正確。


科目:高中化學 來源: 題型:
【題目】現有易溶強電解質的混合溶液10 L,其中可能含K+、Ba2+、Na+、![]() 、Cl、
、Cl、![]() 、
、![]() 、OH中的幾種,向其中通入CO2氣體,產生沉淀的量與通入CO2的量之間的關系如下圖所示:
、OH中的幾種,向其中通入CO2氣體,產生沉淀的量與通入CO2的量之間的關系如下圖所示:
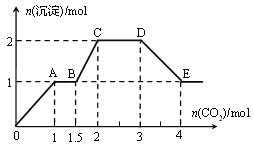
下列說法正確的是
A.該溶液中能確定存在的離子是Ba2+、![]() 、
、![]()
B.肯定不存在的離子是![]() 、OH
、OH
C.若不能確定的離子中至少還存在一種陽離子,則該離子的最小濃度為0.2 mol·L1
D.OA 段反應的離子方程式:2![]() +CO2+3H2O===2Al(OH)3↓+
+CO2+3H2O===2Al(OH)3↓+![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由鐵、鋅、鋁、鎂四種金屬中的兩種組成的混合物11 g,與足量的鹽酸反應產生的氫氣在標準狀況下為11.2 L,則混合物中一定含有的金屬是( )
A. 鐵 B. 鋅 C. 鎂 D. 鋁
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20.00mL 0.1000mol·L-1(NH4)2SO4溶液中逐滴加入0.2000mol·L-1NaOH時,溶液的pH與所加NaOH溶液體積的關系如下圖所示(不考慮揮發)。下列說法正確的是

A. 點a所示溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+)
B. 點b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-)
C. 點c所示溶液中:c(SO42-)+c(H+)=c(NH3H2O)+c(OH-)
D. 點d所示溶液中:c(SO42-)>c(NH3H2O)>c(NH4+)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2L密閉容器內,800℃時反應:2NO(g)+O2(g)![]() 2NO2(g)體系中,c(NO)隨時間的變化如表:
2NO2(g)體系中,c(NO)隨時間的變化如表:
時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
(1)分析上表,該反應達到平衡狀態所需時間是_________。

(2)上圖中表示NO2的濃度變化曲線是_______________。
(3)用NO表示從0~2s內該反應的平均速率v=________。
(4)v(NO):v(O2) = ______________。
(5)達到平衡狀態時O2的轉化率為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有四瓶溶液分別是FeCl3溶液、NaCl溶液、(NH4)2SO4溶液、MgSO4溶液,下列試劑中可用于鑒別它們的是
A.氨水 B.NaOH溶液 C.稀鹽酸 D.BaCl2溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.在一定條件下,將1.00molN2(g)與3.00molH2(g)混合于一個10.0L密閉容器中,在不同溫度下達到平衡時NH3(g)的平衡濃度如圖所示.其中溫度為T1時平衡混合氣體中氨氣的體積分數為25.0%。

(1)當溫度由T1變化到T2時,平衡常數關系K1___________K2(填“>”,“<”或“=”),焓變△H___________0.(填“>”或“<”)
(2)該反應在T1溫度下5.0min達到平衡,這段時間內N2的化學反應速率為___________,N2的轉化率___________;
(3)T1溫度下該反應的化學平衡常數K1=___________;
(4)T1溫度時,若測得高爐中c(N2)=0.5mol/L,c(H2)=0.5mol/L,c(NH3)=0.5mol/L在這種情況下,該反應是否處于平衡狀態___________(填是或否),此時反應速率是v正___________v逆(填>,<,=);
Ⅱ.根據最新研究報道,在常溫常壓和光照條件下N2在催化劑表面與水發生反應:2N2(g)+6H2O(l)=4NH3(g)+3O2(g)。
(1)此反應的△S 0(填“>”或“<”)。
已知2CO(g)+2NO(g)=N2(g)+2CO2(g) △H="-a" kJ·mol-1
2NO(g)+O2(g)=2NO2(g) △H ="-b" kJ·mol-1;CO的燃燒熱△H ="-c" kJ·mol-1。
(2)寫出消除汽車尾氣中NO2的污染時,NO2與CO的反應的熱化學反應方程式
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com