
【題目】淺綠色鹽X僅含四種元素,不含結晶水,M(X)<908gmol-1,某小組為了探究X的組成和性質,設計并完成了如下實驗

上述實驗中,得到23.3g白色沉淀 E、28.8g紅色固體G和12.8g紅色固體H。
已知:①X分解成A、B、C的反應為非氧化還原反應;
②常溫下B呈液態且1個B分子含有10個電子。
請回答如下問題:
(1)寫出B分子的電子式_______________;X的化學式是__________。
(2)在隔絕空氣、570℃溫度下加熱X至完全分解的化學反應方程式為:__________。
(3)請寫出G溶于D溶液的離子方程式:_________________。
(4)請設計實驗檢驗固體C中是否仍含有X:___________________。
【答案】![]() Cu4(OH)6SO4 Cu4(OH)6SO4
Cu4(OH)6SO4 Cu4(OH)6SO4![]() 4CuO+SO3↑+3H2O↑ Cu2O+2H+=Cu2++Cu+H2O 取少量樣品于試管中,加入足量稀鹽酸溶解,再加入少量BaCl2溶液,若產生白色沉淀則樣品中含有X,反之則沒有。
4CuO+SO3↑+3H2O↑ Cu2O+2H+=Cu2++Cu+H2O 取少量樣品于試管中,加入足量稀鹽酸溶解,再加入少量BaCl2溶液,若產生白色沉淀則樣品中含有X,反之則沒有。
【解析】
淺綠色鹽X在570℃、隔絕空氣條件下受熱分解為非氧化還原反應,得到A、B和黑色固體C,常溫下B呈液態且1個B分子含有10個電子,B為H2O,A和水反應生成的D能和氯化鋇反應生成白色沉淀E,E只能為BaSO4,則D為H2SO4,A是SO3;23.3g白色沉淀E的物質的量為0.1mol,黑色固體C可能為Fe3O4、CuO、C等,黑色固體C隔絕空氣在1000℃反應生成氣體F和紅色固體G,G能和H2SO4反應生成紅色固體和藍色溶液應為Cu2O在酸性溶液中的歧化反應,Cu2O+H2SO4=Cu+CuSO4+H2O,所以黑色固體C為CuO,G為Cu2O,氣體F為O2,紅色H為Cu,藍色溶液I為CuSO4,然后結合反應產生的物質的質量計算物質的量,利用物質的量的比等于原子個數比,結合其不含有結晶水,確定X的化學式,并進行有關解答。
根據上述分析可知A是SO3,B是H2O,C是CuO,D是H2SO4,E是BaSO4,F是O2,G為Cu2O,H為Cu,I為CuSO4,X是含有Cu、H、O、S四種元素的化合物。
(1)B為H2O,水分子中H、O原子之間以共價鍵結合,電子式為:![]() ;根據元素守恒可知,在淺綠色鹽X中n(Cu)=2n(Cu2O)=2×
;根據元素守恒可知,在淺綠色鹽X中n(Cu)=2n(Cu2O)=2×![]() =0.4mol,n(CuO)=0.4mol,n(S)=n(BaSO4)=
=0.4mol,n(CuO)=0.4mol,n(S)=n(BaSO4)=![]() =0.1mol,n(CuO):n(SO3)=0.04mol:0.01mol=4:1,僅含四種元素,不含結晶水,設化學式為:Cu4(OH)mSO4,Cu4(OH)mSO4
=0.1mol,n(CuO):n(SO3)=0.04mol:0.01mol=4:1,僅含四種元素,不含結晶水,設化學式為:Cu4(OH)mSO4,Cu4(OH)mSO4![]() 4CuO+SO3↑+
4CuO+SO3↑+![]() H2O↑,根據氧元素守恒得:m=6,符合M(X)<908g/mol,所以X化學式為Cu4(OH)6SO4;
H2O↑,根據氧元素守恒得:m=6,符合M(X)<908g/mol,所以X化學式為Cu4(OH)6SO4;
(2)X在隔絕空氣、570℃溫度下加熱發生Cu4(OH)6SO4![]() 4CuO+SO3↑+3H2O↑;
4CuO+SO3↑+3H2O↑;
(3)磚紅色固體G是Cu2O,與足量稀H2SO4發生氧化還原反應,產生Cu、CuSO4、H2O,反應的離子方程式為:Cu2O+2H+=Cu+Cu2++H2O;
(4)黑色固體C為CuO,如含有X,則可用檢驗SO42-的方法檢驗,方法是:取少量樣品于試管中,加入足量稀鹽酸溶解,再加入少量氯化鋇溶液,若產生白色沉淀,則樣品中含有X,反之則沒有。


科目:高中化學 來源: 題型:
【題目】“低碳經濟”已成為全世界科學家研究的重要課題。為減小和消除 CO2對環境的影響,一方面世界各國都在限制其排放量,另一方面科學家加強了對 CO2 創新利用的研究。
(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g) △H=-41kJ/mol
H2(g)+CO2(g) △H=-41kJ/mol
②C(s)+2H2(g)![]() CH4(g) △H=-73kJ/mol
CH4(g) △H=-73kJ/mol
③2CO(g)![]() C(s)+CO2(g) △H=-17kJ/mol
C(s)+CO2(g) △H=-17kJ/mol
寫出CO2與H2反應生成CH4和H2O(g)的熱化學方程式:_____。
(2)目前工業上有一種方法是用 CO2來生產燃料甲醇。為探究該反應原理,在容積為 2L密閉容器中,充入1molCO2和 3.25molH2在一定條件下發生反應,測得 CO2、CH3OH(g)和 H2O(g)的物質的量(n)隨時間的變化如圖所示:
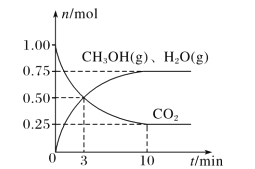
①從反應開始到平衡,氫氣的平均反應速率v(H2)= ____。
②下列措施一定不能使CO2的平衡轉化率增大的是____ (填字母)。
A.在原容器中再充入1molCO2
B.在原容器中再充入1molH2
C.在原容器中充入1mol氦氣
D.使用更有效的催化劑
E.縮小容器的容積
F.將水蒸氣從體系中分離
(3)煤化工通常研究不同條件下CO轉化率以解決實際問題。已知在催化劑存在條件下反應:CO(g)+H2O(g)H2(g)+CO2(g)的平衡轉化率隨p(H2O)/p(CO)及溫度變化關系如圖所示:
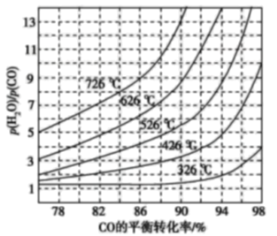
①上述反應的正反應方向是 ____(填“吸熱”或“放熱”)反應;
②對于氣相反應,用某組分(B)的平衡壓強(pB)代替物質的量濃度(cB)也可以表示平衡常數(記作 Kp),則在恒溫密閉容器中,該反應的Kp與Kc的關系是 _______,如果提高p(H2O)/p(CO),則Kp_______ (填“變大”“變小”或“不變”);使用鐵鎂催化劑的實際工業流程中,一般采用400℃左右,p(H2O)/p(CO) =3~5,采取此條件的原因可能是 _________ 。
(4)科學家用氮化鎵材料與銅組裝成如圖所示的人工光合系統,利用該裝置實現了用CO2和H2O合成CH4。下列關于該電池的敘述正確的是 ____(填字母)。
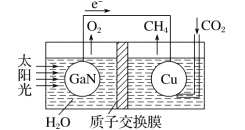
A.該裝置能量轉化形式僅存在太陽能轉化為電能
B.銅電極為正極,電極反應式為CO2+8e-+8H+=CH4+2H2O
C.電池內部H+透過質子交換膜從左向右移動
D.反應結束后,理論上溶液的 pH 值保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于下列有機化合物的說法正確的是( )
A.![]() 、
、![]() 、
、![]() 互為同系物
互為同系物
B.有機化合物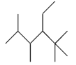 的名稱是2,3,5,5-四甲基-4-乙基己烷
的名稱是2,3,5,5-四甲基-4-乙基己烷
C.有機化合物![]() 中最多有16個原子共面
中最多有16個原子共面
D.含有5個碳原子的飽和鏈烴,其一氯取代物有8種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某工業廢渣的主要成分為 SiO2、FeO、MgO,對其進行處理以回收廢渣中的金屬元素。25℃時,金屬離子的物質的量濃度的負對數(-lg c)與溶液pH的關系如圖所示(一般離子濃度 c≤10-5mol/L時,即認為該離子在溶液中不存在)。下列有關說法不正確的是
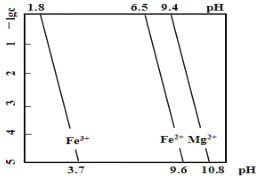
A.分離廢渣中的SiO2,可以用過量的鹽酸充分反應后過濾
B.可以用氯水將Fe2+氧化成Fe3+以便于鐵元素與鎂元素的分離
C.沉淀金屬元素的順序是先沉淀鎂元素再沉淀鐵元素
D.用 NaOH 調節pH沉淀鐵元素時,pH應控制略大于3.7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】疊氮化鈉(NaN3)是汽車安全氣囊最理想的氣體發生劑原料。下面是工業水合肼法制備疊氮化鈉的工藝流程:
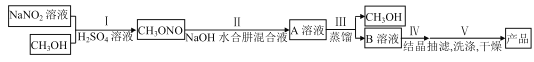
已知 NaN3 能與 AgNO3 反應生成白色難溶于水的 AgN3;有關物質的物理性質如表:
物質 | 熔點℃ | 沸點℃ | 溶解性 |
CH3OH | -97 | 64.7 | 與水互溶 |
水合肼(N2H4H2O) | 2 | 113.5 | 與水、醇互溶,不溶于乙醚和氯仿 |
亞硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
疊氮化鈉(NaN3) | 410(易分解) | —— | 易溶于水,難溶于醇,不溶于乙醚 |
請回答:
(1)步驟Ⅰ中NaNO2與稀硫酸發生副反應生成兩種氣體的離子方程式為:________;步驟Ⅱ中生成NaN3的化學方程式為:____________。
(2)實驗室模擬步驟II 實驗裝置如圖(裝置中冷卻水省略,下同):
①根據實驗發現溫度在20℃左右反應的選擇性和轉化率最高,但是該反應屬于放熱反應,因此可以采取的措施是_______________________。
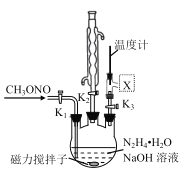
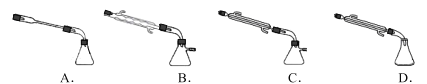
②圖中X處連接的最合適裝置應為下圖中的______ 。
(3)步驟Ⅳ對溶液 B 加熱蒸發至溶液體積的![]() ,NaN3 結晶析出。
,NaN3 結晶析出。
①步驟Ⅴ可以______________洗滌晶體。
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
②沉淀滴定法測定產品純度,是以淡黃色K2CrO4溶液作指示劑,將AgNO3標準溶液滴入樣品溶液,至少量Ag2CrO4出現,即溶液呈淡紅色為終點。AgNO3溶液要裝在棕色的酸式滴定管里進行滴定,理由是_________________________。
③下列操作或判斷合理的是__________。
A.滴定管和移液管管尖不可接觸錐形瓶內壁
B
C.滴定過程中可用蒸餾水將錐形瓶壁上粘附的溶液沖下
D.滴定終點時,若未等滴定管液面穩定就讀數會導致測定結果偏高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】濃硫酸分別和三種鈉鹽反應,下列分析正確的是

A. 對比①和②可以說明還原性Br->Cl-
B. ①和③相比可說明氧化性Br2>SO2
C. ②中試管口白霧是HCl遇水蒸氣所致,說明酸性H2SO4>HCl
D. ③中濃H2SO4被還原成SO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸是一種重要的化工產品.實驗室用硝酸氧化淀粉水解液制備草酸的裝置如圖所示(加熱、攪拌和儀器固定裝置均已略去)。

實驗過程如下:
①將一定量的淀粉水解液加入三頸瓶中;
②控制反應液溫度在55~60℃條件下,邊攪拌邊緩慢滴加一定量含有適量催化劑的混酸(65%HNO3與98%H2SO4的質量比為2∶1.5)溶液;
③反應3h左右,冷卻,抽濾后再重結晶得草酸晶體;
硝酸氧化淀粉水解液過程中可發生下列反應:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
(1)檢驗淀粉是否水解完全所需用的試劑為________;
(2)實驗中若混酸滴加過快,將導致草酸產率下降,其原因是_________;
(3)裝置C用于尾氣吸收,當尾氣中n(NO2)∶n(NO)=1∶1時,過量的NaOH溶液能將NO,全部吸收,原因是_________(用化學方程式表示);
(4)與用NaOH溶液吸收尾氣相比較,若用淀粉水解液吸收尾氣,其優、缺點是________;
(5)草酸重結晶的減壓過濾操作中,除燒杯、玻璃棒外,還必須使用屬于硅酸鹽材料的儀器有_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用酸性蝕刻廢液(含![]() 等)和堿性蝕刻廢液[NH4+、Cu(NH3)42+ 、NH3·H2O等]制備CuI(白色固體)的實驗流程如下:
等)和堿性蝕刻廢液[NH4+、Cu(NH3)42+ 、NH3·H2O等]制備CuI(白色固體)的實驗流程如下:
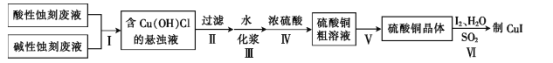
(1)步驟Ⅰ中發生了多個反應,其中![]() 與鹽酸反應生成Cu(OH)Cl的離子方程式為____。
與鹽酸反應生成Cu(OH)Cl的離子方程式為____。
(2)步驟Ⅳ需控制pH為1~2,80 ℃下進行,合適的加熱方式是____。
(3)步驟Ⅴ的具體步驟是蒸發濃縮、______、____。
(4)步驟Ⅵ在下列裝置(夾持及加熱裝置已省略)中進行。
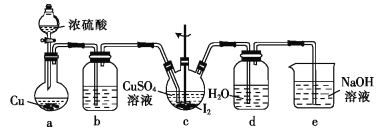
①裝置a中盛裝濃硫酸的儀器的名稱是___,圓底燒瓶中發生反應的化學方程式為___。
②裝置c中反應完成的現象是_____。
③用裝置d中的溶液洗滌制得的CuI的目的是____,然后再用無水乙醇洗滌的目的是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某固體混合物中可能含有: K+、 Na+、Clˉ、CO32ˉ、SO42ˉ等離子,將該固體溶解所得到的溶液進行如下實驗:

下列說法正確的是
A. 該混合物一定是K2CO3和 NaCl B. 該混合物可能是 Na2CO3和 KCl
C. 該混合物一定是Na2CO3和 NaCl D. 該混合物可能是 Na2SO4和 Na2CO3
【答案】B
【解析】焰色反應呈黃色,說明一定含有Na+;加入過量硝酸鋇生成能溶于鹽酸的沉淀,原溶液一定含有CO32ˉ,一定不含SO42ˉ;加入過量硝酸鋇后的濾液中加入硝酸酸化的硝酸銀,生成白色沉淀,則原溶液一定含有Clˉ;根據以上分析,一定含有Na+、Clˉ、CO32ˉ,一定不含SO42ˉ,可能含有K+;所以該混合物可能是 Na2CO3、 KCl或K2CO3、NaCl,故B正確。
【題型】單選題
【結束】
20
【題目】一定量的鈉和鋁的混合物與足量的水充分反應,沒有金屬剩余,收到2.24L氣體,下列說法一定正確的是
A. 所得氣體為氫氣 B. 所得氣體的物質的量為 0.1 mol
C. 上述過程只發生一個化學反應 D. 所得溶液中只有一種溶質
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com