
【題目】某校學生課外活動小組為測定鈉元素的相對原子質量,設計的裝置如圖所示,該裝置(包括水和干燥劑)的總質量為ag,從實驗室取出bg(不足量)鈉放入水中,塞緊瓶塞,完全反應后再稱量此裝置的總質量為cg。試回答:

(1)實驗室取用一小塊鈉,需要用到__________________實驗儀器。
(2)此干燥管的作用是________________________;若此鈉塊有極少量被氧化,則測出的相對原子質量會比實際相對原子質量________(填“偏大”、“偏小”或“不變”)。
(3)有甲同學建議在圖中干燥管上再連一同樣干燥管,其目的是____________________,計算鈉的相對原子質量的表達式為____________________。
(4)有乙同學為避免由于行動不夠迅速產生偏差,又建議在集氣瓶中再加入一定量煤油,其目的是_____。
【答案】濾紙、小刀、鑷子、玻璃片 吸收水蒸氣,避免集氣瓶中水蒸氣逸出 偏大 避免空氣中水蒸氣被干燥劑吸收 b/(a+b—c) 避免鈉投入后,立即與水反應,來不及塞上塞子
【解析】
(1)取用金屬鈉時,用鑷子夾取一小塊金屬鈉,用濾紙吸收煤油或石蠟,在玻璃片或濾紙上用小刀切黃豆大小的金屬鈉,投入水中,用玻璃片覆蓋水槽,防止液體濺出,所以所需用品至少有:小刀、鑷子、濾紙、玻璃片,故答案為:刀、鑷子、濾紙、玻璃片;
(2)無水氯化鈣吸收容易吸收水蒸氣,裝置中的干燥管是用來吸收水蒸氣,避免集氣瓶中水蒸氣逸出;若鈉塊有極少量被氧化,會導致生成的氫氣減少,即(a+b-c)減小,結合(3)中的表達式,測出的相對原子質量會比實際相對原子質量偏大,故答案為:吸收水蒸氣,避免集氣瓶中水蒸氣逸出;偏大;
(3)空氣的水蒸氣容易被無水氯化鈣吸收,影響了氫氣質量的計算,所以應該在干燥管上再連接一同樣的干燥管,目的是避免空氣中水蒸氣被干燥劑吸收;依題設實驗數據,bg鈉與足量水反應產生氫氣的質量為(a+b-c)g,設所求鈉的相對原子質量為x,根據電子守恒可得:![]() =
=![]() ×2,解得:x=
×2,解得:x=![]() ,故答案為:避免空氣中水蒸氣被干燥劑吸收;
,故答案為:避免空氣中水蒸氣被干燥劑吸收; ![]() ;
;
(4)鈉與水的反應比較劇烈,為了避免鈉投入后,立即與水反應,來不及塞上塞子,影響氫氣質量的測定,需要在集氣瓶中再加入一定量的石蠟油或煤油,故答案為:避免鈉投入后,立即與水反應,來不及塞上塞子。


科目:高中化學 來源: 題型:
【題目】多硫化物是含多硫離子(Sx2-)的化合物,可用作廢水處理劑、硫化劑等。回答下列問題:
(1)多硫化鈉(Na2S5)可由H2S與Na2S在一定條件下反應制得,該反應的還原產物為___________,Na2S5中含有的化學鍵類型是______________________。
(2)多硫化物MS4溶液在堿性條件下可高效處理高濃度含CN-電鍍廢水,CN-被氧化成毒性較小的SCN-,S2-轉化為S2-。
①M的離子與S2-具有相同的核外電子排布,則M在周期表中的位置是___________。
②CN-的電子式為______________________。
③處理廢水的離子方程式為______________________。
(3)過硫化銨[(NH4)2S2]可用作硫化試劑,為探究其性質,某研究小組進行如下實驗:取含1.00g(NH4)2S2的溶液加入足量稀硫酸酸化,得到0.32g淡黃色不溶物A和氫化物B。
①A是___________,生成的B在標準狀況的體積為___________mL。
②利用(NN4)2S2溶液中的活性硫能將硫錫礦中的難溶物硫化亞錫(II)(SnS)氧化成硫代錫(IV)酸銨[(NH4)2SnS3]而溶解,寫出反應的離子方程式___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將鋅銅合金溶解后與足量KI溶液反應(Zn2+不與I-反應),生成的I2用Na2S2O3標準溶液滴定,根據消耗的Na2S2O3溶液體積可測算合金中銅的含量。實驗過程如下圖所示:
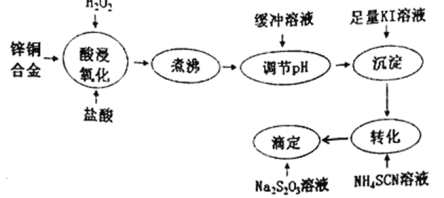
回答下列問題:
(1)H2O2的電子式為___________;“酸浸氧化”后銅元素的主要存在形式是___________(填離子符號)。
(2)“煮沸”的目的是____________________________________________。
(3)用緩沖溶液“調pH”是為了避免溶液的酸性太強,否則“滴定”時發生反應的離子方程式:_______________________________________________________;
①若100mLNa2S2O3溶液發生上述反應時,20s后生成的SO2比S多6.4g,則v(Na2S2O3)=___________mol/(L·s)(忽略溶液體積變化的影響)。
②該緩沖溶液是濃度均為0.10mol/L的CH3COOH和 CH3 COONH4的混合溶液。25℃時,溶液中各種離子濃度由大到小的順序為_________________________________。(已知:25℃時,Ka(CH3COOH)=Kb(NH3·H2O)=1.8×10-5)
(4)“沉淀”步驟中有CuI沉淀產生,反應的離子方程式為______________________。
(5)“轉化”步驟中,CuI轉化為 CuSCN, CuSCN吸附I2的傾向比CuI更小,使“滴定”誤差減小。沉淀完全轉化后,溶液中c(SCN-):c(I-)≥___________。(已知:Ksp(CuI)=1.0×10-12;Ksp( CuSCN)=4.4×10-15)
(6)下列情況可能造成測得的銅含量偏高的是___________(填標號)。
A.銅鋅合金中含少量鐵
B.“沉淀”時,I2與I-結合生成I3-:I2+ I-= I3-
C.“轉化后的溶液在空氣中放置太久,沒有及時滴定
D.“滴定”過程中,往錐形瓶內加入少量蒸餾水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用塊狀碳酸鈣與稀鹽酸反應制取二氧化碳氣體,下列可以降低反應速率的措施是( )
A. 加熱B. 加入濃鹽酸C. 加入蒸餾水D. 減少塊狀碳酸鈣固體質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家已獲得了極具理論研究意義的N4分子,其結構為正四面體(如圖所示),與白磷分子相似。氣態時,已知斷裂1mol N—N鍵吸收193kJ熱量,斷裂1mol N≡N鍵吸收941kJ熱量,則( )
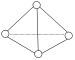
A. N4與N2互稱為同位素 B. 1mol N4氣體轉化為N2時要吸收748kJ能量
C. N4是N2的同系物 D. 1mol N4氣體轉化為N2時要放出724kJ能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,“二氧化碳是否在有水存在時,才能與過氧化鈉反應?”這個問題可通過以下實驗加以證明。

(1)按圖裝置,在干燥的試管Ⅲ中裝入Na2O2后,在通入CO2之前,應事先將活塞(K1、K2)關閉好,目的是____________
(2)試管Ⅰ內的試劑X是________時,打開活塞K1、K2,加熱試管Ⅲ約5分鐘后,將帶火星的小木條插入試管Ⅱ的液面上,可觀察到帶火星的小木條不能劇烈地燃燒起來,且Ⅲ內淡黃色粉末未發生變化。則所得的結論是____________________
(3)試管Ⅰ內試劑為CO2飽和水溶液時,其它操作同(2),通過________的現象,可以證明Na2O2與潮濕的CO2能反應且放出O2。
(4)寫出 Na2O2與CO2反應的化學方程式___________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在固定2L密閉容器中,充入X、Y各2 mol,發生可逆反應 X(g)+2Y(g) ![]() 2 Z(g),并達到平衡,以Y的濃度改變表示的反應速率v(正)、v(逆)與時間t的關系如圖,
2 Z(g),并達到平衡,以Y的濃度改變表示的反應速率v(正)、v(逆)與時間t的關系如圖,

則Y的平衡濃度(mol / L)表示式正確的是(式中S指對應區域的面積)
A、2 – S aob B、1 – Saob
C、2 – S abdo D、1 – S bod
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】結合元素周期表,用化學用語回答下列問題:
(1)表中的實線是元素周期表的部分邊界,請在圖中用實線補全元素周期表的邊界。_______

(2)表中所列元素,屬于短周期元素的有____,屬于主族元素的有___種;i元素位于第_____周期第______族。
(3)元素f是第____周期____族元素,請在如圖方框中按氮元素的式樣寫出該元素的原子序數、元素符號、元素名稱、相對原子質量。______

(4)在元素周期表中,同一族(縱行)的元素具有相似的化學性質。則下列各組元素具有相似化學性質的是_______(填標號)。
A. He和Ne B. B和Mg C. Al和Si D. F和Cl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z都是金屬,把X浸入Z的硝酸鹽溶液中,X的表面有Z析出,X和Y組成原電池時,Y為電池的負極。則X、Y、Z三種金屬的活動性順序為
A. X>Y>Z B. X>Z>Y
C. Y>X>Z D. Y>Z>X
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com