

分析 實驗裝置可知,本實驗首先由CaCO3和鹽酸反應生成CO2,產生氣體通過飽和NaHCO3溶液,以除去CO2氣體中混入的HCl,然后通過氯化鈣固體進行干燥,再通過過氧化鈉,過氧化鈉與CO2反應,產生O2,再氫氧化鈉吸收氧氣未反應的二氧化碳,最后用排水法收集O2,過氧化鈉樣品的純度測定,是利用過氧化鈉與水反應生成氫氧化鈉,再用鹽酸滴定氫氧化鈉,根據鹽酸的量可以計算出原樣品中過氧化鈉的量,在實驗過程中由于過氧化鈉與水反應有過氧化氫生成,所以要用熱水使過氧化氫分解,以減少對指示劑的影響,據此答題.
解答 解:實驗裝置可知,本實驗首先由CaCO3和鹽酸反應生成CO2,產生氣體通過飽和NaHCO3溶液,以除去CO2氣體中混入的HCl,然后通過氯化鈣固體進行干燥,再通過過氧化鈉,過氧化鈉與CO2反應,產生O2,再氫氧化鈉吸收氧氣未反應的二氧化碳,最后用排水法收集O2,過氧化鈉樣品的純度測定,是利用過氧化鈉與水反應生成氫氧化鈉,再用鹽酸滴定氫氧化鈉,根據鹽酸的量可以計算出原樣品中過氧化鈉的量,在實驗過程中由于過氧化鈉與水反應有過氧化氫生成,所以要用熱水使過氧化氫分解,以減少對指示劑的影響,
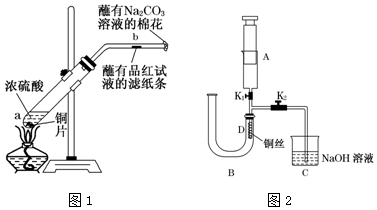
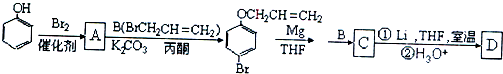
(1)A是實驗室制取CO2的裝置,用碳酸鈣與鹽酸反應,反應的離子方程式是CaCO3+2H+=Ca2++H2O+CO2↑,根據上面的分析可知,裝置B的作用是除去CO2中混有的HCl,裝置C的作用是干燥CO2,裝置E裝的試劑是 NaOH溶液,
故答案為:CaCO3+2H+=Ca2++H2O+CO2↑;除去CO2中混有的HCl;干燥CO2;NaOH溶液;
(2)過氧化鈉作潛水艇供氧劑的化學反應方程為2Na2O2+2CO2=2Na2CO3+O2↑,
故答案為:2Na2O2+2CO2=2Na2CO3+O2;
(3)①過氧化鈉樣品的純度測定步驟中,趁熱加入樣品溶解,因為沸水能使Na2O2溶解時所生成的H2O2迅速分解,消除其對中和滴定(特別是指示劑)的影響,
故答案為:沸水能使Na2O2溶解時所生成的H2O2迅速分解,消除其對中和滴定(特別是指示劑)的影響;
②根據題意,滴定中消耗的鹽酸的物質的量為cV×10-3 mol,即溶液中氫氧化鈉的物質的量為cV×10-3 mol,根據鈉元素守恒可知,原樣品中過氧化鈉樣質量為$\frac{1}{2}×$cV×10-3 mol×78g/mol=39cV×10-3 g,所以樣品的純度是$\frac{39cV×10{\;}^{-3}g}{ag}$×100%=$\frac{3.9cV}{a}$%,
故答案為:$\frac{3.9cV}{a}$%.
點評 本題考查了物質性質實驗方案的設計,題目難度中等,明確過氧化鈉與水反應的實質為解答關鍵,試題知識點較多、綜合性較強,充分考查學生的分析、理解能力及化學計算、化學實驗能力.


科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.85gNaCl晶體中含有0.1 NA 個Na+ | |
| B. | 1molFeCl3 完全水解轉化為Fe(OH)3膠體后能生成NA個膠體粒子 | |
| C. | 過量的Zn與含1molH2SO4的稀H2SO4完全反應,轉移的電子數一定為2NA | |
| D. | 一定量的Fe 與含1molHNO3的稀HNO3恰好完全反應,被還原的氮原子數小于NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 、
、 .
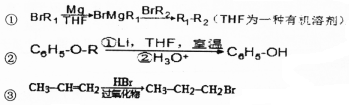
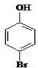
. 是化合物B的一種同分異構體,用1H核磁共振譜可以證明該化合物中有2種氫處于不同的化學環境.
是化合物B的一種同分異構體,用1H核磁共振譜可以證明該化合物中有2種氫處于不同的化學環境. 的有機反應類型取代反應.
的有機反應類型取代反應. .
.
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向FeBr2溶液中通入過量的Cl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| B. | 用食醋除去水壺內的水垢:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | KHCO3與足量澄清石灰水反應:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | 在強堿性溶液中,次氯酸鈉將Mn2+氧化成MnO2:Mn2++ClO-+H2O═MnO2↓+Cl-+2H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 鋼鐵工業是國家工業的基礎.請回答鋼鐵冶煉、腐蝕、防護過程中的有關問題.
鋼鐵工業是國家工業的基礎.請回答鋼鐵冶煉、腐蝕、防護過程中的有關問題.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 ,D的電子排布式為1s22s22p63s23p2.
,D的電子排布式為1s22s22p63s23p2. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com