
【題目】離子化合物A的化學式為NH5,它的所有原子的最外層都符合相應的稀有氣體原子的最外層結構。請回答:
(1)試寫出A的陽離子及陰離子的化學式________、________
(2)適當加熱,A就分解為兩種氣體,其中一種氣體是化合物,該反應的化學方程式為________。
(3)A溶于水后生成一種化合物和一種單質,則A的水溶液呈________性(酸/堿/中),原因:________
【答案】NH4+ H- NH4H ![]() NH3↑+H2↑ 堿 NH4H+H2O=NH3·H2O+H2↑
NH3↑+H2↑ 堿 NH4H+H2O=NH3·H2O+H2↑
【解析】
根據題目的信息可知:NH5的所有原子的最外層都符合穩定結構,因此是銨根離子和氫離子,一個銨根離子帶一個單位的正電荷,一個氫離子帶一個單位的負電荷;根據質量守恒定律可知:NH5分解為氨氣和氫氣;A溶于水后生成一種化合物和一種單質,即NH5和水反應生成氨水和氫氣,氨水顯堿性。
(1)NH5的所有原子的最外層都符合穩定結構,因此是銨根離子和氫離子,一個銨根離子帶一個單位的正電荷,一個氫離子帶一個單位的負電荷,整個物質對外不顯電性,陽離子及陰離子的化學符號為:NH4+;H-;
(2)根據質量守恒定律可知:NH5受熱分解為氨氣和氫氣,反應的化學方程式為:NH4H ![]() NH3↑+H2↑;
NH3↑+H2↑;
(3)A溶于水后生成一種化合物和一種單質,即NH5和水反應生成氨水和氫氣,氨水顯堿性,化學方程式: NH5+H2O=NH3H2O+H2↑。


 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:
【題目】一定溫度下,在體積為1L的密閉容器內進行著某一反應,X氣體、Y氣體的物質的量隨反應時間變化的曲線如圖。下列敘述中正確的是

A.反應的化學方程式為![]()
B.![]() 時,Y的濃度是X濃度的
時,Y的濃度是X濃度的![]() 倍
倍
C.根據![]() 時的數據,可求出該溫度下的平衡常數
時的數據,可求出該溫度下的平衡常數
D.![]() 時,逆反應速率大于正反應速率
時,逆反應速率大于正反應速率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實不能用沉淀溶解平衡原理解釋的是![]()
A.誤食可溶性鋇鹽,用![]() 的硫酸鈉溶液洗胃
的硫酸鈉溶液洗胃
B.除去硫酸銅溶液中的鐵離子,可加![]() ,調節pH
,調節pH
C.在AgI的沉淀體系中加硫化鈉溶液,出現黑色沉淀
D.在配制![]() 溶液時,用稀鹽酸溶解
溶液時,用稀鹽酸溶解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂鋁水滑石(Mg2Al(OH)6ClxH2O)是一種人工合成的新材料.它在高溫下完全分解MgO、Al2O3、HCl和水蒸氣.用如圖所示的裝置進行實驗以確定其化學式.完成下面小題。

【1】若只通過測定裝置中C、D的增重來確定x,則裝置按氣流方向接口的連接順序為
A.a→b→c→eB.a→c→b→dC.a→e→d→bD.a→d→e→c
【2】加熱前通N2,稱取C、D的初始質量后,再持續通N2。對通N2作用敘述錯誤的是
A.加熱前通,為排盡裝置中空氣
B.持續通,為將產生的氣體被C、D完全吸收
C.持續通,為防止倒吸
D.持續通,為防止MgO、Al2O3和氧氣反應
【3】完全分解后測得C增重3.65g、D增重9.90g,則x的值是
A.2B.3C.4D.5
【4】若氣體溫度過高,則不易被液體充分吸收,冷卻玻管B能降低氣體的溫度,但不能液化水蒸氣。若取消B后進行實驗,測定的x值將
A.偏低B.偏高C.無影響D.無法確定
【5】上述鎂鋁水滑石在空氣中放置時易發生反應生成Mg2Al(OH)6Cl1﹣2y(CO3)yzH2O,該生成物也能發生類似的熱分解反應,現以此物為樣品,用上述裝置和試劑進行實驗測定z,除測定D的增重外,至少還需測定
A.樣品的質量
B.裝置C的增重
C.樣品的質量和裝置C的增重
D.樣品分解后殘余物質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可溶性鋇鹽有毒,醫院中常用硫酸鋇這種鋇鹽作為內服造影劑。醫院搶救鋇離子中毒患者時,除催吐外,還需要向中毒者胃中灌入硫酸鈉溶液。已知:Ksp(BaCO3)=5.1×10-9 mol2·L-2;Ksp(BaSO4)=1.1×10-10 mol2·L-2。下列推斷正確的是( )
A. 不用碳酸鋇作為內服造影劑,是因為Ksp(BaCO3)>Ksp(BaSO4)
B. 搶救鋇離子中毒患者時,若沒有硫酸鈉,可以用碳酸鈉溶液代替
C. 若誤飲[Ba2+]=1.0×10-5 mol·L-1的溶液時,會引起鋇離子中毒
D. 可以用0.36 mol·L-1的Na2SO4溶液給鋇離子中毒患者洗胃
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將金屬M的樣品2.5g放入50g 19.6%的硫酸溶液中,恰好完全反應(樣品中的雜質既不溶于硫酸,也不與其發生反應),生成硫酸鹽。實驗測知,此硫酸鹽中硫、氧元素的質量分數之和為80 %。試求:
(1)原金屬樣品中,金屬M的質量分數_____
(2)M的相對原子質量__________
(3)反應所得的硫酸鹽溶液中溶質的質量分數___________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁氫化鈉(NaAlH4)是有機合成的一種重要還原劑。一般的制備方法是將AlC13溶于有機溶劑,再把所得溶液滴加到NaH粉末上,可制得鋁氫化鈉。實驗要求和裝置如下,回答下列問題:
(1)制取鋁氫化鈉要在非水溶液中進行,主要原因是_______(用化學方程式表示)。用下列裝置制取少量鋁氫化鈉(含副產物處理)較為合理的是__________。

(2)對于原料A1C13的制取,某興趣小組設計了如下裝置:
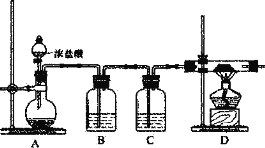
①連接好裝置后,應進行的第一步操作是_________;為保證產物的純凈,應待D中__________(填現象)再加熱酒精燈。
②B裝置中盛裝飽和NaCl溶液,實驗開始后B中產生的現象是_________,選擇飽和NaCl溶液的理由是_____。
③C裝置的作用是_________;若無C裝置,試預測實驗后D中生成物除A1C13外可能還含有_________。(填化學式)
④上述裝置存在的明顯缺陷是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂是一種重要的金屬資源,工業上制取鎂單質主要是電解法。
(1)電解法制取鎂單質的反應方程式是:___。
(2)電解原料無水氯化鎂可由海水制備。主要有以下步驟:①在一定條件下脫水干燥;②海水中加熟石灰;③加鹽酸;④過濾;⑤蒸發濃縮冷卻結晶。其步驟先后順序是___(步驟可重復使用),
(3)上述步驟①中“一定條件下”具體是指:___,其目的是___。
(4)已知某溫度下Mg(OH)2的Ksp=6.4×l012,當溶液中c(Mg2+)≤1.0×105mol·L1可視為沉淀完全,則此溫度下應保持溶液中c(OH-)≥___mol·L1。
(5)將飽和NH4Cl溶液滴入少量的Mg(OH)2懸濁液中,可看到白色沉淀溶解溶液變澄清。反應原理可能有兩方面,請分別用離子方程式表示:
①____;
②____。
要驗證①②誰是Mg(OH)2溶解的主要原因,可選取___代替NH4Cl溶液作對照實驗。
A.NH4NO3 B.(NH4)2SO4 C.CH3COONH4 D.NH4HCO3
(6)鎂電池是近年來科學技術研究的熱點之一。一種“鎂—次氯酸鹽”電池的總反應為:Mg+ClO-+H2O=Mg(OH)2+Cl-。其工作時正極的電極反應式:___;用此鎂電池給鉛蓄電池充電,下列說法中正確的是___。
A.鎂電池正極與鉛蓄電池正極相連
B.電子從Pb電極轉移到鎂電池負極
C.充電后,鉛蓄電池兩極質量均減小,理論上鎂電池消耗24gMg,陰、陽極的質量變化之比為3︰2
D.充電后,鎂電池和鉛蓄電池的pH均增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將0.1mol/L CH3COOH溶液加入水稀釋或加入少量CH3COONa晶體時,都會引起
A. 溶液中pH增大B. CH3COOH的電離程度變大
C. 溶液的導電能力減弱D. CH3COO-的濃度變小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com