
(15分)X、Y、Z、W、Q 五種元素原子序數依次增大,X原子核外的L層電子數是K層的兩倍,Z原子外圍電子排布式為nsnnp2n,W原子核外的M層中只有兩對成對電子,Q的核電荷數是Z與W的核電荷數之和。請回答下列問題:
(1)X、W的元素符號依次為 、 ;
(2)寫出Y2的電子式____________________;
(3)WZ2與XZ2分子的空間結構分別是 和 ,相同條件下兩者在水中的溶解度較大的是 (寫分子式);
(4)Q在元素周期表 區(填s、p、d、ds、f),其外圍電子排布式為 ,在形成化合物時它的最高化合價為 。
(15分)(1)C
S (各2分)(2)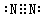 (2分)
(2分)
(3)V形 直線形 SO2 (各1分)
(4)d(2分) 3d54s1 (2分) +6(2分)
【解析】根據元素的結構和性質可判斷,X、Y、Z、W、Q 五種元素分別是C、N、O、S、Cr。
(2)氮氣中含有3對電子對,所以電子式為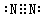 。
。
(3)SO2和CS2中中心原子含有對孤對電子分別是2對和0,所以前者是V形,后者是直線型。由于水水極性分子,所以根據相似相溶原理可知SO2在水中的溶解度大。
(4)區大名稱來自于按構造原理最后填入電子的能級的符號,所以根據構造原理可知,鉻元素是d區,其外圍電子排布式為3d54s1 。外圍電子共計6鉻,所以最高價是+6價。


 優等生題庫系列答案
優等生題庫系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
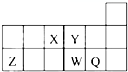 短周期元素X、Y、Z、W、Q在元素周期表中的相對位置如圖,下列說法正確的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相對位置如圖,下列說法正確的是( )| A、元素Y最高正化合價與最低負化合價的絕對值之和的數值等于8 | B、原子半徑的大小順序為:r(X)>r(Y)>r(Z)>r(W)>r(Q) | C、離子Y2-和Z3+半徑的大小順序為:r(Y2-)>r(Z3+) | D、元素W的最高價氧化物對應的水化物的酸性比Q的強 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com