
| 過程Ⅳ,B溶液中含有的離子 | 過程Ⅵ,B溶液中含有的離子 | |
| 甲 | 有Fe3+無Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+無Fe2+ | 有Fe2+ |
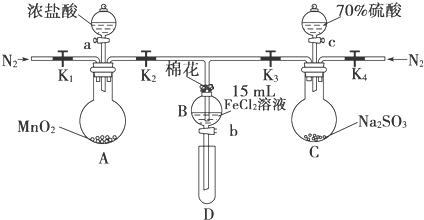
分析 (1)通入一段時間N2,排出裝置中的氧氣;
(2)檢驗B中溶液是否還有Fe2+的方法,用二價鐵與+3價鐵元素的配合物溶液反應生成藍色沉淀;
(3)第Ⅲ步B中發生三價鐵離子與硫化氫反應,生成硫沉淀、二價鐵、水;
(4)SO2通入酸性高錳酸鉀溶液中二者可以發生氧化還原反應;
(5)乙中第一次,說明氯氣不足,氯氣氧化性大于鐵離子,第二次有硫酸根離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫,丙中第一次有Fe3+,無Fe2+,則氯氣的氧化性大于鐵離子,第二次有亞鐵離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫;
(6)根據電子守恒進行計算.
解答 解:(1)打開K1~K4,關閉K5、K6,通入一段時間N2,目的是排出裝置中的氧氣,
故答案為:排出裝置中的空氣,防止干擾;
(2)檢驗B中溶液是否還有Fe2+的方法,用二價鐵與+3價鐵元素的配合物溶液反應生成藍色沉淀的離子方程式為:3Fe2++2(Fe(CN)6)3-=Fe3(Fe(CN)6)2↓,故答案為:3Fe2++2(Fe(CN)6)3-=Fe3(Fe(CN)6)2↓;
(3)三價鐵離子與硫化氫反應,生成硫沉淀、二價鐵、水,離子方程式為:2Fe3++H2S═2Fe2++2H++S↓,
故答案為:2Fe3++H2S═2Fe2++2H++S↓;
(4)SO2具有還原性,酸性高錳酸鉀溶液具有強的氧化性,二者混合后可以發生氧化還原反應:2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4,使高錳酸鉀褪色,故答案為:2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4;
(5)乙中第一次,說明氯氣不足,氯氣氧化性大于鐵離子,第二次有硫酸根離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫,丙中第一次有Fe3+,無Fe2+,則氯氣的氧化性大于鐵離子,第二次有亞鐵離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫,
故答案為:乙、丙;
(6)設FeBr2的物質的量濃度為c,
由電子守恒可知,$\frac{1.12L}{22.4L/mol}$×2×1=c×0.1L×(3-2)+c×0.1L×2×$\frac{1}{2}$×(1-0),
解得c=0.5mol/L,
故答案為:0.5mol/L.
點評 本題考查性質實驗方案的設計及氧化還原反應,明確裝置的作用及發生的反應是解答的關鍵,注意氧化性的比較是解答的難點,題目難度中等.


科目:高中化學 來源: 題型:實驗題
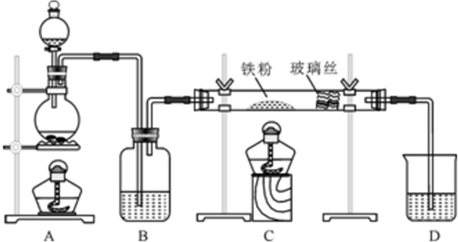
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “滴水石穿、繩鋸木斷”不涉及化學變化 | |
| B. | 明礬凈水的原理和“84”消毒液消毒的原理不相同 | |
| C. | 氟利昂作制冷劑會加劇霧霾天氣的形成 | |
| D. | 汽車尾氣中含有的氮氧化物,是汽油不完全燃燒造成的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe$\stackrel{稀H_{2}SO_{4}}{→}$FeSO4(aq)$\stackrel{NaOH(aq)}{→}$Fe(OH)2 | |
| B. | Al3+$\stackrel{過量氨水}{→}$Al${\;}_{2}^{-}$$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| C. | NH3$\stackrel{O_{2}}{→}$NO$\stackrel{H_{2}O}{→}$HNO3 | |
| D. | 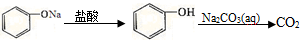 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
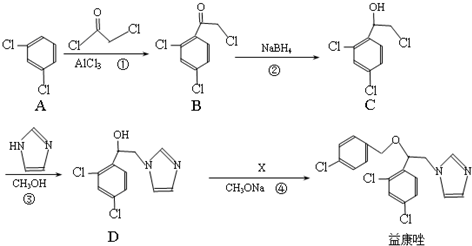
 .
. .
.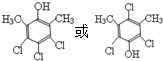 .
. 和
和  為原料制備
為原料制備 的合成路線流程圖(乙醇和無機試劑任用).合成路線流程圖示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{濃硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.
的合成路線流程圖(乙醇和無機試劑任用).合成路線流程圖示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{濃硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 280.58kJ | B. | 562.76kJ | C. | 530.58kJ | D. | 890.3kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 上海屬“水質性缺水”,保護水資源刻不容緩 | |
| B. | 提倡節水產業,加強廢水處理 | |
| C. | 只喝桶裝水或功能性飲料以保證飲用水質量 | |
| D. | 用再生水灌溉城市綠地 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 難失去電子的原子,易形成陰離子 | |
| B. | 只有化合物分子中才存在共價鍵 | |
| C. | 共價分子中所有原子都具有8電子穩定結構 | |
| D. | 含氧酸的組成中可以含有金屬元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
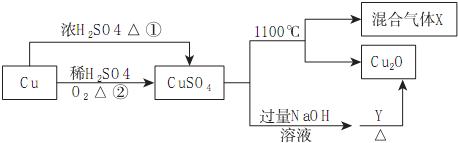
| A. | 途徑①和途徑②都體現了硫酸的酸性和氧化性 | |
| B. | Y可以是乙醛溶液 | |
| C. | CuSO4在1100℃分解所得氣體X可能是SO2和SO3的混合氣體 | |
| D. | 將CuSO4溶液蒸發濃縮、冷卻結晶,可制得膽礬晶體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com