
 ,碳元素的化合價為+2;用ClO2處理泄漏的氰化鈉,得到無毒的NaCl、N2和CO2.若處理4×10-5mol•L-1的廢水1000L,至少需要ClO2的質量為2.7g.
,碳元素的化合價為+2;用ClO2處理泄漏的氰化鈉,得到無毒的NaCl、N2和CO2.若處理4×10-5mol•L-1的廢水1000L,至少需要ClO2的質量為2.7g. 分析 (1)鈉燃燒生成過氧化鈉,過氧化鈉與二氧化碳反應生成氧氣和碳酸鈉;
(2)分析反應中元素化合價變化,依據氧化還原反應得失電子守恒、原子個數守恒配平方程式;
(3)依據化合物中各元素化合價代數和為0判斷碳元素化合價;用ClO2 處理泄漏的氰化鈉(NaCN),得到無毒的NaCl、N2 和CO2,該反應中Cl元素化合價由+4價變為-1價、N元素化合價由-3價變為0價,C元素化合價由+2價變為+4價,根據轉移電子守恒配平方程式,再根據氫氧化鈉和二氧化氯的關系式計算.
解答 解:(1)鈉燃燒生成過氧化鈉,方程式:2Na+O2$\frac{\underline{\;點燃\;}}{\;}$Na2O2,過氧化鈉與二氧化碳反應生成氧氣和碳酸鈉,方程式:2Na2O2+2CO2=2Na2CO3+O2;
故答案為:2Na+O2$\frac{\underline{\;點燃\;}}{\;}$Na2O2;2Na2O2+2CO2=2Na2CO3+O2;
(2)反應中鐵元素從+3價升高為+6價,次氯酸根離子中氯元素從+1價降為-1價,要使得失電子守恒,則三價鐵離子系數為2,次氯酸根離子系數為3,依據原子個數守恒反應的方程式:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
故答案為:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(3)氰化鈉中鈉元素為+1價,氮元素為-3價,依據化合價代數和為0,可知碳元素為+2價;
用ClO2 處理泄漏的氰化鈉(NaCN),得到無毒的NaCl、N2 和CO2,該反應中Cl元素化合價由+4價變為-1價、N元素化合價由-3價變為0價,C元素化合價由+2價變為+4價,根據轉移電子守恒配平方程式2ClO2+2NaCN=2NaCl+N2+2CO2,n(NaCN)=4×10-5mol•L-1×1000L=0.04mol,根據方程式知,消耗二氧化氯物質的量為0.04mol,其質量=0.04mol×67.5g/mol=2.7g,
故答案為:+2;2.7g.
點評 本題考查了氧化還原反應方程式的書寫及有關計算,明確氧化還原反應得失電子守恒規律是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:解答題
 .
.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溫度下的平衡常數為101.25 L/moL | |
| B. | 達到平衡時,SO2的轉化率是90% | |
| C. | 降低溫度,正反應速率減小程度比逆反應速率減小程度大 | |
| D. | 將平衡混合氣體通入過量BaCl2溶液中,得到沉淀的質量為231.4g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | HA物質的量濃度(mol•L1) | NaOH物質的量濃度(mol•Lˉ1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | c1 | 0.2 | 7 |
| 丙 | 0.1 | 0.1 | 7 |
| 丁 | 0.1 | 0.1 | 9 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
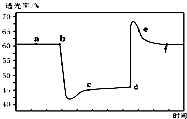 已知反應:2NO2(g)+4CO(g)?N2(g)+4CO2(g)△H<0.將一定量的NO2與CO充入裝有催化劑的注射器中后封口.右圖是在拉伸和壓縮注射器的過程中氣體透光率隨時間的變化(氣體顏色越深,透光率越小).下列說法不正確的是( )
已知反應:2NO2(g)+4CO(g)?N2(g)+4CO2(g)△H<0.將一定量的NO2與CO充入裝有催化劑的注射器中后封口.右圖是在拉伸和壓縮注射器的過程中氣體透光率隨時間的變化(氣體顏色越深,透光率越小).下列說法不正確的是( )| A. | b點的操作是快速壓縮注射器 | |
| B. | c點與a點相比,c(NO2)、c(N2)都增大 | |
| C. | e點:υ(正)<υ(逆) | |
| D. | 若考慮體系溫度變化,且沒有能量損失,則平衡常數K(c)>K(f) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 molAl3+離子含有的核外電子數為3NA | |
| B. | 1.7gH2O2中含有的電子數為0.9NA | |
| C. | 常溫下,11.2L的甲烷氣體含有甲烷分子數為0.5NA個 | |
| D. | 標準狀況下,33.6LH2O含有9.03×1023個H2O分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
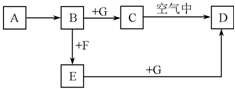 A~G是中學化學中常見的物質,在一定條件下它們之間的轉化關系如圖所示,其中A為金屬,F是一種有毒的氣體單質,G為NaOH溶液.
A~G是中學化學中常見的物質,在一定條件下它們之間的轉化關系如圖所示,其中A為金屬,F是一種有毒的氣體單質,G為NaOH溶液.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com