
| A. | 3種 | B. | 4種 | C. | 8種 | D. | 6種 |
 靈星計算小達人系列答案
靈星計算小達人系列答案 孟建平錯題本系列答案
孟建平錯題本系列答案科目:高中化學 來源: 題型:解答題
 某學校化學興趣小組以在不同的溫度下淀粉遇碘變藍色的快慢為背景來研究溫度對化學反應速率影響.具體研究過程:
某學校化學興趣小組以在不同的溫度下淀粉遇碘變藍色的快慢為背景來研究溫度對化學反應速率影響.具體研究過程:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 溫度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常數 | 0.4 | 0.6 | 1.0 | 1.1 | 1.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 圖1配制250mL0.10mol•L-1鹽酸 | B. | 圖2稀釋濃硫酸 | ||
| C. | 圖3稱量氯化鈉固體 | D. | 圖4CCl4萃取碘水的分液操作 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3 mol | B. | 2.4mol | C. | 2.2mol | D. | 3.2mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Mg2+、Cl-、OH- | B. | SO32-、SO42-、H+、K+ | ||
| C. | Fe2+、Fe3+、Cu2+、Cl- | D. | Ba2+、Na+、SO42-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
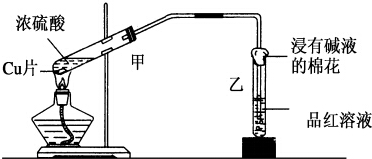 實驗室常用下列裝置來進行銅跟濃硫酸反應等一系列實驗.
實驗室常用下列裝置來進行銅跟濃硫酸反應等一系列實驗.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com