
| A. | 標準狀況下,22.4 L H2O含有的分子數為NA | |
| B. | 常溫常壓下,1.06 g Na2CO3含有的Na+離子數為0.01 NA | |
| C. | 物質的量濃度為0.5 mol/L的MgCl2溶液中,含有Cl-個數為NA | |
| D. | 標準狀況下,NA個CO2分子占有的體積為22.4 L |
分析 A.標況下水是液體;
B.1mol碳酸鈉含有2mol鈉離子;
C.溶液體積未知;
D.氣體摩爾體積22.4L/mol使用條件是標準狀況;
解答 解:A.標況下水是液體,22.4 L H2O物質的量大于1mol,故A錯誤;
B.1.06 g Na2CO3物質的量為$\frac{1.06g}{106g/mol}$=0.01mol,含有鈉離子個數為0.01mol×2×NA=0.02NA,故B錯誤;
C.溶液體積未知,無法計算溶液中氯離子數目,故C錯誤;
D.標準狀況下,NA個CO2分子物質的量為1mol,占有的體積為22.4 L,故D正確;
故選:D.
點評 本題考查阿伏加德羅常數的有關計算和判斷,明確物質的量、粒子數、質量、體積等與阿伏加德羅常數關系是解題關鍵,注意氣體摩爾體積使用條件和對象,題目難度不大.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 新制氯水中加入少量固體NaOH:c(Na+)=c(Cl-)+c(ClO-)+cOH-) | |
| B. | pH=9的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水與pH=3的鹽酸等體積混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1mol•L-1CH3COOH溶液與0.05mol•L-1NaOH溶液等體積混合:2c(H+)+c((CH3COOH)=c(CH3COO-)+2c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.85g | B. | 7.78g | C. | 6.72g | D. | 6g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
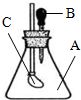 如圖所示,錐形瓶內裝有干燥的氣體A,膠頭滴管內盛有液體B,若擠壓膠頭滴管,使液體B滴入瓶中,振蕩,一會兒可見小氣球C鼓起.則對于氣體A和液體B最可能的是( )
如圖所示,錐形瓶內裝有干燥的氣體A,膠頭滴管內盛有液體B,若擠壓膠頭滴管,使液體B滴入瓶中,振蕩,一會兒可見小氣球C鼓起.則對于氣體A和液體B最可能的是( )| A. | A是Cl2,B是飽和NaCl溶液 | B. | A是NH3,B是酚酞溶液 | ||
| C. | A是H2,B是水 | D. | A是CO2,B是NaHCO3飽和溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 電鍍廠曾采用有氰電鍍工藝,由于排放的廢水中含有的劇毒CN-離子,而逐漸被無氰電鍍工藝替代.處理有氰電鍍的廢水時,可在催化劑TiO2作用下,先用NaClO將CN-離子氧化成CNO-,再在酸性條件下繼續被NaClO氧化成N2和CO2.環保工作人員在密閉系統中用下圖裝置進行實驗,以證明處理方法的有效性,并測定CN-被處理的百分率.將濃縮后含CN-離子的污水與過量NaClO溶液的混合液共200mL(其中CN-的濃度為0.05mol•L-1)倒入甲中,塞上橡皮塞,一段時間后,打開橡皮塞和活塞,使溶液全部放入乙中,關閉活塞.
電鍍廠曾采用有氰電鍍工藝,由于排放的廢水中含有的劇毒CN-離子,而逐漸被無氰電鍍工藝替代.處理有氰電鍍的廢水時,可在催化劑TiO2作用下,先用NaClO將CN-離子氧化成CNO-,再在酸性條件下繼續被NaClO氧化成N2和CO2.環保工作人員在密閉系統中用下圖裝置進行實驗,以證明處理方法的有效性,并測定CN-被處理的百分率.將濃縮后含CN-離子的污水與過量NaClO溶液的混合液共200mL(其中CN-的濃度為0.05mol•L-1)倒入甲中,塞上橡皮塞,一段時間后,打開橡皮塞和活塞,使溶液全部放入乙中,關閉活塞.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Zn(l)=Zn(g)△H=$\frac{1}{2}$(△H1-△H2) | |
| B. | 用硅制作的太陽能電池是將化學能轉化為電能 | |
| C. | 增加 Zn(g)的量,△H2變大 | |
| D. | Zn-Cu-CuSO4溶液構成的原電池中,Cu片質量增加,Zn片質量不變 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com