
【題目】下列問題,與鹽類水解有關的是
①NH4Cl與ZnCl2溶液可作焊接金屬時的除銹劑
②NaHCO3與Al2(SO4)3兩種溶液用于制造泡沫滅火器
③將含有CaSO4的水垢用Na2 CO3溶液處理,使之轉化為疏松、易溶于酸的CaCO3
④實驗室盛放碳酸鈉溶液的試劑瓶不能用磨口玻璃塞
⑤加熱蒸干AlCl3溶液得到Al(OH)3固體
A. ①②⑤ B. ②③④ C. ①②④⑤ D. ①②③④⑤
【答案】C
【解析】①金屬銹是金屬氧化物,NH4Cl和ZnCl2屬于強酸弱堿鹽,NH4+、Zn2+發生水解,使NH4Cl和ZnCl2溶液顯酸性,因此氯化銨與氯化鋅溶液可作焊接金屬時的除銹劑,故①正確;②兩種物質發生雙水解,其離子反應方程式為Al3++3HCO3-=Al(OH)3↓+3CO2↑,與鹽類水解有關,故②正確;③利用CaCO3溶解度小于CaSO4,發生CaSO4+Na2CO3=CaCO3+Na2CO3,CaCO3溶于酸,達到除去水垢的目的,此原理與水解無關,故③錯誤;④因為CO32-發生水解,CO32-+H2O![]() HCO3-+OH-,造成碳酸鈉溶液顯堿性,因此實驗室盛放碳酸鈉溶液的試劑瓶不能用磨口玻璃塞,與水解有關,故④正確;⑤AlCl3溶液:Al3++3H2O
HCO3-+OH-,造成碳酸鈉溶液顯堿性,因此實驗室盛放碳酸鈉溶液的試劑瓶不能用磨口玻璃塞,與水解有關,故④正確;⑤AlCl3溶液:Al3++3H2O![]() Al(OH)3+3H+,鹽類水解屬于吸熱反應,加熱促進平衡向正反應方向移動,HCl易揮發,加熱使之揮發,更加促進水解,因此加熱蒸干AlCl3溶液得到氫氧化鋁固體,與水解有關,故⑤正確;綜上所述,選項C正確。
Al(OH)3+3H+,鹽類水解屬于吸熱反應,加熱促進平衡向正反應方向移動,HCl易揮發,加熱使之揮發,更加促進水解,因此加熱蒸干AlCl3溶液得到氫氧化鋁固體,與水解有關,故⑤正確;綜上所述,選項C正確。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】按要求回答下列問題:
Ⅰ、稀Na2S溶液有一種臭雞蛋氣味,加入AlCl3溶液后,臭雞蛋氣味加劇,用離子方程式表示氣味加劇過程所發生的離子反應方程式_________________________________。
Ⅱ、常溫下,向20mL 0.2molL﹣1H2A溶液中滴加0.2molL﹣1NaOH溶液.有關微粒的物質的量變化如下圖(Ⅰ代表H2A,Ⅱ代表HA﹣,Ⅲ代表A2﹣)

(1)H2A在水中的電離方程式為_________________________。
(2)當V(NaOH)=20 mL時,寫出H2A與NaOH反應的離子方程式_________________。此時溶液中所有離子濃度大小關系:__________________。
(3)向NaHA溶液中加水,HA﹣的電離度_________、溶液的pH________。(填增大、減小、不變、無法確定)。
(4)V(NaOH)=30 mL時,溶液中存在如下關系:2c(H+)﹣2c(OH﹣)________2c(A2﹣)﹣3c(H2A)﹣c(HA﹣)(填“<”“>”或“=”)。
(5)某校研究性學習小組開展了題為“H2A是強酸還是弱酸的實驗研究”的探究活動。該校研究性學習小組設計了如下方案:你認為下述方案可行的是_______(填編號);
A.測量濃度為0.05 mol/L H2A溶液的pH,若pH大于1,則可證明H2A為弱電解質
B.可測NaHA溶液的pH。若pH>7,則H2A是弱酸;若pH<7,則H2A是強酸
C.比較中和等體積、等物質的量濃度的硫酸和H2A溶液所需氫氧化鈉的量多少,可證明H2A是強酸還是弱酸。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)25℃時,0.05mol/LH2SO4溶液的pH=______ ,0.01mol/LNaOH溶液的pH=______ 。
(2)某溫度下純水的c(H+)=4.0×10-7mol/L,則此溶液中的c(OH-)=_______;若溫度不變,滴入稀鹽酸,使c(H+)=2.0×10-4mol/L,則此溶液中由水電離產生的c(H+)=_________。
(3)氫氧化銅懸濁液中存在如下平衡:Cu(OH)2(s) ![]() Cu2+(aq)+2OH-(aq),常溫下其Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸銅溶液里c(Cu2+)=0.02 mol·L-1,如要生成Cu(OH)2沉淀,應調整溶液使之pH>________
Cu2+(aq)+2OH-(aq),常溫下其Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸銅溶液里c(Cu2+)=0.02 mol·L-1,如要生成Cu(OH)2沉淀,應調整溶液使之pH>________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A.反應C(s)+CO2(g)=2CO(g);△H>0,在任何條件下均不能自發進行
B.鉛蓄電池在放電過程中,溶液的PH值增加
C.常溫下,在0.1mol/L氨水中,加入少量NH4Cl晶體,溶液的pH減小
D.溫度一定時,水的離子積常數Kw不隨外加酸(堿)濃度的改變而改變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的數值,下列說法錯誤的是
A. 標準狀況下,2.24LH2S中含有0.1NA個H2S分子
B. 常溫常壓下,7.0g由丁烯與丙烯組成的混合氣體中含有的氫原子數目為NA
C. 常溫下,將2.7g鋁片投入足量的濃硫酸中,轉移電子的數目為0.3NA
D. 向1L的密閉容器中充入46gNO2氣體,容器中氮原子的數目為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米碳酸鈣是一種廣泛應用于塑料、食品、醫藥、飼料等行業的重要無機填料。以磷石膏鈣渣為原料制取高品質納米碳酸鈣的工藝流程如下:

已知某磷石膏鈣渣的主要成分及其含量如下表所示。
CaO | P2O5 | SO3 | Fe2O3 | Al2O3 | SiO2 | 燒失量 |
47.70% | 1.60% | 1.77% | 0.041% | 0.0027% | 9.85% | 37.69% |
請回答下列問題:
(1)對磷石膏鈣渣進行酸溶的目的是獲得機制CaCl2溶液,為了提高溶出率,可以采取的措施有______。(回答兩條即可)
(2)為了探究酸溶的工藝條件,稱取6 份各50g磷石膏鈣渣,分別用不同濃度鹽酸進行溶解,反應時間為30 min,測得濾液中鈣溶出率的結果如圖所示,最適宜的鹽酸濃度為_______。

(3)精制是向粗制CaCl2溶液中通入氨氣,控制溶液的pH,主要除去________ (填金屬陽離子)。
(4)碳化時,先將精制CaCl2溶液稀釋至一定體積,控制反應溫度以及NH3和CO2 的通入量,此過程中,通入氣體有先后順序,應先通入氣體的化學式_______(填化學式);碳化時發生反應的化學方程式為______。
(5)把CaCO3濁液滴入1.0molL-1 的Na2SO3溶液中,能否產生CaSO3沉淀?_______。若不能,說明原因;若能,請從定量的角度簡述判斷依據:_______。[已知:Ksp(CaSO3)=1.4×10-7,Ksp(CaCO3)=2.8×10-9]
(6)試設計簡單的實驗方案,判斷所得碳酸鈣樣品顆粒是否為納米級:__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】《京華時報》2016年8月24報道:京東自營的部分產品和一號店的部分產品二氧化硫嚴重超標,下列有關二氧化硫的說法不正確的是( )
A.二氧化硫有毒,不可以應用于任何食品行業
B.二氧化硫是一種食品添加劑,在國家標準范圍內使用時安全的
C.二氧化硫可以是品紅褪色
D.二氧化硫可以用于工業漂白
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是生物體細胞內部分有機化合物的概念圖,請回答下列問題。
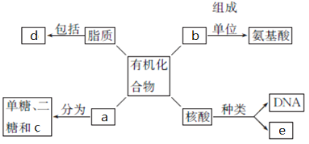
(1)小麥種子中的儲能物質c是__________,人和動物細胞中的儲能物質c是____________。
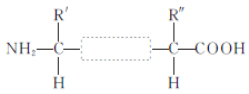
(2)兩個氨基酸發生脫水縮合反應時,產物是__________和__________,下圖方框內的結構簡式是____________。
(3)b結構的多樣性決定其功能的多樣性,如作為結構物質、免疫功能、___________、___________、信息傳遞等。
(4)SARS病毒的遺傳信息貯存在e中,e物質初步水解的產物是________________;在小麥葉肉細胞中,e主要存在于____________中。
(5)d中構成生物膜的主要是________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化硒(SeO2)是一種氧化劑,其被還原后的單質硒可能成為環境污染物,通過與濃HNO3或濃H2SO4反應生成SeO2以回收Se。
已知: ① Se+2H2SO4(濃)=2SO2↑+SeO2+2H2O ② SO2+SeO2+ H2O ![]() Se + SO42-+ H+
Se + SO42-+ H+
(1)依據Se與濃H2SO4的反應,寫出Se和濃HNO3(還原產物為NO2)反應的化學方程式:__________________。
(2)Se與濃HNO3的反應中,氧化劑是_______, 反應中被還原的元素是_______。當有標準狀況下33.6LNO2氣體生成時,轉移電子的物質的量是________mol。
(3)依據反應①②, 判斷SeO2、濃H2SO4、SO2的氧化性由強到弱的順序是__________。
(4) 配平反應②, 并用雙線橋法標出電子轉移的方向和數目:_____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com