
 甲醇合成反應為:CO(g)+2H2(g)?CH3OH(g)工業上用天然氣為原料,分為兩階段制備甲醇:
甲醇合成反應為:CO(g)+2H2(g)?CH3OH(g)工業上用天然氣為原料,分為兩階段制備甲醇:| 10min | 20min | 30min | 40min | 50min | 60min | |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
| 1 |
| 2 |
| 1 |
| 2 |
| 0.4mol/L |
| 10min |
| 0.8 |
| 0.2×(0.4)2 |
| 1 |
| 2 |


 浙江之星學業水平測試系列答案
浙江之星學業水平測試系列答案 高效智能課時作業系列答案
高效智能課時作業系列答案科目:高中化學 來源: 題型:
 (2009?深圳二模)甲醇合成反應為:CO(g)+2H2(g)?CH3OH(g)工業上用天然氣為原料,分為兩階段:
(2009?深圳二模)甲醇合成反應為:CO(g)+2H2(g)?CH3OH(g)工業上用天然氣為原料,分為兩階段:| 10min | 20min | 30min | 40min | 50min | 60min | |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
查看答案和解析>>
科目:高中化學 來源: 題型:
(10分)甲醇合成反應為:CO(g)+2H2(g) CH3OH(g)
工業上用天然氣為原料,分為兩階段制備甲醇:
(1)制備合成氣:CH4+H2O(g) CO+3H2。為解決合成氣中H2過量而CO不足的問題,原料氣中需添加CO2:CO3+H2=CO+H2O。為了使合成氣配比最佳,理論上原料氣中甲烷與二氧化碳體積比為____________________________________。
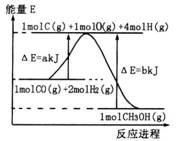
(2)合成甲醇:①反應過程中物質能量變化如右圖所示。寫出合成甲醇的熱化學方程式__________________。
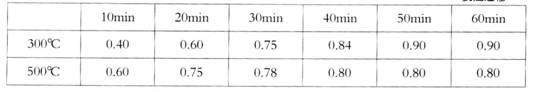
實驗室在1L密閉容器中進行模擬合成實驗。將lmolCO和2molH2通人容器中,分別恒溫在300℃和500℃反應,每隔一定時間測得容器中甲醇的濃度如下:
(表中數據單位:mol·L—1)
②300℃時反應開始10分鐘內,H2的平均反應速率為__________。
③500℃時平衡常數K的數值為___________。
④300℃時,將容器的容積壓縮到原來的1/2,在其他條件不變的情況下,對平衡體系 產生的影響是__________(填字母)。
a.c(H2)減小 b.正反應速率加快,逆反應速率減慢
c.CH3OH的物質的量增加 d.重新平衡時c(H2)/c(CH3OH)減小
查看答案和解析>>
科目:高中化學 來源:2011-2012學年山東省泰安市高三上學期期末檢測化學試卷 題型:填空題
(10分)甲醇合成反應為:CO(g)+2H2(g)  CH3OH(g)
CH3OH(g)
工業上用天然氣為原料,分為兩階段制備甲醇:
(1)制備合成氣:CH4+H2O(g) CO+3H2。為解決合成氣中H2過量而CO不足的問題,原料氣中需添加CO2:CO3+H2=CO+H2O。為了使合成氣配比最佳,理論上原料氣中甲烷與二氧化碳體積比為____________________________________。
CO+3H2。為解決合成氣中H2過量而CO不足的問題,原料氣中需添加CO2:CO3+H2=CO+H2O。為了使合成氣配比最佳,理論上原料氣中甲烷與二氧化碳體積比為____________________________________。
(2)合成甲醇:①反應過程中物質能量變化如右圖所示。寫出合成甲醇的熱化學方程式__________________。
實驗室在1L密閉容器中進行模擬合成實驗。將lmolCO和2molH2通人容器中,分別恒溫在300℃和500℃反應,每隔一定時間測得容器中甲醇的濃度如下:
(表中數據單位:mol·L—1)
 ②300℃時反應開始10分鐘內,H2的平均反應速率為__________。
②300℃時反應開始10分鐘內,H2的平均反應速率為__________。
③500℃時平衡常數K的數值為___________。
④300℃時,將容器的容積壓縮到原來的1/2,在其他條件不變的情況下,對平衡體系 產生的影響是__________(填字母)。
a.c(H2)減小 b.正反應速率加快,逆反應速率減慢
c.CH3OH的物質的量增加 d.重新平衡時c(H2)/c(CH3OH)減小
查看答案和解析>>
科目:高中化學 來源:2011-2012學年山東省泰安市高三(上)期末化學試卷(解析版) 題型:解答題
| 10min | 20min | 30min | 40min | 50min | 60min | |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
 ,在其他條件不變的情況下,對平衡體系產生的影響是______(填字母).
,在其他條件不變的情況下,對平衡體系產生的影響是______(填字母).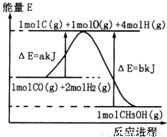
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com