
(13分)下圖是元素周期表的一部分,表中的①—⑩中元素,用化學用語填空回答:
| 族 周期 | I A | IIA | IIIA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 二 | | | | ① | ② | | ③ | |
| 三 | | ④ | ⑤ | ⑥ | | | ⑦ | ⑧ |
| 四 | ⑨ | | | | | | ⑩ | |
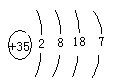
(1)
(2)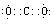
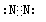
(3)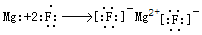
(4)2C+SiO2 Si+2CO↑;
Si+2CO↑;
(5)2Al+2H2O +NaOH=2NaAlO2+3H2↑;Al(OH)3+OH-=AlO-2+2H2O。
(6)660
解析試題分析:(1)⑩原子是Br原子,核內有35個質子,原子結構示意圖為 ;
;
(2)①的最高價氧化物是CO2,電子式為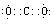 ;②的單質是N2,電子式為
;②的單質是N2,電子式為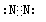 ;
;
(3)③與④形成化合物是MgF2,屬于離子化合物,Mg失去2個電子成為鎂離子,F得到1個電子成為氟離子,用電子式表示其形成過程是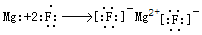 ;
;
(4)①的單質和⑥的氧化物反應即C與二氧化硅高溫下發生置換反應,化學方程式為2C+SiO2 Si+2CO↑;
Si+2CO↑;
(5)⑤是Al,與氫氧化鈉反應的化學方程式為2Al+2H2O +NaOH=2NaAlO2+3H2↑;氫氧化鋁是難溶物,書寫離子方程式時不能拆開,屬于氫氧化鋁與氫氧化鈉溶液反應的離子方程式為Al(OH)3+OH-=AlO-2+2H2O;
(6)甲烷與氧氣燃燒的化學方程式為CH4+2O2 CO2+ 2H2O,根據反應熱與化學鍵鍵能的關系,△H=(4×414+2×498-2×728-2×2×464)kJ/mol="-660" kJ/mol,所以1mol甲烷完全燃燒放出660kJ的熱量。
CO2+ 2H2O,根據反應熱與化學鍵鍵能的關系,△H=(4×414+2×498-2×728-2×2×464)kJ/mol="-660" kJ/mol,所以1mol甲烷完全燃燒放出660kJ的熱量。
考點:考查元素周期表的應用,元素的性質應用,化學用語的表示,化學熱效應的計算


 能考試期末沖刺卷系列答案
能考試期末沖刺卷系列答案科目:高中化學 來源: 題型:填空題
(17分)X、Y、Z、Q、E五種元素中,X原子核外的M層中只有兩對成對電子,Y原子核外的L層電子數是K層的兩倍,Z是地殼內含量(質量分數)最高的元素,Q的核電荷數是X與Z的核電荷數之和,E在元素周期表的各元素中電負性最大。請回答下列問題:
(1)X、Y的元素符號依次為 、 ;
(2)XZ2與YZ2分子的雜化軌道分別是 、 ,立體結構分別是 、 ,相同條件下兩者在水中的溶解度較大的是 (寫分子式),理由是 ;
(3)Q的元素符號是 ,它屬于第 周期,它的核外電子排布式為 ,在形成化合物時它的最高化合價為 ;
(4)用氫鍵表示式 寫出E的氫化物溶液中存在的所有氫鍵_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(15分)請回答以下問題:
(1)第四周期的某主族元素,其第一至五電離能數據如下圖1所示,則該元素對應原子的M層電子排布式為 。
(2)如下圖2所示,每條折線表示周期表ⅣA-ⅦA中的某一族元素氫化物的沸點變化。每個小黑點代表一種氫化物,其中a點代表的是 。簡述你的判斷依據
。
(3)CO2在高溫高壓下所形成的晶體其晶胞如下圖3所示.該晶體的類型屬于 (選填“分子”“原子”“離子”或“金屬”)晶體。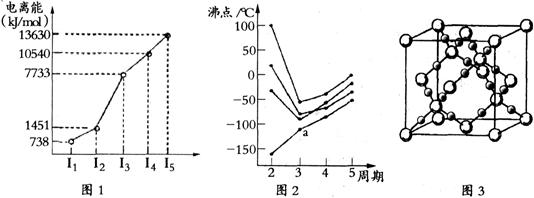
(4)BCl3原子的雜化方式為 。第一電離能介于B、N之間的第二周期元素有
種。寫出與BCl3結構相同的一種等電子體(寫離子) 。
(5)Cu元素形成的單質,其晶體的堆積模型為______,D的醋酸鹽晶體局部結構如圖,該晶體中含有的化學鍵是________ (填選項序號)。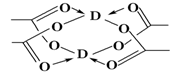
①極性鍵 ②非極性鍵 ③配位鍵 ④金屬鍵
(6)Fe的一種晶體如甲、乙所示,若按甲虛線方向切乙得到的A-D圖中正確的是 .鐵原子的配位數是 ,假設鐵原子的半徑是r cm,該晶體的密度是p g/cm3,則鐵的相對原子質量為 (設阿伏加德羅常數的值為NA)。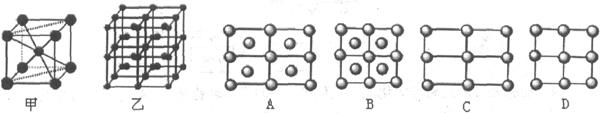
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(4分)(1)寫出表示含有8個質子、10個中子、10個電子的離子的符號 。(寫成ZAXn-的形式)
(2)周期表中位于第8縱行的鐵元素屬于第 族。
(3)周期表中最活潑的非金屬元素位于第 縱行 族。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(10分)下表為元素周期表的一部分,請參照元素①~⑨在表中的位置,用相應化學用語回答下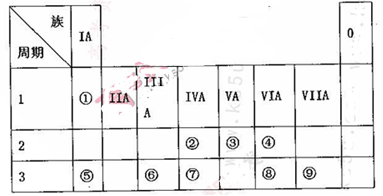
列問題:
(1)畫出表中形成化合物種類最多元素的原子結構示意圖____;寫出它與原予半徑最小的原子形成10電子且為正四面體結構的化合物的電子式____,用電子式表示⑤和⑧形成化合物的過程________。
(2).④⑤⑧形成的簡單離子半徑由大到小的順序為____(填離子符號);③⑦⑨的最高價氧化物對應水化物的酸性由強到弱的順序為_______(填化學式)。
(3).⑤和⑨形成化合物的化學鍵為__________。
(4).這些元素形成的氧化物中,不溶于水,但既能與強酸又能與強堿反應的是_______(填化學式),寫出它與⑤的最高價氧化物對應水化物發生反應的離子方程式___________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序數依次增加,A焰色反應呈黃色;工業常用電解B的熔融的氯化物來制備B,C是一種能被HF和NaOH溶液溶解的單質,D的電負性比磷大,第一電離能卻比磷小,E單質是制備漂白液的原料,F能形成紅色(或磚紅色)和黑色的兩種氧化物,G是一種主族金屬。
(1)前四周期所有元素中,基態原子中未成對電子與其所在周期數相同的元素有 種。
(2)元素A、B、C分別與氟氣化合形成物質X、Y、Z熔點見下表:
| 氟化物 | X | Y | Z |
| 熔點/K | 1266 | 1534 | 183 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
〔化學—選修3:物質結構與性質〕(15分)
早期發現的一種天然準晶顆粒由三種Al、Cu、Fe元素組成。回答下列問題:
(1)準晶是一種無平移周期序,但有嚴格準周期位置序的獨特晶體,可通過 方法區分晶體、準晶體和非晶體。
(2)基態鐵原子有 個未成對電子,三價鐵離子的電子排布式為: 可用硫氰化鉀奉驗三價鐵離子,形成配合物的顏色為
(3)新制備的氫氧化銅可將乙醛氧化為乙酸,而自身還原成氧化亞銅,乙醛中碳原子的雜化軌道類型為 ;一摩爾乙醛分子中含有的σ鍵的數目為: 。乙酸的沸點明顯高于乙醛,其主要原因是: 。氧化亞銅為半導體材料,在其立方晶胞內部有四個氧原子,其余氧原子位于面心和頂點,則該晶胞中有 個銅原子。
(4)鋁單質為面心立方晶體,其晶胞參數a=0.405nm,晶胞中鋁原子的配位數為 。列式表示鋁單質的密度 g·cm-3(不必計算出結果)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(13分)X、Y、Z、R為前四周期元素,且原子序數依次增大。XY2是紅棕色氣體;X與氫元素可形成XH3;Z基態原子的M層與K層電子數相等;R2+離子的3d軌道中有9個電子。請回答下列問題:
(1)Y基態原子的電子排布式是________;Z所在周期中第一電離能最大的主族元素是_____。
(2)XY2-離子的立體構型是_______;R2+的水合離子中,提供孤電子對的是原子是______。
(3)Z與某元素形成的化合物的晶胞如右圖所示,晶胞中陰離子與陽離子的個數之比是___________。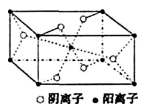
(4)將R單質的粉末加入XH3的濃溶液中,通入Y2,充分反應后溶液呈深藍色,該反應的離子方程式是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(8分)下圖是元素周期表的一部分,其中每個數字編號代表對應的一種元素。
| ① | | | ||||||
| | | | | ② | ③ | ④ | | |
| ⑤ | | ⑥ | ⑦ | | | ⑧ | ⑨ | |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com