
分析 (1)鐵的原子序數(shù)為26,在周期表中處于第四周期第VIII族;結(jié)構(gòu)亞鐵離子和鐵離子的電子排布式進行判斷;
(2)CO與N2結(jié)構(gòu)相似,應含有C≡O鍵;
②Ni的家電子數(shù)為10,每個配體提供一個電子對,根據(jù)10+2n=18計算;
(3)①影響離子晶體的因素有電荷因素和半徑因素;
②NaCl中鈉離子的配位數(shù)為6;
(4)根據(jù)化合價變化可知,氧化亞銅和稀硫酸反應生成硫酸銅、Cu和水,據(jù)此寫出反應的離子方程式;
(5)利用均攤法計算兩種金屬原子個數(shù)之比.
解答 解:(1)鐵為26號元素,元素在周期表中位于第四周期Ⅷ族;由于Fe2+的價電子3d6失去一個電子可形成3d5半充滿穩(wěn)定結(jié)構(gòu),所以Fe2+易被氧化成Fe3+,
故答案為:第四周期Ⅷ族;Fe2+的價電子3d6失去一個電子可形成3d5半充滿穩(wěn)定結(jié)構(gòu);
(2)①CO與N2結(jié)構(gòu)相似,含有C≡O鍵,含有1個σ鍵,2個π鍵,CO分子內(nèi)σ鍵與π鍵個數(shù)之比為1:2,
故答案為:1:2;
②Ni的家電子數(shù)為10,每個配體提供一個電子對,則10+2n=18,n=4,
故答案為:4;
(3)①Ni2+和Fe2+的離子半徑分別為69pm和78pm,離子半徑越小,離子鍵作用力越大,晶體的熔沸點越高,所以熔點NiO>FeO,
故答案為:>;
②NaCl中鈉離子和氯離子的配位數(shù)分別為6,NiO的晶體結(jié)構(gòu)類型與氯化鈉的相同,NiO晶胞中Ni和O的配位數(shù)分別為6,
故答案為:6;
(4)Cu2O與稀硫酸反應得到藍色溶液及一種單質(zhì),根據(jù)氧化還原反應中化合價變化可知,氧化亞銅和稀硫酸反應生成硫酸銅、Cu和水,反應的離子方程式為:Cu2O+2H+=Cu2++Cu+H2O,
故答案為:Cu2O+2H+=Cu2++Cu+H2O;
(5)在晶胞中,Au原子位于頂點,Cu原子位于面心,該晶胞中Au原子個數(shù)=8×$\frac{1}{8}$=1,Cu原子個數(shù)=6×$\frac{1}{2}$=3,所以該合金中Au原子與Cu原子個數(shù)之比=1:3,
故答案為:1:3.
點評 本題考查了金屬單質(zhì)及其化合物的綜合應用、晶體結(jié)構(gòu)與性質(zhì)、晶胞計算等知識,題目難度中等,試題知識點較多、綜合性較強,充分考查學生的分析、理解能力及靈活應用能力,注意掌握常見金屬單質(zhì)及其化合物的性質(zhì),明確均攤法在晶胞計算中的應用.


 小學期末沖刺100分系列答案
小學期末沖刺100分系列答案 期末復習檢測系列答案
期末復習檢測系列答案 超能學典單元期中期末專題沖刺100分系列答案
超能學典單元期中期末專題沖刺100分系列答案 黃岡360度定制密卷系列答案
黃岡360度定制密卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 3:4 | C. | 4:3 | D. | 9:8 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 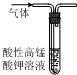 除去CO2中混有的SO2 | B. | 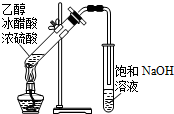 制取較純凈的乙酸乙酯 | ||
| C. | 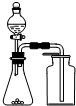 用生石灰和濃氨水制取氨氣 | D. | 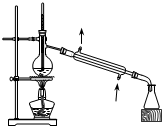 分離苯和四氯化碳的混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
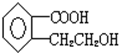
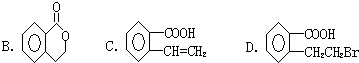
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 熔點:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:CHCl3>H2O>己烷 | |
| C. | 氫元素質(zhì)量分數(shù):甲烷>乙烷>乙烯>乙炔>苯 | |
| D. | 等質(zhì)量物質(zhì)完全燃燒耗O2量:苯>環(huán)已烷>已烷 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化劑和還原劑的物質(zhì)的量之比為1:8 | |
| B. | 該過程說明Fe(NO3)2溶液不宜加酸酸化 | |
| C. | 每1 mol NO3-發(fā)生氧化反應,轉(zhuǎn)移8 mol 電子 | |
| D. | 若把該反應設計為原電池,則負極反應為Fe2+-e-═Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氮氣的電子式: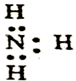 | B. | N2的結(jié)構(gòu)式:N≡N | ||
| C. | 乙酸的結(jié)構(gòu)簡式:C2H4O2 | D. | CH4分子的球棍模型: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在動力、設備、材料允許的條件下盡可能在高壓下進行 | |
| B. | 溫度越高越有利于工業(yè)合成氨 | |
| C. | 在工業(yè)合成氨中N2、H2的循環(huán)利用可提高其利用率,降低成本 | |
| D. | 及時從反應體系中分離出氨氣有利于平衡向正反應方向移動 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com