
【題目】草酸亞鐵晶體(FeC2O4·2H2O,M=180g/mol)呈淡黃色,可用于曬制藍圖。某實驗小組對其進行了一系列探究。
Ⅰ.純凈草酸亞鐵晶體熱分解產物的探究
(1)氣體產物成分的探究。小組成員采用如圖裝置進行實驗:
A.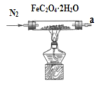 B.
B. C.
C. D.
D. E.
E.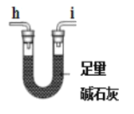
①按照氣流從左到右的方向,上述裝置的接口順序為a→g→f→___→尾氣處理裝置(儀器可重復使用)。
②檢查裝置氣密性后,先通入一段時間N2,其目的為__。
③實驗證明了氣體產物中含有CO,依據的實驗現象為__。
④結束實驗時先熄滅A、C處的酒精燈再停止通入N2,其目的是__。
(2)小組成員設計實驗證明了A中分解后的固體成分為FeO,則草酸亞鐵晶體分解的化學方程式為__。
(3)曬制藍圖時,草酸亞鐵晶體是感光劑,會失去結晶水轉化為FeC2O4,現以K3[Fe(CN)6]溶液為顯色劑,該顯色反應的化學方程式為__。
Ⅱ.草酸亞鐵晶體樣品純度的測定
工業制得的草酸亞鐵晶體中常含有FeSO4雜質,測定其純度的步驟如下:
步驟1:稱取mg草酸亞鐵晶體樣品并溶于稀H2SO4中,配成250mL溶液;
步驟2:取上述溶液25.00mL,用cmol·L-1KMnO4標準液滴定至終點,消耗標準液V1mL;
步驟3:向反應后溶液中加入適量鋅粉,充分反應后,加入適量稀H2SO4,再用cmol·L-1KMnO4標準溶液滴定至終點,消耗標準液V2mL。
(4)步驟2中滴定終點的現象為__;步驟3中加入鋅粉的目的為___。
(5)若步驟![]() 配制溶液時部分Fe2+被氧化變質,則測定結果將__(填“偏高”、“偏低”或“不變”)
配制溶液時部分Fe2+被氧化變質,則測定結果將__(填“偏高”、“偏低”或“不變”)
【答案】b→c→h→i(或i→h)→d→e((或e→d)→b→c 排盡裝置中的空氣,防止干擾實驗(防爆炸或干擾氣體的檢驗) c中固體由黑色變為紅色,后B裝置中出現渾濁 防止倒吸 FeC2O4·2H2O![]() FeO+CO↑+CO2↑+2H2O 3FeC2O4+2K3[Fe(CN)6]=Fe3[Fe(CN)6]2+3K2C2O4 錐形瓶中溶液顏色變為淺紫色(或淺紅色),且
FeO+CO↑+CO2↑+2H2O 3FeC2O4+2K3[Fe(CN)6]=Fe3[Fe(CN)6]2+3K2C2O4 錐形瓶中溶液顏色變為淺紫色(或淺紅色),且![]() 內不褪色 將Fe3+還原為Fe2+ 偏低
內不褪色 將Fe3+還原為Fe2+ 偏低
【解析】
I.在A中草酸亞鐵晶體(FeC2O4·2H2O)受熱發生分解反應:FeC2O4·2H2O![]() FeO+CO↑+CO2↑+2H2O,用D檢驗水蒸氣的存在,用B檢驗CO2氣體,然后用E干燥CO,將CO用通入C使CO與CuO發生反應:CO+CuO
FeO+CO↑+CO2↑+2H2O,用D檢驗水蒸氣的存在,用B檢驗CO2氣體,然后用E干燥CO,將CO用通入C使CO與CuO發生反應:CO+CuO![]() CO2+Cu,反應產生的CO2氣體通過B裝置檢驗,由于反應過程中有CO產生,會導致大氣污染,所以最后將氣體進行尾氣處理。用K3[Fe(CN)6]溶液檢驗溶液中的Fe2+,據此書寫反應方程式;
CO2+Cu,反應產生的CO2氣體通過B裝置檢驗,由于反應過程中有CO產生,會導致大氣污染,所以最后將氣體進行尾氣處理。用K3[Fe(CN)6]溶液檢驗溶液中的Fe2+,據此書寫反應方程式;
II.步驟2中向FeC2O4·2H2O、FeSO4溶解后的酸性溶液中滴入酸性KMnO4溶液,溶液中的Fe2+、H2C2O4都被氧化,Fe2+變為Fe3+;KMnO4被還原為無色的Mn2+;H2C2O4變為CO2氣體逸出;步驟3中向反應后溶液中加入適量鋅粉,Zn將溶液中Fe3+還原為Fe2+,充分反應后,加入適量稀H2SO4,再用 cmol/L KMnO4標準溶液滴定至終點,這時溶液中Fe2+氧化為Fe3+,消耗標準液V2mL。則前后兩次消耗的高錳酸鉀溶液的體積差就是氧化H2C2O4消耗的體積,根據C守恒可知n(H2C2O4)=n(FeC2O4·2H2O),最后根據電子守恒確定KMnO4與FeC2O4·2H2O的物質的量之間的關系,利用該反應消耗的n(KMnO4)計算出FeC2O4·2H2O的質量,從而可得其純度,據此分析。
Ⅰ.(1)①草酸亞鐵晶體在裝置A中加熱分解,生成的氣體通過裝置D中硫酸銅檢驗水蒸氣的存在,通過裝置B中澄清石灰水檢驗二氧化碳的生成,通過裝置E中堿石灰干燥氣體后通入裝置C中玻璃管中,和氧化銅反應生成銅和二氧化碳,再通過B裝置檢驗生成的二氧化碳氣體,按照氣流從左到右的方向,上述裝置正確連接的順序為:b→c→h→i(或i→h)→d→e((或e→d)→b→c,故答案為:b→c→h→i(或i→h)→d→e((或e→d)→b→c;
②實驗前先通入一段時間N2,其目的為:排盡裝置中的空氣,防止加熱時發生爆炸,故答案為:排盡裝置中的空氣,防止干擾實驗(防爆炸或干擾氣體的檢驗);
③實驗證明了氣體產物中含有CO,依據的實驗現象為:c中固體由黑色變為紅色,后B裝置中出現渾濁,故答案為:c中固體由黑色變為紅色,后B裝置中出現渾濁;
④為了防止倒吸,發生安全事故,結束實驗時先熄滅A、C處的酒精燈再停止通入N2,故答案為:防止倒吸;
(2)A處反應管中發生反應是草酸亞鐵晶體分解生成氧化亞鐵、一氧化碳、二氧化碳和水,反應的化學方程式為:FeC2O4·2H2O![]() FeO+CO↑+CO2↑+2H2O,故答案為:FeC2O4·2H2O
FeO+CO↑+CO2↑+2H2O,故答案為:FeC2O4·2H2O![]() FeO+CO↑+CO2↑+2H2O;
FeO+CO↑+CO2↑+2H2O;
(3)FeC2O4與反應K3[Fe(CN)6]生成藍色的Fe3[Fe(CN)6]2沉淀,同時生成K2 C2O4,該反應的化學方程式為:3FeC2O4+2K3[Fe(CN)6]=Fe3[Fe(CN)6]2+3K2C2O4,故答案為:3FeC
Ⅱ.(4) 在步驟2中用酸性KMnO4滴定含有Fe2+、H2C2O4的溶液,KMnO4被還原為無色的Mn2+,所以滴定終點的現象為錐形瓶中溶液顏色變為淺紫色,且30s內不褪色。在步驟3中加入鋅粉的目的為將溶液中的Fe3+氧化為Fe2+,以便于確定溶液H2C2O4的物質的量,并根據C元素守恒,計算出FeC2O4的物質的量,故答案為:滴入最后一滴溶液無色變化為紫紅色且半分鐘不變,說明反應進行到終點;將Fe3+還原為Fe2+;
(5)若步驟1配制溶液時部分Fe2+被氧化,消耗高錳酸鉀減少,計算得到亞鐵離子物質的量減小,測定結果偏低;故答案為:偏低。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】某學生欲在實驗室制備無水 FeCl3 并得到副產物 FeCl3 溶液。經查閱資料得知:無水 FeCl3 在空氣中易潮解,加熱易升華。如圖是他設計的實驗裝置圖(加熱及夾持裝置略去)
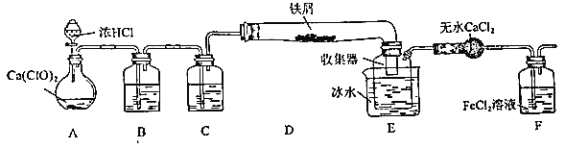
完成下列填空:
(1)裝置 A 是 Cl2 發生裝置,其中的化學反應方程式為_____
(2)B 中的溶液是_____,C 的作用是_____
(3)D 加熱后,少量生成 FeCl3 沉積在D 的右端,要使沉積的 FeCl3 進入E,操作是______________
E 中冰水的作用為_____
(4)實驗員老師對上述裝置提出了 2 點改進建議:一是裝置連接部分都改成標準玻璃接口,不用橡膠連接件的原因是_____;二是這套裝置還存在一個很大的缺陷,改進的方法是_______________
(5)證明 F中 FeCl2 未被完全氧化的方法是_____
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在0.2 L由NaCl溶液、MgCl2溶液、CuCl2溶液組成的混合溶液中,部分離子的濃度如圖所示。
(1)混合液中,NaCl的物質的量為_______mol,MgCl2的質量為_______g。
(2)該混合溶液中CuCl2的物質的量濃度為_____molL﹣1,將該混合溶液加水稀釋至體積為1 L,稀釋后溶液中Cu2+的物質的量濃度為_______molL﹣1。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20mL0.1mol·L-1的HA溶液中逐滴加入0.1mol·L-1的燒堿溶液,溶液中水所電離的c水(H+)隨加入燒堿溶液體積的變化如圖所示,下列說法正確的是( )
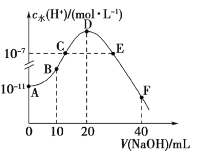
A.B點的溶液中粒子濃度之間存在:c(HA)>c(Na+)>c(A-)
B.由圖可知A-的水解平衡常數Kh約為1×10-9
C.C、E兩點因為對水的電離的抑制作用和促進作用相同,所以溶液均呈中性
D.F點的溶液呈堿性,粒子濃度之間存在:c(OH-)=c(HA)+c(A-)+c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】材料是人類文明進步的階梯,第ⅢA、ⅣA、ⅤA族元素是組成特殊材料的重要元素。請回答下列問題:
(1)基態Ge原子的核外電子有__種不同的空間運動狀態。
(2)P、S、Cl的第一電離能由大到小的順序為__。
(3)M與Ga位于同周期,M3+的一種配合物組成為[M(NH3)5(H2O)]Cl3。
①下列有關NH3、H2O的說法正確的是__(填字母)。
a.分子空間構型相同
b.中心原子雜化類型相同
c.鍵角大小相同
②1mol[M(NH3)5(H2O)]3+含__個σ鍵。
③配合物T與[M(NH3)5(H2O)]Cl3組成元素的種類和數目相同,中心離子的配位數相同。1molT溶于水,加入足量AgNO3溶液可生成2molAgCl。則T的化學式為___。
(4)如圖甲為硼酸晶體的片層結構,其中硼的雜化方式為__。H3BO3在熱水中比冷水中溶解度顯著增大的主要原因是__。
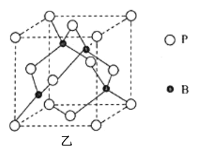
(5)磷化硼(BP)是一種超硬耐磨涂層材料,其晶胞結構如圖乙所示,該晶胞中B原子相連構成幾何體的空間構型為__(填“立方體”或“正四面體”或“正八面體”)。已知該晶體的密度為ρg·cm-3,NA是阿伏加德羅常數的值。BP晶胞中面心上6個P原子相連構成正八面體,該正八面體的邊長為__pm(列式即可)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知化學反應①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化學平衡常數為K1;化學反應②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化學平衡常數為K1;化學反應②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化學平衡常數為K2,在溫度973 K和1173 K的情況下,K1、K2的值分別如下:
FeO(s)+H2(g),其化學平衡常數為K2,在溫度973 K和1173 K的情況下,K1、K2的值分別如下:
溫度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)通過表格中的數值可以推斷:反應①是_______(填“吸熱”或“放熱”)反應。
(2)現有反應③:CO2(g)+H2(g)![]() CO(g)+H2O(g),請你寫出該反應的平衡常數K3的表達式:K3=______。
CO(g)+H2O(g),請你寫出該反應的平衡常數K3的表達式:K3=______。
(3)根據反應①與②可推導出K1、K2與K3之間的關系式為__________,據此關系式及上表數據,能推斷出反應③是________(填“吸熱”或“放熱”)反應。
(4)要使反應③在一定條件下建立的平衡向正反應方向移動,可采取的措施有______ 、_____ (填寫字母序號)。
A.縮小反應容器的容積 B.擴大反應容器的容積
C.升高溫度 D.使用合適的催化劑
E.設法減小平衡體系中的CO的濃度
(5)圖甲、乙分別表示反應③在t1時刻達到平衡,在t2時刻因改變某個條件而發生變化的情況:
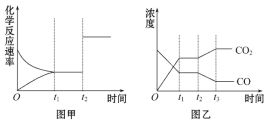
①圖甲中t2時刻發生改變的條件是__________。
②圖乙中t2時刻發生改變的條件是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學用語表達,正確的是
A.鈉投入水中的離子方程式: Na+2H2O=Na++2OH-+H2↑
B.一水合氨的電離方程式: NH3H2O![]() NH4++OH-
NH4++OH-
C.硫酸銅溶液和氫氧化鋇溶液反應的離子方程式反應:Ba2++SO42=BaSO4↓
D.氯氣溶于水的離子方程式:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組同學欲探究NH3的催化氧化反應,按如圖裝置進行實驗。A、B裝置可選用的藥品:濃氨水、H2O2溶液、蒸餾水、NaOH固體、MnO2。

(1)NH3催化氧化的化學方程式是____。
(2)甲、乙兩同學分別按如圖裝置進行實驗。一段時間后,裝置G中的溶液都變成藍色。
①甲觀察到裝置F中有紅棕色氣體,生成紅棕色氣體的化學方程式是___。
②乙觀察到裝置F中只有白煙生成,白煙的成分是___(填化學式)。
③用離子方程式解釋裝置G中溶液變成藍色的原因:___。
(3)為幫助乙實現在裝置F中也觀察到紅棕色氣體,如何改進___。
(4)為實現該反應,也可用如圖所示的裝置替換原裝置中虛線框部分。
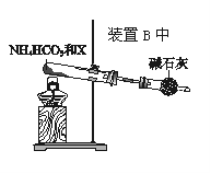
化合物X為__;NH4HCO3的作用是__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應A2(g) + B2(g)=2AB(g) 的能量變化如圖所示,下列敘述中正確的是( )
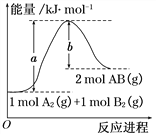
A.每生成2mol AB(g) 共吸收b kJ熱量
B.該反應熱ΔH = +(a-b) kJ·mol-1
C.反應物的總能量大于生成物的總能量
D.斷裂1 mol A—A鍵,放出a kJ能量
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com