
【題目】粉末狀試樣A是由等物質的量的MgO和Fe2O3組成的混合物。進行如下實驗:
①取適量A進行鋁熱反應,產物中有單質B生成;
②另取20 g A全部溶于0.15 L 6.0 mol·L-1鹽酸中,得溶液C;
③將①中得到的單質B和溶液C反應,放出1.12 L(標況)氣體,同時生成溶液D,還殘留有固體物質B;
④用KSCN溶液檢驗時,溶液D不變色。
請填空:
(1)①中引發鋁熱反應的實驗操作是___________,產物中的單質B是________。
(2)②中所發生的各反應的化學方程式是___________。
(3)③中所發生的各反應的離子方程式是___________。
(4)若溶液D的體積仍視為0.15 L,則該溶液中c(Mg2+)為________,c(Fe2+)為________。
【答案】加少量KClO3,插上鎂條并將其點燃 Fe Fe2O3+6HCl=2FeCl3+3H2O、MgO+2HCl=MgCl2+H2O Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑ 0.67 mol·L-1 2.3 mol·L-1
【解析】
(1)鋁熱反應是指單質Al和某些金屬氧化物發生的反應,反應過程中放出大量熱,但該反應需要較高的溫度才能引發。在混合物上加少量KClO3固體并插上Mg條,點燃Mg條后放出熱量,使KClO3固體分解放出O2,進一步加劇Mg的燃燒,可在短時間內使混合物溫度迅速升高,引發反應。發生的反應為Fe2O3+2Al![]() Al2O3+2Fe,所以產物中單質B為Fe,故答案為:加少量KClO3,插上鎂條并將其點燃;Fe;
Al2O3+2Fe,所以產物中單質B為Fe,故答案為:加少量KClO3,插上鎂條并將其點燃;Fe;
(2)Fe2O3和MgO都是堿性氧化物,能和酸反應生成鹽和水:Fe2O3+6HCl=2FeCl3+3H2O,MgO+2HCl=MgCl2+H2O,故答案為:Fe2O3+6HCl=2FeCl3+3H2O、MgO+2HCl=MgCl2+H2O;
(3)混合物中只有Fe2O3能和Al發生鋁熱反應,生成Fe單質。C溶液中有反應生成的FeCl3,還有未反應的HCl。發生的離子反應為Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑。
(4)假設步驟②用去的20 g固體中,MgO的物質的量為x,則Fe2O3的物質的量也為x,則40 g·mol-1×x+160 g·mol-1×x=20 g,解得:x=0.1 mol。根據MgO~MgCl2的關系,則溶液中MgCl2的濃度為0.1 mol÷0.15 L≈0.67 mol·L-1。步驟④說明溶液中沒有Fe3+,也就是溶質為FeCl2和MgCl2。根據Cl-守恒的關系,可知MgCl2和FeCl2的總的物質的量等于![]() =0.45mol,所以,FeCl2的濃度為
=0.45mol,所以,FeCl2的濃度為![]() ≈2.3 mol·L-1,故答案為:Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑;0.67 mol·L-1;
≈2.3 mol·L-1,故答案為:Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑;0.67 mol·L-1;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數,下列有關說法正確的是( )
A. 100mL12mol/L濃鹽酸與足量的MnO2加熱充分反應生成Cl2分子數為0. 3 NA
B. 80gSO3在標準狀況下所占體積約為22.4L
C. 向FeI2溶液中通入適量Cl2,當有1 mol Fe2+被氧化時,轉移的電子的數目為NA
D. 5.4g鋁粉與足量的氫氧化鈉溶液充分反應生成H2分子數為0. 3 NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2份50mL同樣的NaOH的溶液,分別向其中逐漸通入一定量的CO2,得到甲和乙 兩種溶液,在甲和乙溶液中分別逐漸加入1mol/LHCl的鹽酸溶液,產生的二氧化碳氣體(標準狀況)與所加入鹽酸的體積之間的關系如圖所示的關系。
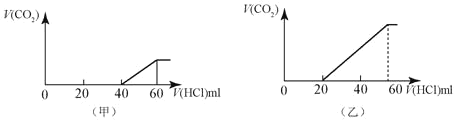
請回答下列問題:
(1)甲溶液中的溶質是____,其物質的量的比值是____。
(2)乙溶液中的溶質是____,其物質的量的比值是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高純硫酸錳作為合成鎳鈷錳三元正極材料的原料,工業上可由天然二氧化錳粉與硫化錳礦(還含Fe、Al、Mg、Zn、Ni、Si等元素)制備,工藝如下圖所示。回答下列問題:
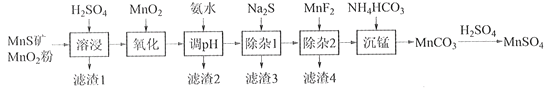
相關金屬離子[c0(Mn+)=0.1 mol·L1]形成氫氧化物沉淀的pH范圍如下:
金屬離子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
開始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“濾渣1”含有S和__________________________;寫出“溶浸”中二氧化錳與硫化錳反應的化學方程式____________________________________________________。
(2)“氧化”中添加適量的MnO2的作用是將________________________。
(3)“調pH”除鐵和鋁,溶液的pH范圍應調節為_______~6之間。
(4)“除雜1”的目的是除去Zn2+和Ni2+,“濾渣3”的主要成分是______________。
(5)“除雜2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度過高,Mg2+沉淀不完全,原因是_____________________________________________________________________。
(6)寫出“沉錳”的離子方程式___________________________________________________。
(7)層狀鎳鈷錳三元材料可作為鋰離子電池正極材料,其化學式為LiNixCoyMnz2,其中Ni、Co、Mn的化合價分別為+2、+3、+4。當x=y=![]() 時,z=___________。
時,z=___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物a為某種感冒藥的同系物,其結構簡式如圖所示,下列說法正確的是( )
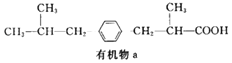
A.1mol有機物a最多可與4molH2發生加成反應
B.有機物a的化學式為C14H22O2
C.0.1mol有機物a與足量的NaHCO3溶液完全反應得到氣體的體積為2.24L
D.有機物a苯環上的二氯代物有4種(不含立體異構)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,利用培養皿探究NH3的性質。實驗時向NaOH固體上滴幾滴濃氨水,立即用另一表面皿扣在上面。下表中對實驗現象所做的解釋正確的是( )

選項 | 實驗現象 | 解釋 |
A | 濃鹽酸附近產生白煙 | NH3與濃鹽酸反應產生了NH4Cl固體 |
B | 濃硫酸附近無明顯現象 | NH3與濃硫酸不發生反應 |
C | 氯化物溶液變渾濁 | 該溶液一定是AlCl3溶液 |
D | 干燥紅石蕊試紙不變色,濕潤紅石蕊試紙變藍 | NH3是一種可溶性堿 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)室溫下,2g苯(C6H6)完全燃燒生成液態水和CO2,放出83.6kJ的熱量,寫出1molC6H6完全燃燒的熱化學方程式:______。
(2)已知:Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s)△H=+akJmol-1;C(s)+O2(g)=CO2(g)△H=-bkJmol-1,則2Fe(s)+
CO2(g)+2Fe(s)△H=+akJmol-1;C(s)+O2(g)=CO2(g)△H=-bkJmol-1,則2Fe(s)+![]() O2(g)=Fe2O3(s)的△H=________。
O2(g)=Fe2O3(s)的△H=________。
(3)已知幾種化學鍵的鍵能如表所示:
化學鍵 | Cl—Cl | F—F | Cl—F |
鍵能/ kJ·mol—1 | 242 | 159 | 172 |
則反應Cl2(g)+3F2(g)![]() 2ClF3(g)的△H=_____________ kJ·mol-1。
2ClF3(g)的△H=_____________ kJ·mol-1。
(4)如圖是乙烷、二甲醚燃燒過程中的能量變化圖。
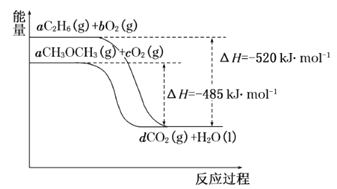
請回答下列問題:
①乙烷的燃燒熱ΔH=_______kJ·mol-1。
②根據題圖寫出二甲醚完全燃燒時的熱化學方程式__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】19.2 g Cu加入到100 mL一定濃度的硝酸溶液中,假定兩者恰好完全反應,同時產生標準狀況下8.96 L NO和NO2的混合氣體(忽略氣體的溶解及轉化)。求:
(1)混合氣體中NO和NO2的體積比。_____________
(2)硝酸溶液的物質的量濃度。__________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】探索CO和NO2這類化合物的特征及反應機理,對處理該類化合物的污染問題具有重要意義。回答下列問題:
I.CO可以與H2反應制備合成天然氣(SNG)。涉及反應如下:
CO甲烷化:CO(g)+3H2(g)CH4(g)+H2O(g)![]() 1=-206.2kJ·mol-1
1=-206.2kJ·mol-1
水煤氣變換:CO(g)+H2O(g)CO2(g)+H2(g)![]() 2=-41.2kJ·mol-1
2=-41.2kJ·mol-1
(1)反應CO2(g)+4H2(g) CH4(g)+2H2O(g)的![]() =_____kJ·mol-1。某溫度下,分別在起始體積相同的恒容容器A、恒壓容器B中加入1molCO2和4molH2的混合氣體,兩容器反應達平衡后放出或吸收的熱量較多的是_____(填“A”或“B”)。
=_____kJ·mol-1。某溫度下,分別在起始體積相同的恒容容器A、恒壓容器B中加入1molCO2和4molH2的混合氣體,兩容器反應達平衡后放出或吸收的熱量較多的是_____(填“A”或“B”)。
(2)在恒壓管道反應器中將原料氣H2和CO按一定比例通入,在催化劑作用下制備合成天然氣,400℃、p總為100kPa時反應體系平衡組成如表所示。
組分 | CH4 | H2O | H2 | CO2 | CO |
體積分數 | 45.0 | 42.5 | 10.0 | 2.00 | 0.500 |
該條件下CO的總轉化率α=______。若將管道反應器升溫至500℃,反應達到平衡后CH4的體積分數![]() ______45.0%(填“>”、“<”或“=”)。
______45.0%(填“>”、“<”或“=”)。
II.NO2可發生二聚反應生成N2O4,化學方程式為2NO2![]() N2O4。該反應達到平衡后,升高溫度可使體系顏色加深。
N2O4。該反應達到平衡后,升高溫度可使體系顏色加深。
(3)已知該反應的正反應速率方程為υ正=k正·c2(NO2),逆反應速率方程為υ逆=k逆·c(N2O4),其中k正、k逆分別為正、逆反應的速率常數。則右圖(lgk表示速率常數的對數;![]() 表示溫度的倒數)所示①、②、③、④四條斜線中,能表示lgk正隨
表示溫度的倒數)所示①、②、③、④四條斜線中,能表示lgk正隨![]() 變化關系的是斜線______,能表示lgk逆隨
變化關系的是斜線______,能表示lgk逆隨![]() 變化關系的是斜線______。
變化關系的是斜線______。
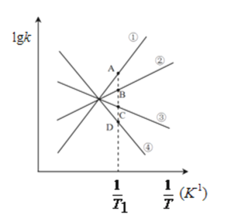
(4)圖中A、B、C、D點的縱坐標分別為a+1.5、a+0.5、a-0.5、a-1.5,則T1溫度時化學平衡常數K=______mol-1·L。已知T1溫度時,某時刻恒容密閉容器中NO2、N2O4濃度均為0.2mol·L-1,此時υ正______υ逆(填>或<);該反應達到平衡后,若將溫度從T1升高到T2重新達到平衡,則T1溫度時平衡壓強p(T1)______T2溫度時平衡壓強p(T2)(填“>”、“=”或“<”),原因是______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com