
【題目】一種由菱鎂礦(主要成分MgCO3、CaCO3、FeCO3、SiO2)制備高純氫氧化鎂的工藝如下:
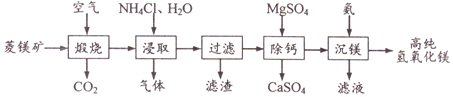
(1)“煅燒”時FeCO3發生反應的方程式為_____。
(2)“浸取”溫度100℃左右,該步驟含鎂化合物參與反應的化學方程式為______。
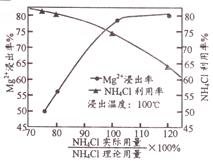
(3)“浸取”時NH4Cl用量對Mg2+浸出率的影響曲線如右圖所示。下列有關說法正確的____(填序號)。
A.“浸取”時適當攪拌漿料
B.用超理論用量20%的NH4Cl進行浸取
C.可用NH4Cl對浸取后的濾渣進行二次浸取,將兩次浸取液合并
D.浸出溫度采用100℃可促進NH4Cl的水解和NH3的逸出
(4)本工藝流程中可循環利用的物質有______。
(5)若要得到高純Mg(OH)2,需對“沉鎂”步驟所得的固體進行洗滌,檢驗固體已洗凈的方法是_______。
(6)25℃時,Ksp(CaSO4)=7.2×10-5。實驗測得“除鈣”前后溶液中c(Ca2+)分別為2.8g/L和0.8g/L,則1L溶液至少需加入MgSO4固體的質量為____g。
【答案】 4FeCO3+O2![]() 2Fe2O3+4CO2 MgO+2NH4Cl
2Fe2O3+4CO2 MgO+2NH4Cl![]() MgCl2+2NH3+H2O ACD NH4Cl、NH3 取最后一次洗滌濾液,加入硝酸酸化的BaCl2溶液,若無白色沉淀生成,則已洗凈 6.4g
MgCl2+2NH3+H2O ACD NH4Cl、NH3 取最后一次洗滌濾液,加入硝酸酸化的BaCl2溶液,若無白色沉淀生成,則已洗凈 6.4g
【解析】(1)菱鎂礦中含有FeCO3,“煅燒”時FeCO3與空氣中的氧氣發生氧化還原反應,反應的方程式為:4FeCO3+O2![]() 2Fe2O3+4CO2,答案為:4FeCO3+O2
2Fe2O3+4CO2,答案為:4FeCO3+O2![]() 2Fe2O3+4CO2
2Fe2O3+4CO2
(2)“浸取”時控制溫度100 ℃左右,此時由“煅燒”產生的MgO與NH4Cl的水溶液發生反應,反應的化學方程式為:MgO+2NH4Cl![]() MgCl2+2NH3↑+H2O,答案為:MgO+2NH4Cl
MgCl2+2NH3↑+H2O,答案為:MgO+2NH4Cl![]() MgCl2+2NH3↑+H2O
MgCl2+2NH3↑+H2O
(3)A. “浸取”時適當攪拌漿料增大接觸面積,有利于Mg2+浸出,A正確;B. 由圖像可知,當用超理論用量20%的NH4Cl進行浸取時,NH4Cl的利用率較低,B錯誤;C.用NH4Cl對浸取后的濾渣進行二次浸取,將兩次浸取液合并,能提高Mg2+浸出率,C正確;D. 浸出溫度采用100 ℃可促進NH4Cl的水解,導致酸性增強和NH3的逸出,有利于MgO被溶解,從而提高Mg2+浸出率,D正確。答案選ACD.
(4) 由菱鎂礦制備高純氫氧化鎂的工藝流程中用到NH4Cl和NH3,因此本工藝流程中NH4Cl和NH3可循環利用。答案為:NH4Cl和NH3
(5)檢驗Mg(OH)2固體已洗凈,只要檢驗洗滌液中沒有Cl-即可,因此檢驗固體已洗凈的方法是取最后一次洗滌濾液,加入硝酸酸化的BaCl2溶液,若無白色沉淀生成,則已洗凈。答案為:取最后一次洗滌濾液,加入硝酸酸化的BaCl2溶液,若無白色沉淀生成,則已洗凈。
(6)溶液中c(SO42-)=![]() =
=![]() =3.6
=3.6![]() mol·L-1, 1 L溶液生成的CaSO4為
mol·L-1, 1 L溶液生成的CaSO4為![]() =0.05mol,所以需要MgSO4固體的質量為3.6
=0.05mol,所以需要MgSO4固體的質量為3.6![]() mol·L-1×1 L×120g/mol+0.05 mol×120g/mol=6.4g,答案為:6.4
mol·L-1×1 L×120g/mol+0.05 mol×120g/mol=6.4g,答案為:6.4


科目:高中化學 來源: 題型:
【題目】ClO2是一種消毒、殺菌效率高、二次污染小的水處理劑。實驗室可通過以下反應制得:(已知H2C2O4中的碳為+3價)2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O。試回答下列問題。
(1)該反應中氧化產物的化學式是___________;被還原的元素是___________。
(2)用雙線橋標出上述反應的電子轉移情況______。
2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
(3)若反應共產生了4.48L氣體(標準狀況),則反應轉移電子的物質的量為_________mol,消耗還原劑的物質的量為___________mol。
(4)標準狀況下44.8mL的ClO2氣體恰好能與50mL 0.1mol·L-1的Na2SO3溶液液完全反應,生成Na2SO4,氯元素在產物中的化合價為___________;此過程說明ClO2具有____(填“氧化”或“還原”)性。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,兩圓圈相交的部分表示圓圈內的物質相互發生的反應。已知鈉及其氧化物的物質的量均為0.1 mol,水的質量為100 g。下列說法正確的是( )
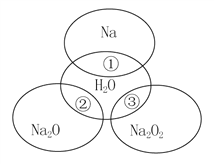
A. Na2O2中陰陽離子數目之比為1∶1
B. 反應①的離子方程式為Na+2H2O===Na++2OH-+H2↑
C. ①、②、③充分反應后所得溶液中溶質的質量分數:①>②>③
D. 反應③轉移電子的物質的量為0.1mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】丁苯酞是一種治療急性腦缺血的藥物,部分合成流程如下。下列說法正確的是( )
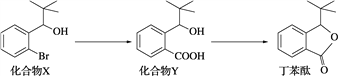
A. 化合物X、Y和丁苯酞三種分子中各含有1個手性碳原子
B. 化合物Y可以發生取代、加成和加聚反應
C. 可用Na2CO3溶液鑒別化合物X和化合物Y
D. 化合物X、Y和丁苯酞各1 mol最多消耗NaOH的量均為1 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】純堿(Na2CO3)在生產生活中具有廣泛的用途。
Ⅰ.以下是實驗室模擬制堿原理制取Na2CO3的流程圖。
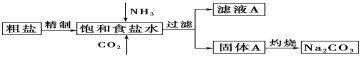
下表是四種物質在100g水中不同溫度的溶解度

(1)粗鹽中含有的雜質離子有Ca2+、Mg2+、SO42-等。精制除雜的步驟順序是a→________→________→________→b(填字母編號)。
a.粗鹽溶解,濾去沉渣 b.加入鹽酸調pH c.加入Ba(OH)2溶液
d.加入Na2CO3溶液 e.過濾
(2)向飽和食鹽水中先通入_______,后通入________,生成固體A的化學方程式為____
Ⅱ.制得的碳酸鈉樣品中往往含有少量NaCl,現欲測定樣品中Na2CO3的質量分數,某探究性學習小組分別設計了如下實驗方案.請回答下列有關問題:
方案一:把6g樣品溶解后加入過量的CaCl2溶液,將所得沉淀過濾、洗滌、烘干后得到5g固體。
(3)洗滌沉淀的具體操作是_____________________________。
(4)根據實驗中測得的有關數據,計算純堿樣品Na2CO3的質量分數為___________(結果保留小數點后一位)。
方案二:利用下圖所示裝置來測定純堿樣品中碳酸鈉的質量分數(鐵架臺、鐵夾等在圖中均已略去)。
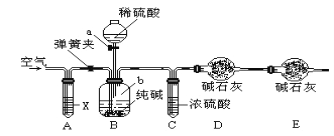
已知:堿石灰為氫氧化鈉和氧化鈣的混合物。
(5)實驗開始前應進行的操作是______________________________。
(6)儀器a的名稱為___________________,裝置A中試劑X應選用_________________。
(7)裝置E的作用是_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】日常生活中使用的購物袋的材料多為聚乙烯,下列說法中正確的是( )
A.用純凈的乙烯合成的聚乙烯是純凈物
B.聚乙烯可以人工合成,也是天然高分子化合物
C.聚乙烯能使酸性高錳酸鉀溶液褪色
D.合成聚乙烯的原料能夠使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】小龍同學在實驗室選用碘量法測定某磁鐵礦(主要成分是 Fe3O4,雜質SiO2、CuO)中鐵元素質量分數,實驗步驟如下:
①酸浸:取樣m g,先將礦石粉碎,加入足量2mol/LH2SO4浸取,過濾后得到浸取液;
②除雜:先向浸取液中加入足量 H2S溶液,過濾后加入足量酸性 H2O2溶液氧化Fe2+(過量的H2S轉化為S),再加入一定量MnO2固體除去過量的H2O2,一段時間后過濾得到Vml 濾液;
③定容:將濾液稀釋至250mL,取出25.00mL于帶塞子的錐形瓶中待用;
④轉化:向25.00mL溶液中加入足量KI固體,塞上塞子于暗處靜置30min;
⑤滴定:加入指示劑后,用cmol/LNa2S2O3標準溶液進行滴定至終點,消耗Na2S2O3標準溶液 V1mL;
⑥重復④⑤操作2次。 已知:2S2O32-+I2==S4O62-+2I-
1)①中將礦石粉碎的目的是____________________________________________,加入足量 H2SO4的目的是__________________________________。
2)寫出②中加入足量 H2S 溶液發生反應的離子反應方程式:_____________________________。
3)③中用______________________________ _(填儀器名稱)取出 25.00mL 溶液。
4)⑤中加入的指示劑是________,滴定終點的現象是:滴入最后一滴 Na2S2O3標準溶液 后,__________。⑥中重復進行實驗的目的是______。
5)該磁鐵礦中鐵元素質量分數為______________(用含 m、c、V1的代數式表示,需要化簡)。
6)若滴定過程中溶液 pH 過低則會導致測定結果______ (填“偏高”、“偏低”),寫出 導致這種誤差的離子反應方程式___________。
若②中過量的 H2O2溶液沒除則會導致測定結果_____(填“偏高”、“偏低”) 若②中 MnO2固體沒有過濾除去則會導致測定結果_________(填“偏高”、“偏低”)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com