
(07年天津卷)為達到預期的實驗目的,下列操作正確的是()
A.欲配制質量分數為10%的ZnSO4溶液,將l0 g ZnSO4?7H2O溶解在90 g水中
B.欲制備F(OH)3膠體,向盛有沸水的燒杯中滴加FeCl3飽和溶液并長時間煮沸
C.為鑒別KCl、AICl3和MgCl2溶液,分別向三種溶液中滴加NaOH溶液至過量
D.為減小中和滴定誤差,錐形瓶必須洗凈并烘干后才能使用
答案:C
解析:本題是對教材中的實驗進行綜合考查。A項中10gZnSO4?7H2O中所含的ZnSO4
小于10g,故其質量分數小于10%,A項錯誤。B項中制備Fe(OH)3膠體是向沸水中滴加FeCl3飽和溶液繼續煮沸即可,長時間煮沸則會導致生成的Fe(OH)3膠體凝聚而生成沉淀析出。C項中向三種溶液中滴加NaOH溶液至過量的現象分別是:無明顯現象;先生成白色沉淀后溶解消失;生成白色沉淀過量也不消失,故可以達到鑒別的目的。D項錐形瓶洗凈后不必烘干,因其不影響溶質的物質的量,對測定結果無影響。
高考考點:化學實驗原理的考查
易錯提醒:對教材中的實驗原理及操作注意事項不熟悉而誤選B、C、D。
備考提示:化學實驗原理及操作是高考的必考點,應系統復習。


 53天天練系列答案
53天天練系列答案科目:高中化學 來源: 題型:
① 將干燥的氯氣在110℃ ~ 140℃與硫反應,即可得S2C12粗品。
② 有關物質的部分性質如下表:
物質 | 熔點/℃ | 沸點/℃ | 化學性質 |
S | 112.8 | 444.6 | 略 |
S2C12 | -77 | 137 | 遇水生成HCl、SO2、S; 300℃以上完全分解; S2C12 + C12 |
設計實驗裝置圖如下:

⑴.上圖中氣體發生和尾氣處理裝置不夠完善,請你提出改進意見____________________________________________________________________________。
利用改進后的正確裝置進行實驗,請回答下列問題:
⑵.B中反應的離子方程式:_________________________________________________;
E中反應的化學方程式:_________________________________________________。
⑶.C、D中的試劑分別是__________________________、_______________________。
⑷.儀器A、B的名稱分別是____________、____________,F的作用是___________。
⑸.如果在加熱E時溫度過高,對實驗結果的影響是_____________________________,
在F中可能出現的現象是________________________________________________。
⑹.S2C12粗品中可能混有的雜質是(填寫兩種)______________、________________,為了提高S2C12的純度,關鍵的操作是控制好溫度和______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
① 將干燥的氯氣在110℃ ~ 140℃與硫反應,即可得S2C12粗品。
② 有關物質的部分性質如下表:
物質 | 熔點/℃ | 沸點/℃ | 化學性質 |
S | 112.8 | 444.6 | 略 |
S2C12 | -77 | 137 | 遇水生成HCl、SO2、S; 300℃以上完全分解; S2C12 + C12 |
設計實驗裝置圖如下:

⑴.上圖中氣體發生和尾氣處理裝置不夠完善,請你提出改進意見____________________________________________________________________________。
利用改進后的正確裝置進行實驗,請回答下列問題:
⑵.B中反應的離子方程式:_________________________________________________;
E中反應的化學方程式:_________________________________________________。
⑶.C、D中的試劑分別是__________________________、_______________________。
⑷.儀器A、B的名稱分別是____________、____________,F的作用是___________。
⑸.如果在加熱E時溫度過高,對實驗結果的影響是_____________________________,
在F中可能出現的現象是________________________________________________。
⑹.S2C12粗品中可能混有的雜質是(填寫兩種)______________、________________,為了提高S2C12的純度,關鍵的操作是控制好溫度和______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
(07年天津卷)(19分)二氯化二硫(S2C12)在工業上用于橡膠的硫化。為在實驗室合成S2C12,某化學研究性學習小組查閱了有關資料,得到如下信息:
① 將干燥的氯氣在110℃ ~ 140℃與硫反應,即可得S2C12粗品。
② 有關物質的部分性質如下表:
物質 | 熔點/℃ | 沸點/℃ | 化學性質 |
S | 112.8 | 444.6 | 略 |
S2C12 | -77 | 137 | 遇水生成HCl、SO2、S; 300℃以上完全分解; S2C12 + C12 |
設計實驗裝置圖如下:

利用改進后的正確裝置進行實驗,請回答下列問題:
⑴.上圖中氣體發生和尾氣處理裝置不夠完善,請你提出改進意見______。
⑵.B中反應的離子方程式:_________________________________________________;E中反應的化學方程式:_________________________________________________。
⑶.C、D中的試劑分別是__________________________、_______________________。
⑷.儀器A、B的名稱分別是____________、____________,F的作用是___________。
⑸.如果在加熱E時溫度過高,對實驗結果的影響是_____________________________,
在F中可能出現的現象是________________________________________________。
⑹.S2C12粗品中可能混有的雜質是(填寫兩種)______________、________________,為了提高S2C12的純度,關鍵的操作是控制好溫度和______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
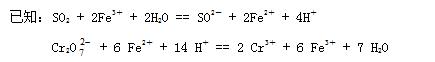
⑴.樣品中FeS2的質量分數是(假設雜質不參加反應)________________。
⑵.若灼燒6 g FeS2產生的SO2全部轉化為SO3氣體時放出9.83 kJ熱量,產生的SO3與水全部化合生成H2SO4 ,放出13.03 kJ熱量,寫出SO3氣體轉化為H2SO4的熱化學方程式:______________________________________________________________________。
⑶.煅燒10 t上述黃鐵礦,理論上產生SO2的體積(標準狀況)為_______________L,制得98%的硫酸質量為__________ t ,SO2全部轉化為H2SO4時放出的熱量是_______ kJ。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com