
【題目】氯化亞銅(![]() )在化工、印染、電鍍等行業應用廣泛。
)在化工、印染、電鍍等行業應用廣泛。![]() 微溶于水,不溶于醇和稀酸,可溶于
微溶于水,不溶于醇和稀酸,可溶于![]() 濃度較大的溶液,在潮濕空氣中易水解氧化。以海綿銅(主要成分是Cu和少量
濃度較大的溶液,在潮濕空氣中易水解氧化。以海綿銅(主要成分是Cu和少量![]() )為原料,采用硝酸銨氧化分解技術生產
)為原料,采用硝酸銨氧化分解技術生產![]() 的工藝過程如圖。回答下列問題:
的工藝過程如圖。回答下列問題:

(1)步驟①中N元素被還原為最低價,寫出此反應的離子方程式______________。
(2)步驟②中,亞硫酸銨要略保持過量,原因是___________,濾液中可循環利用的物質是__________。
(3)步驟⑤中,用“醇洗”可快速去除濾渣表面的水,防止濾渣被空氣氧化為![]() 被氧化為
被氧化為![]() 的化學方程式為______________________。
的化學方程式為______________________。
(4)用![]() 溶液測定氯化亞銅樣品純度(假設雜質不參與反應),步驟如下:準確稱取所制備的氯化亞銅樣品
溶液測定氯化亞銅樣品純度(假設雜質不參與反應),步驟如下:準確稱取所制備的氯化亞銅樣品![]() ,將其置于過量的
,將其置于過量的![]() 溶液中,待樣品完全溶解后,加入適量稀硫酸配成
溶液中,待樣品完全溶解后,加入適量稀硫酸配成![]() 溶液,取溶液
溶液,取溶液![]() 用
用![]() 溶液進行滴定,反應中
溶液進行滴定,反應中![]() 被還原成
被還原成![]() ,相關數據記錄如表所示:該樣品中
,相關數據記錄如表所示:該樣品中![]() 的質量分數__________________。
的質量分數__________________。
實驗編號 | 1 | 2 | 3 |
消耗 | 14.98 | 16.03 | 15.02 |
(5)制造印刷電路板產生的廢液中含大量![]() 等離子,利用膜電解技術對此廢液進行電解,電解裝置如圖所示。電解后的陰極液中加入適量鹽酸并用水稀釋可得到
等離子,利用膜電解技術對此廢液進行電解,電解裝置如圖所示。電解后的陰極液中加入適量鹽酸并用水稀釋可得到![]() ,電解時陰極的電極反應式為___________,生成
,電解時陰極的電極反應式為___________,生成![]() 的離子方程式為________________________________。
的離子方程式為________________________________。

【答案】![]() 使完全反應,阻止生成的被氧化 硫酸
使完全反應,阻止生成的被氧化 硫酸 ![]() 89.55%
89.55% ![]()
![]()
【解析】
銅與硝酸根和氫離子反應生成銅離子,加入亞硫酸銨和氯化銨生成硫酸、氯化亞銅等,過濾得到氯化亞銅,經水洗、醇洗、烘干等到氯化亞銅產品。
⑴步驟①中N元素被還原為最低價變為銨根離子,銅變為銅離子,因此反應的離子方程式;![]() ;故答案為:
;故答案為:![]() 。
。
⑵步驟②中,亞硫酸根具有還原性,銅離子具有氧化性,CuCl在潮濕空氣中易水解氧化,因此亞硫酸銨要略保持過量,原因是使完全反應,阻止生成的被氧化,Cu2+、Cl-、SO32和H2O反應CuCl、SO22、H+,因此濾液中可循環利用的物質是硫酸;故答案為:使完全反應,阻止生成的被氧化;硫酸。
⑶步驟⑤中,用“醇洗”可快速去除濾渣表面的水,防止濾渣被空氣氧化為![]()
![]() 與空氣中氧氣、水反應生成
與空氣中氧氣、水反應生成![]() 和HCl,其反應的的化學方程式為
和HCl,其反應的的化學方程式為![]() ;故答案為:
;故答案為:![]() 。
。
⑷三次消耗中第二次是錯誤數據,舍去,求另外兩次平均數為15.00mL,根據得失電子守恒關系得到n(CuCl)=6n(Cr2O72) = 6×0.1 molL1×0.015L = 0.009mol,該樣品中CuCl的質量分數![]()
⑸根據圖中信息,陰極![]() 得到電子變為
得到電子變為![]() 和
和![]() ,因此電解時陰極的電極反應式為
,因此電解時陰極的電極反應式為![]() ,電解后的陰極液中加入適量鹽酸并用水稀釋可得到CuCl,生成CuCl的離子方程式為
,電解后的陰極液中加入適量鹽酸并用水稀釋可得到CuCl,生成CuCl的離子方程式為![]() ;故答案為:
;故答案為:![]() 。
。


科目:高中化學 來源: 題型:
【題目】下列說法中錯誤的是
A. 從CH4、NH4+、SO42-為正四面體結構,可推測PH4+、PO43-也為正四面體結構
B. 1 mol金剛石晶體中,平均含有2 mol C—C鍵
C. 水的沸點比硫化氫的高,是因為H2O分子間存在氫鍵,H2S分子間不能形成氫鍵
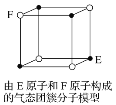
D. 某氣態團簇分子結構如圖所示,該氣態團簇分子的分子式為EF或FE
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積為2 L的恒容密閉容器中,一定溫度下,發生反應:aM(g)+bN(g)![]() cQ(g)。氣體M、N、Q的物質的量隨時間的變化如右圖所示,則下列敘述正確的是( )
cQ(g)。氣體M、N、Q的物質的量隨時間的變化如右圖所示,則下列敘述正確的是( )

A. 體系平衡時與反應起始時的壓強之比為3∶2
B. 平衡時,M的轉化率為50%,若條件改為恒溫恒壓,則達平衡時M的轉化率小于50%
C. 若開始時向容器中充入2 mol M和1 mol N,達到平衡時,M的體積分數小于50%
D. 在5 min時,再向體系中充入少量He,重新達到平衡前v(正)>v(逆)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四氫噻吩(![]() )是家用天然氣中人工添加的氣味添加劑具有相當程度的臭味。下列關于該化合物的說法正確的是( )
)是家用天然氣中人工添加的氣味添加劑具有相當程度的臭味。下列關于該化合物的說法正確的是( )
A.不能在O2中燃燒
B.![]() 所有原子可能共平面
所有原子可能共平面
C.![]() 與Br2的加成產物只有一種
與Br2的加成產物只有一種
D.生成1molC4H9SH至少需要2molH2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,在含有Pb2+、Sn2+的某溶液中,加入過量金屬錫(![]() ),發生反應:
),發生反應:![]()
![]()
![]() ,體系中c(Pb2+)和c(Sn2)變化關系如右圖所示。下列判斷正確的是
,體系中c(Pb2+)和c(Sn2)變化關系如右圖所示。下列判斷正確的是
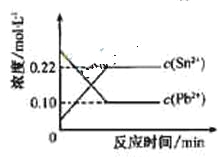
A.往平衡體系中加入少量金屬鉛后,c(Pb2+)增大
B.往平衡體系中加入少量![]() 固體后,c(Sn2-)變小
固體后,c(Sn2-)變小
C.升高溫度,平衡體系中c(Pb2+)增大,說明該反應![]()
D.25℃時,該反應的平衡常數K=2.2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醇催化氧化制取乙醛(沸點為20.8℃,能與水混溶)的裝置(夾持裝置已略)如圖所示:
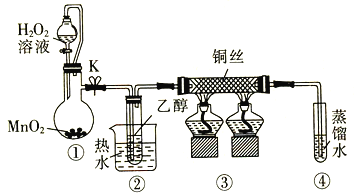
下列說法錯誤的是
A.向圓底燒瓶中滴入H2O2溶液前需打開K
B.實驗開始時需先加熱②,再通O2,然后加熱③
C.裝置③中發生的反應為2CH3CH2OH +O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D.實驗結束時需先將④中的導管移出。再停止加熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】自然界中的許多植物中含有醛,其中有些具有特殊香味,可作為植物香料使用,例如桂皮含肉桂醛(![]() ),杏仁含苯甲醛(
),杏仁含苯甲醛(![]() )。下列說法錯誤的是
)。下列說法錯誤的是
A. 肉桂醛和苯甲醛互為同系物
B. 肉桂醛能發生加成反應、取代反應和加聚反應
C. 可用新制氫氧化銅懸濁液檢驗肉桂醛分子中的含氧官能團
D. 1mol肉桂醛分子在一定條件下最多與5mol氫氣加成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮、磷、硼、砷的化合物用途非常廣泛。根據所學知識回答下列問題:
(1)如圖所示,每條折線表示周期表ⅣA-ⅦA中的某一族元素氫化物的沸點變化。每個小黑點代表一種氫化物,其中a、b、c、d、e對應元素電負性最大的是__(用元素符號表示),e點代表的第三周期某元素的基態原子核外電子占據的最高能層符號為__,該能層具有的原子軌道數為__。
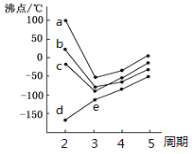
(2)已知反應:(CH3)3C-F+SbF5→(CH3)3CSbF6,該反應可生成(CH3)3C+,該離子中碳原子雜化方式有__。
(3)一種新型儲氫化合物氨硼烷是乙烷的等電子體,且加熱氨硼烷會慢慢釋放氫氣,推斷氨硼烷的結構式為__(若含有配位鍵,要求用箭頭表示)。
(4)PCl5是一種白色晶體,在恒容密閉容器中加熱可在148℃液化,形成一種能導電的熔體,測得其中含有一種正四面體形陽離子和一種正八面體形陰離子,熔體中P-Cl的鍵長只有198nm和206nm兩種,這兩種離子的化學式為__;正四面體形陽離子中鍵角大于PCl3的鍵角原因為___。
(5)砷化硼為立方晶系晶體,該晶胞中原子的分數坐標為:
B:(0,0,0);(![]() ,
,![]() ,0);(
,0);(![]() ,0,
,0,![]() );(0,
);(0,![]() ,
,![]() )
)
As:(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() )
)
①請在圖中畫出砷化硼晶胞的俯視圖__。
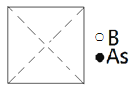
②與砷原子緊鄰的硼原子有__個,與每個硼原子緊鄰的硼原子有__個。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com