
下列對某些離子的檢驗及結論一定正確的是
A.先加入BaCl2溶液,產生白色沉淀,再加入HNO3溶液,白色沉淀不溶解,則溶液中一定含有大量的SO42﹣
B.用潔凈的鉑絲蘸取待測液,置于酒精燈火焰上灼燒,觀察到火焰呈黃色,則表明待測液中一定含有Na+而不含K+
C.加入鹽酸,能產生使澄清石灰水變渾濁的氣體,則溶液中一定含有CO32﹣
D.加入氯化鈉溶液,有白色沉淀產生,再加入稀硝酸沉淀不消失,一定有 Ag+
Ag+
 教學練新同步練習系列答案
教學練新同步練習系列答案 課前課后同步練習系列答案
課前課后同步練習系列答案科目:高中化學 來源:2016屆吉林省高三上學期第五次模擬理綜化學試卷(解析版) 題型:選擇題
化工生產中常用FeS作沉淀劑除去工業廢水中的Cu2+:Cu2+(aq)+FeS(s) CuS(s)+Fe2+(aq)下列有關敘述中正確的是( )
CuS(s)+Fe2+(aq)下列有關敘述中正確的是( )
①FeS的Ksp大于CuS的Ksp
②該反應平衡常數K=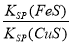
③溶液中加入少量Na2S固體后,溶液中c(Cu2+)、c(Fe2+)保持不變
④達到平衡時c(Fe2+)=c(Cu2+)
A.②③ B.①③④ C.①② D.②③④
查看答案和解析>>
科目:高中化學 來源:2015-2016學年廣西欽州港經濟開發區中學高二上12月月考化學試卷(解析版) 題型:選擇題
在水泥、冶金工廠常用高壓電對氣熔膠作用,以除去大量煙塵,減少對空氣的污染,此法應用的原理是
A.滲析 B.丁達爾現象 C.電泳 D.布朗運動
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一上學期12月月考化學試卷(解析版) 題型:選擇題
下列說法中正確的是
A.O2的摩爾質量是16g
B.堿性氧化物一定是金屬氧化物,酸性氧化物一定是非金屬氧化物
C.碳酸鈉溶液能使酚酞試液變紅,因此它是堿
D.雖然二氧化碳溶于水能導電,但它是非電解質
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江西省高二上學期12月月考化學試卷(教師版) 題型:選擇題
常溫下,將等體積、等物質的量濃度的NH4HCO3與NaCl溶液混合,析出部分NaHCO3晶體,過濾,所得濾液pH<7。下列關于濾液中的離子濃度關系不正確的是
A. 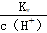 <1.0×10-7 mol/L
<1.0×10-7 mol/L
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-)
D.c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-)
查看答案和解析>>
科目:高中化學 來源:2014-2015學年江西省高三上學期第六次考試理綜化學試卷(解析版) 題型:填空題
甲醇可作為燃料電池的原料。工業上利用CO2和H2在一定條件下反應合成甲醇。
(1)已知在常溫常壓下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
寫出甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式: 。
(2)甲醇脫氫可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡轉化率隨溫度變化曲線如下圖所示。回答下列問題:
HCHO(g)+H2(g),甲醇的平衡轉化率隨溫度變化曲線如下圖所示。回答下列問題:
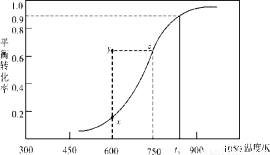
①600K時,Y點甲醇的υ(逆) (正)(填“>”或“<”)
②從Y點到X點可采取的措施是____________________________。
③有同學計算得到在t1K時,該反應的平衡常數為8.1mol·L-1。你認為正確嗎?請說明理由 。
(3)納米級Cu2O由于具有優良的催化性能而受到關注。在相同的密閉容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分別進行催化CH3OH的脫氫實驗:CH3OH(g) HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH的濃度(mol·L-1)隨時間t (min)變化如下表:
序號 | 溫度 | 0 | 10 | 20 | 30 | 40 | 50 |
① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
可以判斷:實驗①的前20 min的平均反應速率 ν(H2)= ;實驗溫度T1 T2(填“>”、“<”);催化劑的催化效率:實驗① 實驗②(填“>”、“<”)。
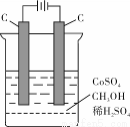
(4)電解法可消除甲醇對水質造成的污染,原理是:通電將Co2+氧化成Co3+,然后Co3+將甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。現用如下圖所示裝置模擬上述過程, 除去甲醇的離子方程式為 。
查看答案和解析>>
科目:高中化學 來源:2016屆福建省閩粵聯合體高三上學期第三次聯考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.7.1g氯氣與足量的氫氧化鈉溶液反應轉移的電子數為0.2×6.02×1023
B.V L a mol·L﹣1的氯化鐵溶液中,若Fe3+的數目為6.02×1023,則Cl﹣的數目大于3×6.02×1023
C.標準狀況下,22.4L NO和11.2L O2混合后氣體的分子總數為1.0×6.02×1023
D.工業用電解法進行粗銅精煉時,每轉移1mol電子,陽極上溶解的銅原子數為0.5×6.02×1023
查看答案和解析>>
科目:高中化學 來源:2016屆福建省高三上12月月考化學試卷(解析版) 題型:選擇題
下列圖示與對應的敘述相符的是
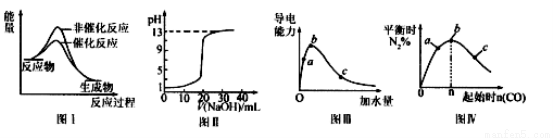
A.圖I表示某吸熱反應分別在有、無催化劑的情況下反應過程中的能量變化
B.圖Ⅱ表示常溫下,0. 100 mol/L NaOH溶液滴定20. 00 mL、0.100 mol/L HC1溶液所得到的滴定曲線
C.圖Ⅲ表示一定質量的冰醋酸加水稀釋過程中,醋酸溶液電離程度:c<a<b
D.圖Ⅳ表示反應4CO(g)+2NO2(g) N2(g)+4CO2(g),在其他條件不變的情況下改變起始物CO的物質的量,平衡時N2的體積分數變化情況,由圖可知的轉化率c>b>a
N2(g)+4CO2(g),在其他條件不變的情況下改變起始物CO的物質的量,平衡時N2的體積分數變化情況,由圖可知的轉化率c>b>a
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省高二上第三次月考化學試卷(解析版) 題型:填空題
FeCl3 具有凈水作用,但腐蝕設備,而聚合氯化鐵是一種新型的絮凝劑,處理污水比FeCl3 高效,且腐蝕性小。(已知25℃Ksp[Fe(OH)3]=4.0×10﹣38 lg2=0.3)
請回答下列問題:
(1)FeCl3 凈水的原理是____________ 。(用離子方程式表示),Fe3+水解生成的Fe(OH)3膠體粒子能吸附水中的懸浮雜質,常溫下此反應的平衡常數為_________________(填寫數值)。
(2)將FeCl3 溶液與NaHCO3 溶液混合,其離子方程式為 _______________。
(3)25℃時pH=3的溶液中,c(Fe3+)= mol•L﹣1要使Fe3+ 沉淀完全,pH應大于________。
(4)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反應的平衡常數K1、K2、K3由大到小的順序是 。
通過控制條件,以上水解產物聚合,生成聚合氧化鐵,離子方程式為:
xFe3++yH2O Fex(OH)y(3x-y)++yH+ 欲使平衡正向移動可采用的方法是(填序號) 。
Fex(OH)y(3x-y)++yH+ 欲使平衡正向移動可采用的方法是(填序號) 。
a.降溫 b.加水稀釋 c.加入NH4Cl d.加入NaHCO3
(5) FeCl3溶液可腐蝕印刷電路板,其反應為Cu +2FeCl3=CuCl2+2FeCl2 要將此反應設計在原電池中進行,則正極反應式為__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com