
 ,A→C的反應類型:加成反應.
,A→C的反應類型:加成反應.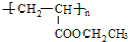 ,寫出D的同分異構體的結構簡式:CH3OCH3.
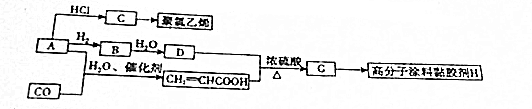
,寫出D的同分異構體的結構簡式:CH3OCH3.分析 A與HCl反應的生成物C能夠制取聚氯乙烯,可知A為CH≡CH,乙炔與HCl通過加成反應生成的C為CH2=CHCl,C發(fā)生加聚反應得到聚氯乙烯.乙炔與氫氣發(fā)生加成反應生成B為CH2=CH2,乙烯水化生成的D為CH3CH2OH,乙醇與CH2=CHCOOH發(fā)生酯化反應生成的G為CH2=CHCOOCH2CH3,G通過加聚反應生成高分子涂料H為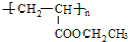 .乙炔與CO、水反應加成反應得到CH2=CHCOOH.
.乙炔與CO、水反應加成反應得到CH2=CHCOOH.
解答 解:A與HCl反應的生成物C能夠制取聚氯乙烯,可知A為CH≡CH,乙炔與HCl通過加成反應生成的C為CH2=CHCl,C發(fā)生加聚反應得到聚氯乙烯.乙炔與氫氣發(fā)生加成反應生成B為CH2=CH2,乙烯水化生成的D為CH3CH2OH,乙醇與CH2=CHCOOH發(fā)生酯化反應生成的G為CH2=CHCOOCH2CH3,G通過加聚反應生成高分子涂料H為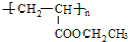 .乙炔與CO、水反應加成反應得到CH2=CHCOOH.
.乙炔與CO、水反應加成反應得到CH2=CHCOOH.
(1)A為CH≡CH,電子式為 ,A為CH≡CH,乙炔與HCl通過加成反應生成的C為CH2=CHCl,
,A為CH≡CH,乙炔與HCl通過加成反應生成的C為CH2=CHCl,
故答案為: ;加成反應;
;加成反應;
(2)H的結構簡式: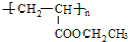 ,D為CH3CH2OH,D的同分異構體的結構簡式:CH3OCH3,
,D為CH3CH2OH,D的同分異構體的結構簡式:CH3OCH3,
故答案為: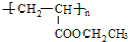 ;CH3OCH3;
;CH3OCH3;
(3)生成G的化學方程式:CH2=CHCOOH+CH3CH2OH$→_{△}^{濃硫酸}$CH2=CHCOOCH2CH3+H2O,
故答案為:CH2=CHCOOH+CH3CH2OH$→_{△}^{濃硫酸}$CH2=CHCOOCH2CH3+H2O;
(4)若要除去甲烷中混有的B(乙烯)氣體,可將混合氣體通入酸性高錳酸鉀溶液中,D可由葡萄糖在酶的作用下產生,葡萄糖屬于還原性糖,而蔗糖不是還原性糖,若要鑒別葡萄糖與蔗糖可選用的化學試劑是:新制的氫氧化銅濁液,
故答案為:酸性高錳酸鉀溶液;新制的氫氧化銅濁液;
(5)D(乙醇)也可由有機物C4H8O2在氫氧化鈉溶液加熱的條件下生成,是乙酸乙酯發(fā)生水解反應,該反應的化學方程式:CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH,
故答案為:CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH.
點評 本題考查有機物的推斷,注意根據有機物的結構進行推斷,需要學生熟練掌握官能團的性質與轉化,難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 鹵代烴中鹵原子的檢驗:先加NaOH溶液、加熱、冷卻后加AgNO3溶液 | |
| B. | 乙烷中有乙烯可KMnO4溶液洗氣,除去雜質 | |
| C. | 碳原子數小于10,且一氯代物只有一種的烷烴有3種 | |
| D. | 可用水鑒別苯和四氯化碳 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不能自發(fā)進行的氧化還原反應,通過電解的原理可以實現 | |
| B. | 電鍍時保持電流恒定,升高溫度不改變電解反應速率 | |
| C. | 電解精煉銅電解槽底部會形成含少量Ag、Fe、Pt等金屬的陽極泥 | |
| D. | 氫氧燃料電池是一種不需要將還原劑和氧化劑全部儲藏在電池內的新型發(fā)電裝置 | |
| E. | MnO2的生產方法之一是以石墨為電極,電解酸化的MnSO4溶液,若電解電路中通過2mol電子,MnO2的理論產量為1mol | |
| F. | 燃料電池是將燃料燃燒所放出的能量轉化為化學能的裝置 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2+X2═2HX | B. | X2+H20═HX+HXO | ||
| C. | NaX+AgNO3═AgX↓+NaNO3 | D. | 2NaX+H2SO4(濃)═Na2SO4+2HX |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2>Fe3+>Cu2+>PbO2 | B. | PbO2>Cl2>Fe3+>Cu2+ | ||
| C. | Fe3+>Cu2+>PbO2>Cl2 | D. | Cu2+>Fe3+>Cl2>PbO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
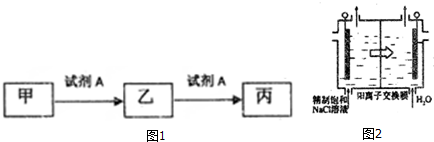
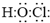 .二氧化氯還能溶于強堿溶液,該過程中發(fā)生反應生成等物質的量的氯酸鈉(NaClO3)和另一種氯的含氯酸鹽,同時生成水,該反應的離子方程式為2ClO2+2OH-═ClO3-+ClO2-+H2O
.二氧化氯還能溶于強堿溶液,該過程中發(fā)生反應生成等物質的量的氯酸鈉(NaClO3)和另一種氯的含氯酸鹽,同時生成水,該反應的離子方程式為2ClO2+2OH-═ClO3-+ClO2-+H2O查看答案和解析>>
科目:高中化學 來源: 題型:解答題
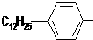
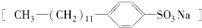 是常用洗滌劑的主要成分.其結構可用圖形
是常用洗滌劑的主要成分.其結構可用圖形 來表示,•端為鏈烴基,O端為極性基.根據這一結構特點,試分析和回答下列問題:
來表示,•端為鏈烴基,O端為極性基.根據這一結構特點,試分析和回答下列問題: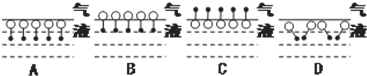
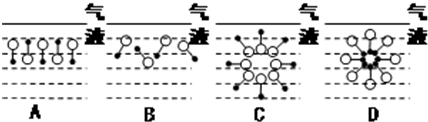
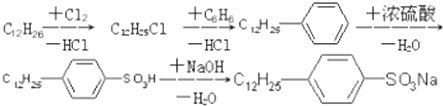
 .
.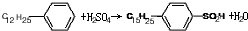 ,反應類型為取代反應.
,反應類型為取代反應.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不同元素的原子發(fā)生躍遷時,會釋放不同的光 | |
| B. | 第一電離能與電負性的數值都是以氣態(tài)中性基態(tài)原子為研究對象測得到 | |
| C. | 分子中的原子有固定的空間位置,組成完全相同的分子,由于原子位置的不同會表現出不同的性質 | |
| D. | 兩個相同的原子的任意未成對電子的電子云在兩個原子核間重疊,形成非極性共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com