
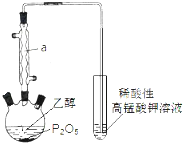
 已知用P2O5作催化劑,加熱乙醇可制備乙烯,反應溫度為80℃~210℃.某研究性小組設計了如下的裝置制備并檢驗產生的乙烯氣體(夾持和加熱儀器略去).
已知用P2O5作催化劑,加熱乙醇可制備乙烯,反應溫度為80℃~210℃.某研究性小組設計了如下的裝置制備并檢驗產生的乙烯氣體(夾持和加熱儀器略去).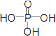 )
) ,
, ;
; ,
, ;
;

科目:高中化學 來源: 題型:
| A、常溫常壓下,0.1NA個HCl分子的體積為2.24L |
| B、標準狀況下,22.4L 氖氣含有2NA 個原子 |
| C、1L 0.2mol/L 硫酸鐵溶液中含有的SO42- 離子數目為0.2 NA |
| D、1 mol氖中含有的電子數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、可以根據PbI2和AgCl的Ksp的大小比較兩者的溶解度 |
| B、常溫下,同濃度的Na2S與NaHS溶液相比,NaHS溶液的pH大 |
| C、等物質的量濃度的CH3COONH4溶液和NH4HSO4溶液,前者的c(NH4+)小 |
| D、用惰性電極電解飽和NaCl溶液,若有1.0 mol電子轉移,則理論生成1.0 mol NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:
 在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等離子.試分析回答下列問題:
在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等離子.試分析回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:

| A、增大Z的濃度 |
| B、減小X的濃度 |
| C、增大壓強 |
| D、減小壓強 |
查看答案和解析>>
科目:高中化學 來源: 題型:
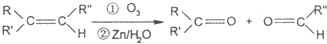
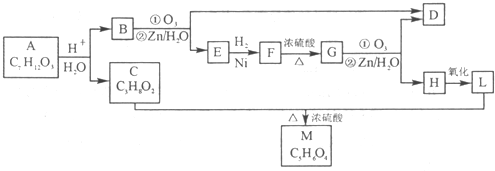
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、所得溶液中由水離出的C(OH-)=1.0×10-13mol?L-1 |
| B、所加燒堿溶液的pH=13 |
| C、所得溶液中C(Mg2+)=5.6×10-10mol?L-1 |
| D、在整個反應過程中,H2O的電離度在逐漸減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、欲配制質量分數為10%的ZnSO4溶液,將5g ZnSO4溶解在45g水中 |
| B、在25℃溫度條件下,配制100g溶解度為25g的NaCl飽和溶液,將25g的NaCl溶解在75g水中 |
| C、加熱蒸發質量分數為10%的鹽酸,可得到質量分數為36.5%的濃鹽酸 |
| D、向25℃的飽和CuSO4溶液中加入CuSO4粉末,制備CuSO4?5H2O晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、NaHSO4 |
| B、NaCl |
| C、HCl |
| D、Ba(OH)2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com