
無機化合物可根據其組成和性質進行分類。
(1)如圖所示的物質分類方法是 。
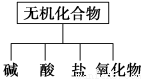
(2)以Na、K、H、O、C、S、N中任兩種或三種元素組成合適的物質,分別填在下表②③⑥的后面。
物質類別 | 酸 | 堿 | 鹽 | 氧化物 |
化學式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O2 |
(3)寫出⑦轉化為⑤的化學方程式: 。
(4)呼吸面具中用⑧作為O2來源的反應原理為: 。
(5)實驗室制備⑦常用 和 反應,檢驗該氣體的方法是 。
(1)樹狀分類法
(2)②H2SO4 ③NaOH ⑥K2CO3(合理即可)
(3)2NaOH+CO2=Na2CO3+H2O
(4)2Na2O2+2CO2=2Na2CO3+O2(或2Na2O2+2H2O=4NaOH+O2↑)
(5)CaCO3 稀鹽酸 把生成的無色無味氣體通入澄清石灰水,若變渾濁,則生成的氣體為CO2
【解析】(1)常見的分類法有兩種:交叉分類法和樹狀分類法,圖為樹狀分類法。(2)酸可填寫H2S、H2SO4、HNO3、H2CO3、H2SO3中的一種,堿可填寫KOH、NaOH、NH3·H2O中的一種,鹽可填寫K2SO4、K2CO3、NH4NO3、Na2SO4、Na2CO3、Na2SO3等中的一種。(3)CO2是酸性氧化物,可與NaOH反應生成Na2CO3和H2O。(4)Na2O2和H2O、CO2反應都能產生O2。(5)CaCO3和稀鹽酸反應,產生的CO2氣體可用澄清石灰水來檢驗。


 名牌學校分層周周測系列答案
名牌學校分層周周測系列答案 黃岡海淀全程培優測試卷系列答案
黃岡海淀全程培優測試卷系列答案科目:高中化學 來源:2014年高考化學蘇教版總復習 1-1 物質的分類、轉化及分散系練習卷(解析版) 題型:填空題
在如下圖所示的有關物質轉化關系中,各物質均是我們中學化學所學的物質。C為一種黑色粉末,D為一種氣體。
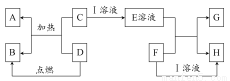
請根據框圖中物質的轉化關系及相關信息,用化學式填寫下列空白:
(1)若F為可溶性堿,G為藍色沉淀,則A為 ;D可能為 。
(2)若G為藍色沉淀,H為難溶性鹽,則I為 。
(3)若G、H都屬于鹽,且G為藍色溶液,則I可能為 ;F可能為 。
查看答案和解析>>
科目:高中化學 來源:2014年高考化學蘇教版一輪復習3-1鈉、鎂及其化合物練習卷(解析版) 題型:選擇題
物質的量為0.10 mol的鎂條在只含有CO2和O2混合氣體的容器中燃燒(產物不含碳酸鎂),反應后容器內固體物質的質量不可能為 ( )。
A.3.2 g B.4.0 g C.4.2 g D.4.6 g
查看答案和解析>>
科目:高中化學 來源:2014年高考化學蘇教版一輪復習2-2電解質 離子反應練習卷(解析版) 題型:填空題
離子反應是中學化學中重要的反應類型。回答下列問題:
(1)在發生離子反應的反應物或生成物中,一定存在有 (填序號)。
①單質;②氧化物;③電解質;④鹽;⑤化合物
(2)可用圖示的方法表示不同反應類型之間的關系。如分解反應和氧化還原反應可表示為下圖。請在下面的方框中畫出離子反應、置換反應和氧化還原反應三者之間的關系。


(3)離子方程式是重要的化學用語。下列是有關離子方程式的一些錯誤觀點,請在下列表格中用相應的“離子方程式”否定這些觀點。
①所有的離子方程式均可以表示一類反應 |
|
②酸堿中和反應均可表示為H++OH-=H2O |
|
③離子方程式中凡是難溶性酸、堿、鹽均要標“↓”符號 |
|
(4)試列舉出三種不同類別的物質(酸、堿、鹽)之間的反應,它們對應的離子方程式都可用“Ba2++SO42-=BaSO4↓”來表示,請寫出有關反應的化學方程式(3個):
① ;
② ;
③ 。
查看答案和解析>>
科目:高中化學 來源:2014年高考化學蘇教版一輪復習2-2電解質 離子反應練習卷(解析版) 題型:選擇題
常溫下,下列各組離子在指定溶液中一定能大量共存的是 ( )。
A.1.0 mol·L-1的KNO3溶液中:H+、Fe2+、Cl-、SO42-
B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO-
C.能使pH試紙變紅的溶液中:K+、Ba2+、AlO2-、Cl-
D.pH=0的溶液中:Mg2+、Na+、F-、SO42-
查看答案和解析>>
科目:高中化學 來源:2014年高考化學蘇教版一輪復習2-1物質的分類與轉化 分散系練習卷(解析版) 題型:選擇題
下列說法正確的是 ( )。
A.石油裂解、煤的氣化、海水制鎂等過程中都包含化學變化
B.可通過電解熔融MgCl2來制取金屬鎂,故也能通過電解熔融AlCl3來制取鋁
C.鋁熱劑、鹽酸、水玻璃、雙氧水、明礬均為混合物
D.Na2O2、MgCl2、NaOH、NH4Cl均為含共價鍵的離子化合物
查看答案和解析>>
科目:高中化學 來源:2014年高考化學蘇教版一輪復習1-2-2溶液的配制及誤差分析練習卷(解析版) 題型:填空題
在標準狀況下,將224 L HCl氣體溶于635 mL水中,所得鹽酸的密度為1.18 g·cm-3。試計算:
(1)所得鹽酸的質量分數和物質的量濃度分別是 、 。
(2)取出這種鹽酸100 mL,稀釋至1.18 L,所得稀鹽酸的物質的量濃度是 。
(3)在40.0 mL 0.065 mol·L-1 Na2CO3溶液中,逐漸加入(2)所稀釋的稀鹽酸,邊加邊振蕩。若使反應不產生CO2氣體,加入稀鹽酸的體積最多不超過 mL。
(4)將不純的NaOH樣品1 g(樣品含少量Na2CO3和水),放入50 mL 2 mol·L-1的鹽酸中,充分反應后,溶液呈酸性,中和多余的酸又用去40 mL 1 mol·L-1的NaOH溶液。蒸發中和后的溶液,最終得到 克固體。
查看答案和解析>>
科目:高中化學 來源:2014年高考化學蘇教版一輪復習1-2-1物質的量 氣體摩爾體積練習卷(解析版) 題型:選擇題
下列有關氣體體積的敘述中,正確的是 ( )。
A.在一定的溫度和壓強下,各種氣態物質體積的大小由氣體分子的大小決定
B.在一定的溫度和壓強下,各種氣態物質體積的大小由物質的量的多少決定
C.不同的氣體,若體積不同,則它們所含的分子數一定不同
D.氣體摩爾體積是指1 mol任何氣體所占的體積約為22.4 L
查看答案和解析>>
科目:高中化學 來源:2014年高考化學考前題型專練 保溫訓練(三)(解析版) 題型:選擇題
短周期元素X、Y、Z、W的原子序數依次增大,它們原子的最外層電子數之和為14。X與Z同主族,Y與W同主族,且X的原子半徑小于Y。下列敘述正確的是( )。
A.Y的簡單陰離子半徑小于Z的簡單陽離子半徑
B.Y與X形成的化合物沸點高于W與X形成的化合物的沸點
C.X2Y2加入酸性高錳酸鉀溶液中,X2Y2作氧化劑
D.W元素的最高價氧化物對應的水化物是弱酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com