
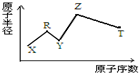
 現有短周期主族元素X、Y、Z、R、T.R原子最外層電子數是電子層數的2倍;Y與Z能形成Z2Y、Z2Y2型離子化合物,Z與T形成的Z2T 化合物能破壞水的電離平衡.六種元素的原子半徑與原子序數的關系如圖所示.下列推斷正確的是( )
現有短周期主族元素X、Y、Z、R、T.R原子最外層電子數是電子層數的2倍;Y與Z能形成Z2Y、Z2Y2型離子化合物,Z與T形成的Z2T 化合物能破壞水的電離平衡.六種元素的原子半徑與原子序數的關系如圖所示.下列推斷正確的是( )| A. | 原子半徑和離子半徑均滿足:Y<Z | |
| B. | 氫化物的沸點排序:Y>T>R | |
| C. | 最高價氧化物對應的水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四種元素組成的化合物水溶液一定顯堿性 |
分析 R原子最外層電子數是電子層數的2倍,可能為C或S,由于圖示原子半徑和原子序數關系可知R應為C;Y與Z能形成Z2Y、Z2Y2型離子化合物,應為Na2O、Na2O2,則Y為O,Z為Na;Z與T形成的Z2T化合物能破壞水的電離平衡,T應為S,Na2S水解呈堿性,可促進水的電離;X的原子半徑最小,原子序數最小,應為H元素,結合對應單質、化合物的性質以及題目要求解答該題.
解答 解:R原子最外層電子數是電子層數的2倍,可能為C或S,由于圖示原子半徑和原子序數關系可知R應為C;Y與Z能形成Z2Y、Z2Y2型離子化合物,應為Na2O、Na2O2,則Y為O,Z為Na;Z與T形成的Z2T化合物能破壞水的電離平衡,T應為S,Na2S水解呈堿性,可促進水的電離;X的原子半徑最小,原子序數最小,應為H元素.
A.原子半徑O>Na,離子半徑O2->Na+,故A錯誤;
B.Y、T、R的簡單氫化物分別為H2O、H2S、CH4,水分子之間存在氫鍵,沸點最高,硫化氫相對分子質量大于甲烷的,分子間作用力較甲烷的強,故硫化氫的沸點高于甲烷的,故沸點H2O>H2S>CH4,故B正確;
C.非金屬性S>C,元素的非金屬性越強,對應的最高價氧化物的水化物的酸性越強,故C錯誤;
D.由H、C、O、Na四種元素組成的化合物不僅僅為NaHCO3,可能為有機鹽且含有羧基,溶液不一定為堿性,可能為酸性,故D錯誤.
故選B.
點評 本題考查結構性質位置關系應用,側重于學生的分析能力的考查,推斷元素是解題的關鍵,D為易錯點,學生容易忽略有機物,難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①②③④⑤⑥ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | |
| C | D | E |
| A. | 原子半徑:C<D<E | |
| B. | 金屬性:A>C | |
| C. | 氫氧化物的化學式及其堿性:COH>D(OH)2>E(OH)3 | |
| D. | 最外層電子數:A>B |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 將漫射日光照射到裝有氯氣和甲烷混合氣體(體積比為4:1)的裝置上(如圖).現列出如下現象,其中正確的是( )
將漫射日光照射到裝有氯氣和甲烷混合氣體(體積比為4:1)的裝置上(如圖).現列出如下現象,其中正確的是( )| A. | ① | B. | ①④和⑤ | C. | ①和⑤ | D. | ②和⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質 | MgO | CaO | ZnCl2 | ZnBr2 |
| 干燥效率 | 0.008 | 0.2 | 0.8 | 1.1 |
| A. | MgO 的干燥性能比CaO差 | |
| B. | 干燥效率可能與干燥劑的陰陽離子半徑大小有關 | |
| C. | MgCl2可能是比CaCl2更好的干燥劑 | |
| D. | 上述干燥劑中陽離子對干燥性能的影響比陰離子大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
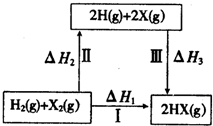
| A. | 2H(g)+2X(g)═2HX(g)△H3<0 | |
| B. | 途徑Ⅰ生成HX的反應熱與途徑無關,所以△H1=△H2+△H3 | |
| C. | 途徑Ⅰ生成HCl放出的熱量比生成HBr的多,說明HCl比HBr穩定 | |
| D. | Cl、Br、I的非金屬性依次減弱,所以途徑Ⅱ吸收的熱量依次增多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 15 | B. | 14 | C. | 13 | D. | 10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯是重要的化工原料 | |
| B. | 甲烷和乙烯互為同系物 | |
| C. | 甲烷和乙烯可以用溴水加以鑒別 | |
| D. | 甲烷是最簡單的有機物,是天然氣的主要成分 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com