
| 64 |
| 80 |
| 64 |
| 80 |
| 0.24g |
| 0.34g |


 培優好卷單元加期末卷系列答案
培優好卷單元加期末卷系列答案科目:高中化學 來源: 題型:
| A、該反應屬于置換反應 |
| B、N2H4是氧化劑 |
| C、N2O4是還原劑 |
| D、N2既是氧化產物又是還原產物 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、原電池工作時,正極和負極上不一定都發生氧化還原反應 | |||
B、xLi+Li1-xNiO2
| |||
| C、在鉛、銀和鹽酸構成的原電池工作時,鉛板上有5.175 g鉛溶解,正極上就有1120 mL(標準狀況)氣體析出 | |||
| D、在理論上可將該反應:CH4(g)+2O2(g)→CO2(g)+H2O(l)△H<0,設計成原電池 |
查看答案和解析>>
科目:高中化學 來源: 題型:
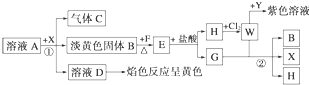
查看答案和解析>>
科目:高中化學 來源: 題型:
 研究和開發CO2和CO的創新利用是環境保護和資源利用雙贏的課題.
研究和開發CO2和CO的創新利用是環境保護和資源利用雙贏的課題.查看答案和解析>>
科目:高中化學 來源: 題型:
 短周期主族元素A、B、C、D、E在元素周期表中的位置如圖所示,其中A為地殼中含量最高的金屬元素.
短周期主族元素A、B、C、D、E在元素周期表中的位置如圖所示,其中A為地殼中含量最高的金屬元素.查看答案和解析>>
科目:高中化學 來源: 題型:
| A、向鹽酸中滴加氨水的過程,可能滿足c(H+)>c(NH4+) |
| B、0.1mol/L的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| C、等濃度的NaClO、NaHCO3混合溶液中:c(Na+)=c(ClO?)+c(HClO)+c(HCO3-)+c(H2CO3)+c(CO32-) |
| D、濃度均為0.1mol/L的HA(一元弱酸)和NaA溶液等體積混合后,若溶液呈酸性,則c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com