
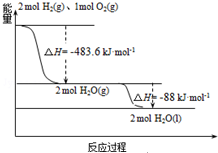
 發射用的運載火箭使用的是以液氫為燃燒劑,液氧為氧化劑的高能低溫推進劑,已知:
發射用的運載火箭使用的是以液氫為燃燒劑,液氧為氧化劑的高能低溫推進劑,已知:| A. | H2(g)與O2(g)反應生成H2O(g)放熱483.6kJ•mol-1 | |
| B. | 氫氣的燃燒熱為△H=-241.8 kJ•mol-1 | |
| C. | 火箭中液氫燃燒的熱化學方程式為:2H2(l)+O2(l)═2H2O(g)△H=-474.92kJ•mol-1 | |
| D. | H2O(g)=H2O(l)△H=-88kJ•mol-1 |
分析 A.由圖象分析,2mol H2(g)與1mol O2(g)反應生成2mol H2O(g)放出483.6kJ的熱量;
B.氫氣的燃燒熱是指1mol氫氣完全燃燒生成液態水放出的熱量;
C.由圖象分析,2H2(g)+O2(g)═H2O(l)△H1=-483.6kJ•mol-1①,
H2(g)=H2(l)△H1=-0.92kJ•mol-1②
O2(g)=O2(l)△H2=-6.84kJ•mol-1③
將①-②×2-③×2利用蓋斯定律計算;
D.根據圖象可知,2molH2O(g)生成2molH2O(l)時放出88kJ熱量.
解答 解:A.由圖象分析,2mol H2(g)與1mol O2(g)反應生成2mol H2O(g),放出483.6kJ的熱量,則H2(g)與O2(g)反應生成1molH2O(g)放熱為$\frac{1}{2}$×483.6kJ•mol-1=-241.8 kJ•mol-1,故A錯誤;
B.氫氣的燃燒熱是指1mol氫氣完全燃燒生成液態水放出的熱量,則氫氣的燃燒熱為:$\frac{483.6+88}{2}$=285.8kJ•mol-1,故B錯誤;
C.由圖象分析,2H2(g)+O2(g)═H2O(l)△H1=-483.6kJ•mol-1①,
H2(g)=H2(l)△H1=-0.92kJ•mol-1②
O2(g)=O2(l)△H2=-6.84kJ•mol-1③
將①-②×2-③×2可得2H2(l)+O2(l)═2H2O(g)△H=-474.92kJ•mol-1,故C正確;
D.由圖象可知,2molH2O(g)生成H2O(l)放出88kJ熱量,則2H2O(g)=2H2O(l)△H=-88kJ•mol-1,即H2O(g)=H2O(l)△H=-44kJ•mol-1,故D錯誤;
故選C.
點評 本題綜合考查化學反應與能量變化知識,為高頻考點,題目難度中等,側重于學生的分析能力和計算能力的考查,注意把握燃燒熱的定義以及蓋斯定律的應用,試題培養了學生的分析能力及靈活應用能力.


科目:高中化學 來源: 題型:填空題
 Ⅰ:A、B、W、D、E為短周期元素,且原子序數依次增大,質子數之和為39,B、W同周期,A、D同主族,A、W能形成兩種液態化合物A2W和A2W2,E元素的周期序數與主族序數相等.
Ⅰ:A、B、W、D、E為短周期元素,且原子序數依次增大,質子數之和為39,B、W同周期,A、D同主族,A、W能形成兩種液態化合物A2W和A2W2,E元素的周期序數與主族序數相等.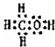 .
.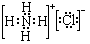 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
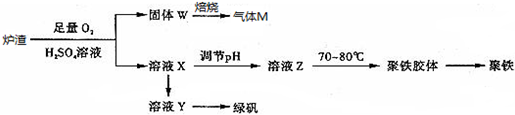
| A. | 爐渣中FeS與硫酸和氧氣的反應的離子方程式為:4FeS+3O2+12H+═4Fe3++4S↓+6H2O | |
| B. | 溶液Z的pH影響聚鐵中鐵的質量分數,若其pH偏小,將導致聚鐵中鐵的質量分數偏大 | |
| C. | 氣體M的成分是SO2,通入雙氧水得到硫酸,可循環使用 | |
| D. | 向溶液X中加入過量鐵粉,充分反應后過濾得到溶液Y,再經蒸發濃縮、冷卻結晶、過濾等步驟得到綠礬 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

| 溫度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| 溶解度/g | 41.6 | 47.5 | 53.8 | 61.3 | 70.5 | 75.4 | 71.1 | 60.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
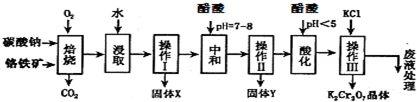
| 物質 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KNO3是鉀鹽、硝酸鹽,也是正鹽 | |
| B. | 漂白粉、明礬、鋁熱劑都是混合物 | |
| C. | 有機玻璃、氮化硅都是有機高分子材料 | |
| D. | CO、CO2、SO2均為酸性氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
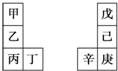 甲~辛等元素在周期表中的相對位置如右表.甲與戊的原子序數相差3,戊的一種單質是自然界硬度最大的物質,丁與辛屬同周期元素,下列判斷正確的是( )
甲~辛等元素在周期表中的相對位置如右表.甲與戊的原子序數相差3,戊的一種單質是自然界硬度最大的物質,丁與辛屬同周期元素,下列判斷正確的是( )| A. | 金屬性:甲>乙>丁 | |
| B. | 最高價氧化物水化物酸性:戊<己 | |
| C. | 丙與庚的原子核外電子數相差13 | |
| D. | 乙的單質在空氣中燃燒生成只含離子鍵的化合物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com