
【題目】關于電解池應用的規律提煉題組某化學興趣小組用下圖所示裝置進行電化學原理的實驗探究,回答下列問題:
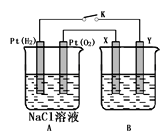
(1)通O2的Pt電極為電池__________極(填電極名稱),其電極反應式為______________。
(2)若B電池為電鍍池,目的是在某鍍件上鍍一層銀,則X電極材料為_________,電解質溶液為__________。
(3)若B電池為精煉銅,且粗銅中含有Zn、Fe、Ag、Au等雜質,在__________電極(填“X”或“Y”)周圍有固體沉積成陽極泥,陽極泥的成分為___________。
(4)若X、Y均為Pt,B電池的電解質溶液為500 mL 1.0mol/L的NaCl溶液,當電池工作一段時間斷開電源K,Y電極有560mL(標準狀況)無色氣體生成(假設電極產生氣體完全逸出,溶液體積不變)。恢復到常溫下,B電池溶液的pH=___________,要使該溶液恢復到原來的狀態,需加入__________(填物質并注明物質的量)。
(5)若X、Y均是銅,電解質溶液為NaOH溶液,電池工作一段時間,X極附近生成磚紅色沉淀,查閱資料得知是Cu2O,試寫出該電極發生的電極反應式為_______________。
(學法題)通過以上題目,請總結書寫電極反應式的關鍵____________ 。
【答案】 正 O2+4e-+2H2O=4OH- Ag AgNO3溶液 X Ag、Au 13 0.05molHCl 2Cu-2e-+2OH-=Cu2O+H2O 電池的判斷、電極是活性電極還是惰性電極及電解質溶液中的離子放電先后順序(其他答案合理也給分)。
【解析】試題分析:(1)裝置A是氫氧燃料電池,氧氣發生還原反應,所以通入氧氣的電極是正極;(2)電鍍時,鍍件作陰極、鍍層金屬作陽極、含有鍍層金屬的鹽作電解質;(3)電解法精煉銅,粗銅作陽極、精銅作陰極,粗銅中銅及活潑性大于銅的金屬失電子,活潑性小于銅的金屬不能失電子;(4)Y極是陰極,發生還原反應生成氫氣,Y電極有560mL(標準狀況)氫氣生成,根據電解方程式計算溶液的pH,根據放出氣體的物質的量分析要使該溶液恢復到原來的狀態需加入的物質。(5)根據題目信息,X極是銅失電子生成Cu2O。
解析:(1)裝置A是氫氧燃料電池,氧氣發生還原反應,所以通入氧氣的電極是正極;在中性溶液中氧氣得電子生成氫氧根離子,電極反應式為O2+4e-+2H2O=4OH-;(2)電鍍時,鍍件作陰極、鍍層金屬作陽極、含有鍍層金屬的鹽作電解質,X與正極相連,X是陽極,所以X電極材料為Ag,電解質溶液為AgNO3溶液。(3)電解法精煉銅,粗銅作陽極、精銅作陰極,粗銅中銅及活潑性大于銅的金屬失電子,活潑性小于銅的金屬不能失電子,X是陽極,所以在X極周圍有固體沉積成陽極泥,Ag、Au的活潑性小于銅,所以陽極泥的成分為Ag、Au;(4)Y極是陰極,發生還原反應生成氫氣,Y電極有560mL(標準狀況)氫氣生成,生成氫氣的物質的量是0.025mol,設生成氫氧化鈉的物質的量是xmol、生成氯氣的物質的量是ymol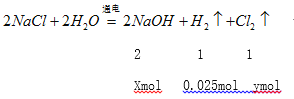
X=0.05mol、y=0.025mol;B池溶液氫氧化鈉的濃度是![]() ,所以pH=13;由于反應放出0.025mol氫氣和0.025mol氯氣,所以要使該溶液恢復到原來的狀態,需加入0.05molHCl;
,所以pH=13;由于反應放出0.025mol氫氣和0.025mol氯氣,所以要使該溶液恢復到原來的狀態,需加入0.05molHCl;
(5)根據題目信息,X極是銅失電子生成Cu2O,電極反應為:2Cu-2e-+2OH-=Cu2O+H2O。
書寫電極反應式的關鍵:電極的判斷、電極是活性電極還是惰性電極及電解質溶液中的離子放電先后順序。


 怎樣學好牛津英語系列答案
怎樣學好牛津英語系列答案科目:高中化學 來源: 題型:
【題目】常溫下,用0.10 mol·L-1鹽酸分別滴定20.00 mL濃度均為0.10 mol·L-1 CH3COONa溶液和NaCN溶液,所得滴定曲線如右圖(忽略體積變化)。下列說法正確的是

A. 溶液中陽離子的物質的量濃度之和:點②等于點③
B. 點①所示溶液中:c(CN—)+ c(HCN)=2c(Cl—)
C. 點②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)> c(CH3COOH)
D. 點④所示溶液中:c(Na+)+ c(CH3COOH)+ c(H+)>0.10 mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關物質的性質或應用正確的是( )
A.鈉與硫酸銅溶液反應會置換出紅色的銅
B.常溫下干燥氯氣與鐵不反應,可以用鋼瓶儲存液氯
C.SO2具有漂白性,通入紫色石蕊溶液中能使溶液先變紅后褪色
D.普通玻璃的組成可用Na2OCaO6SiO2表示,是純凈物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】葡萄糖酸亞鐵[(C6H11O7)2Fe2H2O]是重要的礦物質添加劑,它的吸收效果比無機鐵鹽好。一種工業上制備葡萄糖酸亞鐵的工藝流程如下:
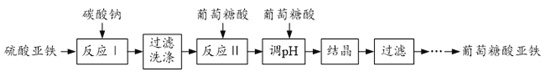
(1)反應Ⅰ的化學方程式為______。
(2)①碳酸亞鐵過濾時需在表面保留水層的原因是______;
②檢驗FeCO3已經洗滌干凈的操作為______。
(3)反應Ⅱ后加入葡萄糖酸調節溶液pH至5.8,其原因是______。
(4)葡萄糖酸亞鐵溶液結晶、洗滌時均需加入乙醇,其目的分別是______,______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海洋植物如海帶和海藻中含有豐富的碘元素,碘元素以碘離子的形式存在。實驗室里從海洋中提取碘的流程如下:
![]()
某化學興趣小組將上述流程②、③設計成如下圖所示操作。
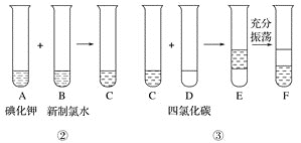
已知過程②發生反應的化學方程式為Cl2+2KI=2KCl+I2
回答下列問題:
(1)寫出提取過程①、③中實驗操作的名稱:①____________,③____________。
(2)在灼燒過程中,使用到的實驗儀器有酒精燈、泥三角、三腳架、玻璃棒、____________、____________。
(3)F中下層液體的顏色為________色,上層液體中溶質的主要成分為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下列實驗裝置和操作,回答有關問題。
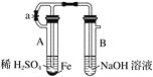
按圖中所示裝置,用兩種不同的操作分別進行實驗,觀察B容器中的現象。
(1)先夾緊止水夾a,再使A容器中開始反應:①實驗中B容器中觀察到的現象是_________________;
②B容器中發生反應的離子方程式是____________________________________。
(2)打開止水夾a,使A容器開始反應一段時間后再夾緊止水夾a,①實驗中觀察到的現象是__________;②B容器中發生反應的離子方程式是________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由單質A與化合物B兩種粉末組成的混合物,在一定條件下可按如圖所示發生轉化:
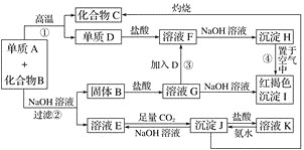
請回答:
(1)A、B的化學式分別為________、________。
(2)反應①的化學方程式:_____________________________________________________。
(3)寫出反應②③的離子方程式:
②________________________________________________________________________;
③________________________________________________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com