
【題目】某溫度下,在容積為1L的密閉容器中充入1molCO2和3.25molH2,發(fā)生CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0,測得CH3OH的物質(zhì)的量隨時間的變化如圖所示,(已知,此溫度下,該反應(yīng)的平衡常數(shù)K=2.25)下列說法正確的是
CH3OH(g)+H2O(g) △H<0,測得CH3OH的物質(zhì)的量隨時間的變化如圖所示,(已知,此溫度下,該反應(yīng)的平衡常數(shù)K=2.25)下列說法正確的是
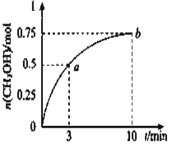
A.0-10min,v(H2)=0.075 mol/(L·min)
B.點(diǎn) b 所對應(yīng)的狀態(tài)沒有達(dá)到化學(xué)平衡狀態(tài)
C.CH3OH 的生成速率,點(diǎn) a 大于點(diǎn) b
D.欲增大平衡狀態(tài)時![]() ,可保持其他條件不變,升高溫度
,可保持其他條件不變,升高溫度
【答案】C
【解析】
A.0~10min,v(CH3OH)=  =0.075 molL-1min-1,v(H2)=3v(CH3OH)=3×0.075 molL-1min-1=0.225molL-1min-1,故A錯誤;
=0.075 molL-1min-1,v(H2)=3v(CH3OH)=3×0.075 molL-1min-1=0.225molL-1min-1,故A錯誤;
B.b點(diǎn)時,n(CH3OH)=0.75mol,c(CH3OH)= ![]() =0.75mol/L,則
=0.75mol/L,則 b點(diǎn)濃度商Qc=
b點(diǎn)濃度商Qc=![]() =
=![]() =2.25,則Qc=K=2.25,b點(diǎn)達(dá)到平衡狀態(tài),故B錯誤;
=2.25,則Qc=K=2.25,b點(diǎn)達(dá)到平衡狀態(tài),故B錯誤;
C.可逆反應(yīng)在沒有達(dá)到平衡狀態(tài)前,隨著反應(yīng)的進(jìn)行,正反應(yīng)速率逐漸減小,所以a點(diǎn)甲醇的生成速率大于b點(diǎn),故C正確;
D.該反應(yīng)的正反應(yīng)是放熱反應(yīng),升高溫度平衡逆向移動,則甲醇濃度減小,二氧化碳濃度增大,所以![]() 減小,故D錯誤;
減小,故D錯誤;
答案為C。


 課程達(dá)標(biāo)測試卷闖關(guān)100分系列答案
課程達(dá)標(biāo)測試卷闖關(guān)100分系列答案 新卷王期末沖刺100分系列答案
新卷王期末沖刺100分系列答案 全能闖關(guān)100分系列答案
全能闖關(guān)100分系列答案
| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:
【題目】(1)寫出下列物質(zhì)在水溶液中的電離方程式。
①CH3COOH _________ ② NaHSO4 __________________
(2)某溫度下,純水中的c(H+)=2×10-7 mol/L,則此時c(OH-)=______。若溫度不變,滴入稀硫酸使c(H+)=5×10-6 mol/L,則由水電離出的c(H+)為_______ 。
(3)常溫下,濃度均為0.01 mol/L 的兩瓶溶液鹽酸和氫氟酸,升高相同的溫度,c(Cl-)/ c(F-)的值__________(填“變大”“變小”“不變”)。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】下列事實(shí)能說明醋酸是弱電解質(zhì)的是 ( )
A. 醋酸能使石蕊溶液變紅
B. ![]() 時.
時.![]() 醋酸的pH約為3
醋酸的pH約為3
C. 向醋酸中加入氫氧化鈉溶液,溶液pH增大
D. 醋酸能與碳酸鈣反應(yīng)產(chǎn)生![]() 氣體
氣體
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】碲(52Te)被譽(yù)為“國防與尖端技術(shù)的維生素”。工業(yè)上常用銅陽極泥(主要成分是Cu2Te、含Ag、Au等雜質(zhì))為原料提取碲并回收金屬,其工藝流程如下:

已知:TeO2微溶于水,易與較濃的強(qiáng)酸、強(qiáng)堿反應(yīng)。回答下列問題:
(1)已知Te為VIA族元素,TeO2被濃NaOH溶液溶解,所生成鹽的化學(xué)式為____________。
(2)“酸浸2”時溫度過高會使Te的浸出率降低,原因是________________________。
(3)“酸浸1”過程中,控制溶液的酸度使Cu2Te轉(zhuǎn)化為TeO2,反應(yīng)的化學(xué)方程式為____________;
“還原”過程中,發(fā)生反應(yīng)的離子方程式為_____________________________。
(4)工業(yè)上也可用電解法從銅陽極泥中提取碲,方法是:將銅陽極泥在空氣中焙燒使碲轉(zhuǎn)化為TeO2,再用NaOH溶液堿浸,以石墨為電極電解所得溶液獲得Te。電解過程中陰極上發(fā)生反應(yīng)的電極方程式為____________________。在陽極區(qū)溶液中檢驗(yàn)出有TeO42-存在,生成TeO42-的原因是_____________________。
(5)常溫下,向l mol·L-1 Na2TeO3溶液中滴加鹽酸,當(dāng)溶液pH=5時,c(TeO32-):c(H2TeO3)=__________。(已知:H2TeO3的Ka1=1.0×10-3 Ka2=2.0×10-8)
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】一種熔融碳酸鹽燃料電池原理示意圖如下。下列有關(guān)該電池的說法正確的是( )
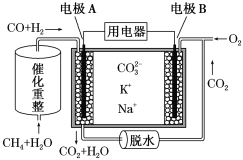
A.電池工作時,CO32-向電極B移動
B.電極B上發(fā)生的電極反應(yīng)為O2+2CO2+4e-=2 CO32-
C.電極A上H2參與的電極反應(yīng)為H2+2OH--2e-=2H2O
D.反應(yīng)CH4+H2O 3H2+CO,每消耗1 mol CH4轉(zhuǎn)移12 mol電子
3H2+CO,每消耗1 mol CH4轉(zhuǎn)移12 mol電子
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】工業(yè)上利用鋅焙砂(主要含ZnO、ZnFe2O4,還含有少量FeO、CuO等雜質(zhì))制取金屬鋅的工藝流程如下:

(1)酸浸時要將鋅焙砂粉碎,其目的是提高酸浸效率,為達(dá)到這一目的,還可采用的措施是_____(任答一條)。寫出ZnFe2O4溶于酸的離子方程式____________________________
(2)凈化Ⅰ中H2O2 參與反應(yīng)的離子方程式為_________________________
(3)凈化Ⅱ中Y 的主要成分是________(填化學(xué)式)。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】分離提純、溶液的配制和分析是化學(xué)家常用的研究物質(zhì)的實(shí)驗(yàn)方法,根據(jù)所學(xué)知識,回答下列問題:
Ⅰ.實(shí)驗(yàn)室從海藻中提取碘的流程如圖:

(1)提取碘的過程中,操作③的名稱為___。
(2)“后期處理”中涉及的操作為___。
(3)在灼燒過程中,使用到的實(shí)驗(yàn)儀器有___(除三腳架和酒精燈外)。
A.燒杯 B.蒸發(fā)皿 C.坩堝鉗 D.瓷坩堝 E.泥三角
Ⅱ.依據(jù)粗鹽提純的原理,除去硝酸鉀固體中少量的硝酸鎂、硫酸鎂雜質(zhì),按如圖步驟操作,回答下列問題:

(1)試劑A和B的化學(xué)式分別是___,___。
(2)操作Ⅱ?yàn)?/span>___,___,___。
Ⅲ.實(shí)驗(yàn)室現(xiàn)需配制物質(zhì)的量濃度為1mol/L的NaOH溶液480mL。
(1)實(shí)驗(yàn)過程中用到的玻璃儀器有:燒杯、玻璃棒、___、___。
(2)要配制此溶液,需要稱量NaOH固體的質(zhì)量為___。
(3)下列操作會使所配溶液濃度偏大的有___。
A.溶解固體溶質(zhì)時,未冷卻到室溫即轉(zhuǎn)入容量瓶定容
B.容量瓶中原有少量蒸餾水
C.定容時仰視讀數(shù)
D.砝碼生銹但未脫落
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】隨著氮氧化物對環(huán)境及人類活動影響的日趨嚴(yán)重,如何消除大氣污染物中的氮氧化物成為人們關(guān)注的主要問題之一。
Ⅰ.利用NH3的還原性可以消除氮氧化物的污染,其中除去NO的主要反應(yīng)如下:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) △H<0
5N2(g)+6H2O(l) △H<0
(1)寫出一種可以提高NO的轉(zhuǎn)化率的方法:__________
(2)一定溫度下,在恒容密閉容器中按照n(NH3)︰n(NO) =2︰3充入反應(yīng)物,發(fā)生上述反應(yīng)。下列不能判斷該反應(yīng)達(dá)到平衡狀態(tài)的是___________
A.c(NH3)︰c(NO) =2︰3 B.n(NH3)︰n(N2) 不變 C.容器內(nèi)壓強(qiáng)不變 D.容器內(nèi)混合氣體的密度不變 E.1molN—H鍵斷裂的同時,生成1molO—H鍵
(3)已知該反應(yīng)速率v正=k正·c4(NH3)·c6 (NO),v逆=k逆·cx(N2)·cy(H2O) (k正、k逆分別是正、逆反應(yīng)速率常數(shù)),該反應(yīng)的平衡常數(shù)K=k正/k逆,則x=_____,y=_______。
(4)某研究小組將2molNH3、3molNO和一定量的O2充入2L密閉容器中,在Ag2O催化劑表面發(fā)生上述反應(yīng),NO的轉(zhuǎn)化率隨溫度變化的情況如圖所示:

①在5min內(nèi),溫度從420K升高到580K,此時段內(nèi)NO的平均反應(yīng)速率v(NO)=_______;
②在有氧條件下,溫度580K之后NO生成N2的轉(zhuǎn)化率降低的原因可能是___________。
Ⅱ.用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一種可行的方法。NO和NO2不同配比混合氣通入尿素溶液中,總氮還原率與配比關(guān)系如圖。

(5)用尿素[(NH2)2CO]水溶液吸收體積比為1∶1的NO和NO2混合氣,可將N元素轉(zhuǎn)變?yōu)閷Νh(huán)境無害的氣體。寫出該反應(yīng)的化學(xué)方程式____。
(6)隨著NO和NO2配比的提高,總氮還原率降低的主要原因是________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】25℃時,改變醋酸溶液的pH[溶液中c(CH3COOˉ)與c(CH3COOH)之和始終為0.1mol·Lˉ1],溶液中H+、OHˉ、CH3COOˉ及CH3COOH濃度的對數(shù)值(lgc)與pH關(guān)系如圖所示。

下列說法錯誤的是
A. lgK(CH3COOH)=-9.26
B. 圖中①表示 CH3COOH濃度的對數(shù)值與pH的關(guān)系曲線
C. 0.1mol·Lˉ1CH3COOH溶液的pH約為2.88
D. 0.1mol·Lˉ1CH3 COONa溶液的pH約為8.87
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com