
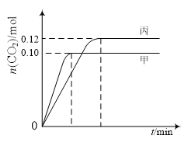
【題目】一定溫度下,在三個容積均為2.0 L的恒容密閉容器中發生反應:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物質的量與反應溫度如下表所示,反應過程中甲、丙容器中CO2的物質的量隨時間變化關系如圖所示:
N2(g)+2CO2(g)。各容器中起始物質的量與反應溫度如下表所示,反應過程中甲、丙容器中CO2的物質的量隨時間變化關系如圖所示:
容器 | 溫度/℃ | 起始物質的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
下列說法正確的是
A. 該反應的正反應為吸熱反應
B. 達到平衡時,乙中CO2的體積分數比甲中的小
C. T1℃時,若起始時向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,則反應達到新平衡前v(正)<v(逆)
D. T2℃時,若起始時向丙中充入0.06molN2和0.12 molCO2,則達平衡時N2的轉化率大于40%
【答案】D
【解析】
A.先拐先平溫度高,甲平衡狀態時二氧化碳物質的量小,說明溫度越高平衡逆向進行;
B.乙中可以看做是甲起始量達到平衡狀態,再加入0.1molNO和0.1molCO,相當于增大平衡壓強,平衡正向進行;
C.甲狀態下平衡時CO物質的量為0.10mol,結合三段式計算平衡常數,依據起始量計算濃度商和平衡常數比較判斷反應進行方向;
D.T2℃時,依據圖象可知平衡狀態下CO物質的量為0.12mol,若起始時向丙中充入0.06mol N2和0.12 mol CO2,反應逆向進行得到平衡狀態,和起始量為0.12molNO和0.12molCO達到的平衡相比較,和起始量0.2molCO、NO相比,相當于減少了NO、CO0.08mol的CO、NO,壓強減小平衡逆向進行.
A.2NO(g)+2CO(g)![]() N2(g)+2CO2(g),先拐先平溫度高,甲狀態溫度高于丙,T1>T2,此時甲平衡狀態二氧化碳物質的量小,說明溫度越高平衡逆向進行,逆反應為吸熱反應,正反應為放熱反應,故A錯誤;
N2(g)+2CO2(g),先拐先平溫度高,甲狀態溫度高于丙,T1>T2,此時甲平衡狀態二氧化碳物質的量小,說明溫度越高平衡逆向進行,逆反應為吸熱反應,正反應為放熱反應,故A錯誤;
B.乙中可以看做是甲起始量達到平衡狀態,再加入0.1molNO和0.1molCO,相當于增大平衡壓強,平衡正向進行,達到平衡時,乙中CO2的體積分數比甲中的大,故B錯誤;
C.甲狀態下平衡時CO物質的量為0.10mol,結合三段式計算平衡常數,
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol·L-1) 0.1 0.1 0 0
變化量(mol·L-1) 0.05 0.05 0.025 0.05
平衡量(mol·L-1) 0.05 0.05 0.025 0.05
K=![]() =10,T1℃時,若起始時向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,Qc=
=10,T1℃時,若起始時向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,Qc=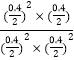 =5<K=10.則反應達到新平衡前v(正)>v(逆),故C錯誤;
=5<K=10.則反應達到新平衡前v(正)>v(逆),故C錯誤;
D.T2℃時,平衡狀態CO物質的量為0.12mol,
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol) 0.2 0.2 0 0
轉化量(mol) 0 0 0.1 0.2
變化量(mol) 0.08 0.08 0.04 0.08
平衡量(mol) 0.12 0.12 0.04 0.08
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
起始量(mol) 0 0 0.06 0.12
轉化量(mol) 0.12 0.12 0 0
若起始時向丙中充入0.06mol N2和0.12 mol CO2,反應逆向進行得到平衡狀態,和起始量為0.12molNO和0.12molCO達到的平衡相同,和起始量0.2molCO、NO相比,相當于減少了NO、CO 0.08mol的CO、NO,壓強減小平衡逆向進行,所以氮氣轉化率大于40%,故D正確;
故選:D。


科目:高中化學 來源: 題型:
【題目】碳、氮、銅形成的單質及它們形成的化合物有重要研究和應用價值,回答下列問題:
(1)鄰氨基吡啶的銅配合物在有機不對稱合成中起催化誘導效應,其結簡式如圖所示。

①基態Cu原子的價電子排布式為_________,在元素周期表中銅位于_________區(填“s”“p”“d”或“ds”)。
②C、N、O三種元素的第一電離能由大到小的順序為_________。
③鄰氨基吡啶的銅配合物中,Cu2+的配位數是_________,N原子的雜化類型為_________。
(2)C60是富勒烯族分子中穩定性最高的一種,N60是未來的火箭燃料,二者結構相似。
①有關C60和N60的說法中正確的是_________。
A.C60和N60均屬于分子晶體 B.N60的穩定性強于N2
C.C60中碳原子是sp3雜化 D.C60易溶于CS2、苯
②近年來,科學家合成了一種具有“二重結構”的球形分子,它是把足球形分子C60容納在足球形分子Si60中,則該分子中含有的化學鍵類型為___________ (填“極性鍵”“非極性鍵”)。
(3)原子坐標參數和晶胞參數是晶胞的兩個基本參數。
①圖中原子坐標參數分別為:A(0,0,0),B(1/2,1/2,0),C(1/2,0,1/2),則D的原子坐標參數為_________。

②圖為銅的晶胞,銅原子半徑為Rnm,NA是阿伏加德羅常數的值,則銅晶體的密度為_________g·cm-3(用含R、NA的式子表示)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如下實驗方案,以分離KCl和BaCl2兩種固體混合物,試回答下列問題:

(1)操作①的名稱是_____,操作②的名稱是____。
(2)試劑a是_____(填化學式,下同),試劑b是____,固體B是_____。
(3)加入試劑a所發生反應的化學方程式為_______________________。加入試劑b所發生反應的化學方程式為_______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是

A. 圖1表示1 L pH=2的CH3COOH溶液加水稀釋至V L,pH隨lg V的變化
B. 圖2表示不同溫度下水溶液中H+和OH-濃度的變化的曲線,圖中溫度T2<T1
C. 圖3表示一定條件下的合成氨反應中,NH3的平衡體積分數隨H2起始體積分數(N2的起始量恒定)的變化,圖中a點N2的轉化率等于b點
D. 圖4表示同一溫度下,相同物質的量BaO2在不同容積的容器中進行反應:2BaO2(s)![]() 2BaO(s)+O2(g),O2的平衡濃度與容器容積的關系
2BaO(s)+O2(g),O2的平衡濃度與容器容積的關系
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高溫下,某反應達平衡,平衡常數K=![]() 。恒容時,溫度升高,H2濃度減小。下列說法正確的是
。恒容時,溫度升高,H2濃度減小。下列說法正確的是
A. 該反應的焓變為正值
B. 恒溫恒容下,通入N2,壓強增大,反應速率加快
C. 升高溫度,正反應速率加快,逆反應速率減慢,平衡正向移動
D. 該反應化學方程式為CO+H2O![]() CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室需要80 mL 1 mol·L1的稀硫酸,要用98%的濃硫酸(密度為1.84 g·cm3)來配制。現給出下列儀器(配制過程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL燒杯 ④托盤天平 ⑤100 mL容量瓶 ⑥膠頭滴管 ⑦玻璃棒 ⑧80 mL容量瓶。按使用儀器的先后順序排列正確的是
A. ④③⑦⑧⑥ B. ②⑤⑦⑥ C. ①③⑧⑥⑦ D. ②⑥③⑦⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學用如圖所示的實驗裝置研究氣體X的性質。氣體X的主要成分是氯氣,其中還含有水蒸氣。請回答下列問題:
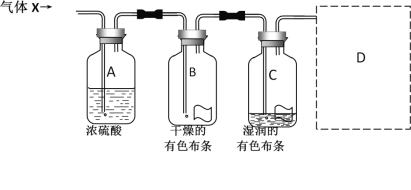
(1)該實驗的主要目的是__________________________。
(2)與實驗目的直接相關的實驗現象是_________________________。
(3)圖中所示的實驗設計還存在不足。請根據相關物質的性質,在圖中的D處畫圖補充有關實驗裝置和所用試劑。_______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應C(s)+H2O(g)![]() CO(g)+H2(g)在一體積可變的容器中進行。下列條件的改變對其化學反應速率幾乎沒有影響的是:①增加C的用量;②將容器體積縮小一半;③保持容器體積不變,充入氮氣使容器內壓強增大;④保持壓強不變,充入氮氣使容器的體積變大
CO(g)+H2(g)在一體積可變的容器中進行。下列條件的改變對其化學反應速率幾乎沒有影響的是:①增加C的用量;②將容器體積縮小一半;③保持容器體積不變,充入氮氣使容器內壓強增大;④保持壓強不變,充入氮氣使容器的體積變大
A. ②④ B. ①③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】羰基硫(COS)與氫氣或與水在催化劑作用下的反應如下:
Ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g) △H1=-17kJ/mol;
H2S(g)+CO(g) △H1=-17kJ/mol;
Ⅱ.COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H2=-35kJ/mol。
H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列問題:
(1)兩個反應在熱力學上趨勢均不大,其原因是:________________。
(2)反應CO(g)+H2O(g)![]() H2(g)+CO2(g)的△H=_______。
H2(g)+CO2(g)的△H=_______。
(3)羰基硫、氫氣、水蒸氣共混體系初始投料比不變,提高羰基硫與水蒸氣反應的選擇性的關鍵因素是______。
(4)在充有催化劑的恒壓密閉容器中只進行反應Ⅰ![]() 設起始充入的n(H2):n(COS)=m,相同時間內測得COS轉化率與m和溫度(T)的關系如圖所示:
設起始充入的n(H2):n(COS)=m,相同時間內測得COS轉化率與m和溫度(T)的關系如圖所示:

①m1______m2(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 。
。
②溫度高于T0,COS轉化率減小的可能原因為:i有副應發生;ii______;iii______。
(5)在充有催化劑的恒壓密閉容器中進行反應Ⅱ.COS(g)與H2O(g)投料比分別為1:3和1:1,反應物的總物質的量相同時,COS(g)的平衡轉化率與溫度的關系曲線如圖所示:
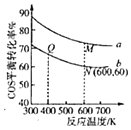
①M點對應的平衡常數______Q點![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ;
;
②N點對應的平衡混合氣中COS(g)物質的量分數為______;
③M點和Q點對應的平衡混合氣體的總物質的量之比為______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com