
【題目】下列熱化學方程式及有關應用的敘述中,正確的是( )
A.甲烷的燃燒熱為 890.3kJmol-1,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJmol-1
B.已知強酸與強堿在稀溶液里反應的中和熱為 57.3kJmol-1,則![]() H2SO4(aq)+
H2SO4(aq)+ ![]() Ba(OH)2(aq)═
Ba(OH)2(aq)═![]() BaSO4(s)+H2O(l) △H = -57.3kJmol-1
BaSO4(s)+H2O(l) △H = -57.3kJmol-1
C.500℃、30MPa 下,將 0.5mol N2 和 1.5molH2 置于密閉的容器中充分反應生成 NH3(g),放熱19.3kJ,其熱化學方程式為:N2(g) + 3H2(g) ![]() 2NH3(g) △H= -38.6kJmol-1
2NH3(g) △H= -38.6kJmol-1
D.已知 25℃、101KPa 條件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H= -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,則 O2比 O3 穩定
【答案】D
【解析】
A、燃燒熱是指1mol可燃物完全燃燒生成穩定的氧化物時所放出的熱量,氫元素應該轉化成液態水,選項A錯誤;
B、硫酸和氫氧化鋇溶液的反應中,硫酸根和鋇離子反應生成硫酸鋇沉淀也伴隨著能量變化,選項B錯誤;
C、合成氨的反應為可逆反應,不能進行到底,題給信息無法確定該反應的焓變,選項C錯誤;
D、已知25℃、101KPa條件下:①4Al(s)+3O2(g)=2A12O3(s) △H=-2834.9 kJ·mol-1,②4Al(s)+2O3(g)=2A12O3(s) △H=-3119.1 kJ·mol-1,根據蓋斯定律:①-②得3O2(g)=2O3(g),△H=+288.2 kJ·mol-1,則O2比O3穩定,選項D正確。
答案選D。


 孟建平小學滾動測試系列答案
孟建平小學滾動測試系列答案 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:高中化學 來源: 題型:
【題目】觀察![]() Cl-粒子,完成下列問題:
Cl-粒子,完成下列問題:
(1)所含質子數________,中子數________,電子數________,質量數________。
(2)該元素的最高正化合價是________。
(3)該粒子的結構示意圖________________,電子式________________。
(4)該粒子與![]() Cl的半徑大小的關系是________________。
Cl的半徑大小的關系是________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮、磷、鉀是農作物生長的必須營養元素,磷和鈣都是促成骨骼和牙齒的鈣化不可缺少的營養元素。回答下列問題:
(1)基態K的核外電子排布式為____________,基態N的價電子排布圖為____________。
(2)元素的第一電離能:Ca________(填“>”或“<”)P。
(3)白磷P4在CS2中的溶解度________(填“大于”或“小于”)在水中的溶解度,N4是氮的一種新型單質,若N4分子結構類似于白磷P4,則N的雜化方式為________。
(4)下表是幾種碳酸鹽的熱分解溫度和陽離子半徑:
碳酸鹽 | CaCO3 | SrCO3 | BaCO3 |
熱分解溫度/℃ | 900 | 1172 | 1360 |
陽離子半徑/pm | 99 | 112 | 135 |
根據上表數據分析碳酸鋇分解溫度最高的原因是_______________________
(5)常溫下PCl5是一種白色晶體,晶體結構為氯化銫型,由A、B兩種離子構成。已知A、B兩種離子分別與CCl4、SF6互為等電子體,則A、B兩種離子的符號分別為________、________。
(6)用晶體的X射線衍射法可以測得阿伏加德羅常數的值。已知金屬鈣的晶胞為面心立方(如圖)晶胞,晶胞邊長為d pm;又知鈣的密度為ρ g/cm3,則一個鈣晶胞的質量為________(用d、ρ表示,下同)g,阿伏加德羅常數的值為______________(化成最簡式)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】物質的結構決定其性質,元素周期表和元素周期律揭示了化學元素間的內在聯系,使其構成了一個完整的體系。回答下列問題:
(1)在硼、氮、氧、氟中,第一電離能由大到小排序為___________(用元素符號表示,下同)。四種元素中的基態原子中,未成對電子數最多的是___________。
(2)已知硼酸的電離方程式為H3BO3+H2O![]() [B(OH)4]+H+。
[B(OH)4]+H+。
①硼酸是___________元酸。
②[B(OH)4]-中含有的化學鍵類型有___________(填標號)。
a.σ鍵 b.π鍵 c.配位鍵 d.非極性鍵
③由[B(OH)4]-推出[Al(OH)4]-的結構式為______________________。
(3)氟化硝酰(NO2F)與NO3-的結構相似,則其分子的立體構型是___________,N原子的雜化軌道類型為___________。
(4)已知單質硼晶體的熔點為1873℃,單質硼晶體是___________晶體。
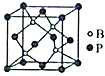
(5)磷化硼(BP)是一種超硬耐磨涂層材料,其立方晶胞如圖所示。已知晶胞中B-P鍵鍵長均為anm,阿伏加德羅常數的值為NA,則磷化硼晶體的密度為___________g·cm-3(列出計算式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】美、德兩國成功合成具有化學特性的氫鋁化合物![]() ,關于氫鋁化合物的推測不正確的是( )
,關于氫鋁化合物的推測不正確的是( )
A.氫鋁化合物中鋁顯![]() 價,氫顯
價,氫顯![]() 價
價
B.氫鋁化合物與水反應生成氫氧化鋁和氫氣
C.鋁與水蒸氣高溫下反應生成氫鋁化合物
D.氫鋁化合物具有強還原性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】試管實驗操作簡單,現象明顯。以下試管實驗操作及現象均正確的是( )
![]()
A. 直接向淀粉水解液中滴加新制氫氧化銅懸濁液,加熱,產生磚紅色沉淀
B. 向苯中滴加少量溴的四氯化碳溶液,充分振蕩后靜置,分層,上層無色,下層橙紅色
C. 向FeSO4 溶液中滴加 K3[Fe(CN)6]溶液,振蕩,溶液變血紅色
D. 用一束強光照射雞蛋白溶液,產生一條光亮的通路
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】酮洛芬是優質抗炎鎮痛藥,合成原理如下:
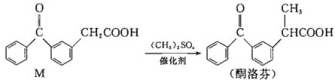
下列說法正確的是( )
A.M和酮洛芬都能發生酯化、鹵代和加成反應
B.M和酮洛芬分子中所有碳原子都可能共平面
C.M和酮洛芬在一定條件下最多消耗![]() 的物質的量相等
的物質的量相等
D.M分子中苯環上一氯代物有9種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機物的說法正確的是
A. 苯佐卡因(![]() )是局部麻醉藥,分子中含有2種官能團,分子式為C9H10NO2
)是局部麻醉藥,分子中含有2種官能團,分子式為C9H10NO2
B. 香葉醇( )能發生加成反應不能發生取代反應
)能發生加成反應不能發生取代反應
C. 青蒿素(![]() ) 的一氯代物有5種(不含立體異構)
) 的一氯代物有5種(不含立體異構)
D. 某有機物的分子式為C4H8,能使溴的CCl4溶液褪色,則它在一定條件下與水反應時最多可生成的有機物(不考慮立體異構)有4種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2SO2(g)+O2(g) ![]() 2SO3(g)反應過程的能量變化如圖所示。已知 1 molSO2(g)氧化為1 mol SO3(g)的ΔH=-99 kJ·mol-1 。
2SO3(g)反應過程的能量變化如圖所示。已知 1 molSO2(g)氧化為1 mol SO3(g)的ΔH=-99 kJ·mol-1 。

請回答下列問題:
(1)圖中A、C分別表示____________________、___________________,E的大小對該反應的反應熱有無影響?________________。該反應通常用 V2O5 作催化劑,加V2O5會使圖中B點升高還是降低?__________, 理由是______________________;
(2)圖中ΔH=_____kJ·mol-1;
(3) V2O5的催化循環機理可能為:V2O5氧化SO2時,自身被還原為四價釩化合物;四價釩化合物再被氧氣氧化。寫出該催化循環機理的化學方程式_____;
(4)已知單質硫的標準燃燒熱 ΔH=﹣296 kJ·mol-1,計算由S(s)生成3 mol SO3(g)放出的熱量 為_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com