
【題目】設計如下實驗探究橄欖石(僅含三種短周期元素)的組成和性質。
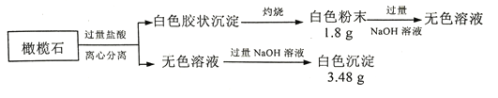
(1)橄欖石的組成元素是O和____、____(填元素符號),化學式為__________。
(2)寫出白色粉末A的一種用途:__________________________。
(3)白色粉末A溶于NaOH溶液的離子方程式是 _________________________________。
【答案】Mg Si 2MgO·SiO2 光導纖維等合理即可 SiO2+2OH-=SiO32-+H2O
【解析】
橄欖石與鹽酸反應后生成了白色膠狀沉淀,推知該膠狀沉淀為硅酸,灼燒后生成二氧化硅,質量為1.8g,則物質的量為![]() ,二氧化硅能溶于NaOH溶液生成Na2SiO3,橄欖石與過量鹽酸反應后的無色溶液,與過量的NaOH溶液反應后,生成白色沉淀,該沉淀應是Mg(OH)2,質量為3.48g,則物質的量為
,二氧化硅能溶于NaOH溶液生成Na2SiO3,橄欖石與過量鹽酸反應后的無色溶液,與過量的NaOH溶液反應后,生成白色沉淀,該沉淀應是Mg(OH)2,質量為3.48g,則物質的量為![]() ,因此該化合物中,硅元素與鎂元素的物質的量之比為1:2,因此橄欖石的化學式為:2MgO·SiO2;
,因此該化合物中,硅元素與鎂元素的物質的量之比為1:2,因此橄欖石的化學式為:2MgO·SiO2;
(1)根據以上分析可知,橄欖石的組成元素是O和Mg、Si,化學式為2MgO·SiO2,本題答案為:Mg;Si;2MgO·SiO2;
(2)白色粉末為二氧化硅,用途有:制造玻璃、石英玻璃、水玻璃、光導纖維、電子工業的重要部件、光學儀器、工藝品和耐火材料的原料,本題答案為:光導纖維等;
(3)白色粉未為二氧化硅,與NaOH溶液反應的離子方程式為:SiO2+2OH-=SiO32-+H2O,
本題答案為:SiO2+2OH-=SiO32-+H2O。


科目:高中化學 來源: 題型:
【題目】[Fe(CN)6]3可將氣態廢棄物中的硫化氫轉化為可利用的硫,自身還原為[Fe(CN)6]4。工業上常采用如圖所示的電解裝置,通電電解,然后通入H2S加以處理。下列說法不正確的是

A. 電解時陽極反應式為[Fe(CN)6]4e![]() [Fe(CN)6]3
[Fe(CN)6]3
B. 電解時陰極反應式為2HCO3-+2e![]() H2↑+2CO32-
H2↑+2CO32-
C. 當電解過程中有22.4 L標準狀況下的H2生成時,溶液中有32 g S析出(溶解忽略不計)
D. 整個過程中需要不斷補充K4[Fe(CN)6]與KHCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述與圖象對應符合的是

A. 對于達到平衡狀態的N2(g)+3H2(g) ![]() 2NH3(g) 在t0時刻充入了一定量的NH3,平衡逆向移動
2NH3(g) 在t0時刻充入了一定量的NH3,平衡逆向移動
B. 對于反應2A(g)+B(g)![]() C(g)+D(g) ΔH < 0,p2 > p1,T1 > T2
C(g)+D(g) ΔH < 0,p2 > p1,T1 > T2
C. 該圖象表示的化學方程式為:2A===B+3C
D. 對于反應2X(g)+3Y(g) ![]() 2Z(g) ΔH < 0,y可以表示Y的百分含量
2Z(g) ΔH < 0,y可以表示Y的百分含量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,用濃度均為0.1 mol·L-1的NaOH溶液和鹽酸分別滴定體積均為20mL、濃度均為0.1 mol·L-1的HA溶液與BOH溶液。滴定過程中溶液的pH隨滴加溶液的體積變化關系如圖所示。下列說法中正確的是
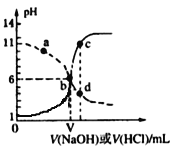
A. HA為弱酸,BOH為強堿
B. a點時,溶液中粒子濃度存在關系:c(B+) > c(Cl-) > c(OH-) > c(BOH)
C. c、d兩點溶液混合后微粒之間存在關系:c(H+) = c(OH-) + c(BOH)
D. b點時兩種溶液中水的電離程度相同,且V=20
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某回學用下列裝置完成了濃硫酸和SO2性質實驗(夾持裝置已省略)
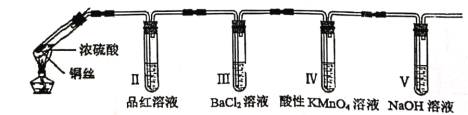
下列說法錯誤的是
A. 反應后,試管Ⅰ中出現白色固體,將其放入水中,溶液顯藍色
B. 試管Ⅱ中品紅溶液逐漸褪色,對其加熱溶液又恢復紅色
C. 試管Ⅳ中高錳酸鉀褪色,體現了SO2的漂白性
D. 試管Ⅴ可以改為裝有堿石灰的干燥管
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是中學化學中常用于混合物的分離和提純裝置,請根據裝置回答問題:
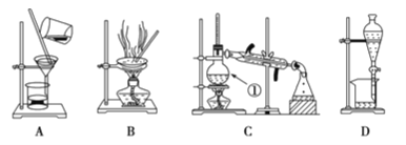
(1)在裝置A和裝置B中都用到玻璃棒,裝置A中玻璃棒的作用是_______,裝置C中冷凝水從____通入。
(2)裝量C中①的名稱是________,裝置D中的分液漏斗在使用之前應該進行的操作為__________,在分液時為使液體順利滴下,應進行的操作為________________________。
(3)青蒿素是從復合花序植物黃花蒿莖葉中提取的有過氧基團的倍半萜內酯的一種無色針狀晶體,是一種高效的抗瘧疾藥,為無色針狀晶體,易溶于丙酮、氯仿和苯中,在乙醇、乙醚中可溶解,在水中幾乎不溶,熔點為156-157℃,熱穩定性差。
已知:乙醚沸點為35℃。提取青蒿素的主要工藝為:
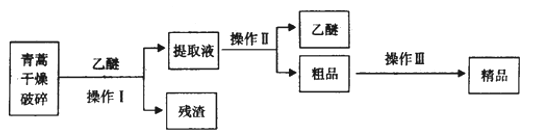
若要在實驗室模擬上述工藝,操作Ⅰ選擇的裝置是_______,操作Ⅱ的名稱是________,操作Ⅲ的主要過程可能是_______(填字母)
A. 加95%的乙醇,濃縮、結晶、過濾
B. 加水溶解,蒸發濃縮、冷卻結晶、過濾
C. 加入乙醚進行萃取分液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列熱化學方程式:
①H2(g)+![]() O2(g)===H2O(l) ΔH=-285.8 kJ/mol
O2(g)===H2O(l) ΔH=-285.8 kJ/mol
②H2(g)+![]() O2(g)===H2O(g) ΔH=-241.8 kJ/mol
O2(g)===H2O(g) ΔH=-241.8 kJ/mol
③C(s)+![]() O2(g)===CO(g) ΔH=-110.5 kJ/mol
O2(g)===CO(g) ΔH=-110.5 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
回答下列問題:
(1)上述反應中屬于放熱反應的是_____________(填序號)。
(2)H2的燃燒熱為_____________,C的燃燒熱為_____________。
(3)燃燒10 g H2生成液態水,放出的熱量為________。
(4)CO的燃燒熱為______________,其熱化學方程式為_______________________。
(5)在某溫度時,測得0.01 molL-1的NaOH溶液的pH為11。該溫度下,水的離子積常數Kw =________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】pH=2的A、B兩種酸溶液各1mL,分別加水稀釋到1000mL,其溶液的pH與溶液體積(V)的關系如圖所示,則下列說法不正確的是

A. 稀釋后A酸溶液的酸性比B酸溶液弱
B. a=5時,A是強酸,B是弱酸
C. 若A、B都是弱酸,則5>a>2
D. A、B兩種酸濟液物質的量濃度一定相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分析如圖所示的四個原電池裝置,其中結論正確的是( )

A. ①②中Mg作為負極,③④中Fe作為負極
B. ②中Mg作為正極,電極反應式為6H2O+6e-===6OH-+3H2↑
C. ③中Fe作為負極,電極反應式為Fe-2e-===Fe2+
D. ④中Cu作為正極,電極反應式為2H++2e-===H2↑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com