
| A. | CH3Cl | B. | CH2Cl2 | C. | CHCl3 | D. | HCl |
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
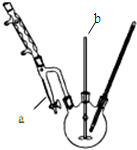 塑化劑DBP(鄰苯二甲酸二丁酯)主要應用于PVC等合成材料中作軟化劑.反應原理為:
塑化劑DBP(鄰苯二甲酸二丁酯)主要應用于PVC等合成材料中作軟化劑.反應原理為: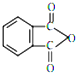 +2CH3CH2CH2CH2OH→
+2CH3CH2CH2CH2OH→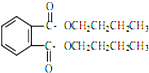 +H2O
+H2O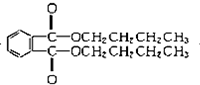 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$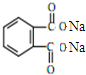 +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 質量:④<①<③<② | B. | 密度:①<④<③<② | ||
| C. | 體積:④<①<②<③ | D. | 氫原子數:②<④<③<① |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:2:3 | B. | 2:1:1 | C. | 4:2:1 | D. | 1:2:4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol H2O中含有的原子數為NA | |
| B. | 2g H2中含有的氫原子數為2NA | |
| C. | 常溫常壓下,11.2L N2中含有的分子數為0.5N A | |
| D. | 1L 0.1 mol/L NaNO3溶液中含有的鈉離子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+Mg2+ Cl- OH- | B. | H+Ca2+ CO32-NO3- | ||
| C. | Cu2+K+SO42-NO3- | D. | Na+ HCO3-OH- Ca2+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com