
對于在恒溫恒容容器中進行的反應A(g)+2B(g)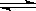 3C(g)+D(g),以下不能說明已達平衡狀態的是
3C(g)+D(g),以下不能說明已達平衡狀態的是
| A.反應容器中,壓強不隨時間改變而改變 |
| B.單位時間內生成3nmolC的同時生成nmolA |
| C.反應容器中,混合氣體的平均相對分子質量不再改變 |
| D.反應容器中的氣體密度不隨時間變化 |
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:單選題
下列事實不能用平衡移動原理解釋的是
| A.鋼鐵在潮濕的空氣中比在干燥空氣中更容易生銹 |
| B.用加熱蒸干AlCl3溶液的方法不能制得無水AlCl3 |
| C.蒸餾水和0.1 mol?L-1 NaOH溶液中的c(H+),前者大于后者 |
| D.向含有少量Fe3+的MgCl2酸性溶液中加入MgCO3,可將Fe3+轉化成Fe(OH)3除去 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定條件下,可逆反應N2 + 3H2 2NH3達到化學平衡狀態,下列說法一定正確的是
2NH3達到化學平衡狀態,下列說法一定正確的是
| A.每1 mol N≡N斷裂的同時有2 mol N—H生成 |
| B.N2、H2、NH3的濃度之比為1:3:2 |
| C.N2減少的速率和NH3減少的速率之比為1:2 |
D.氣體體積為初始體積的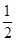 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
T℃時,某一氣態平衡體系中含有X(g)、Y(g)、Z(g)、W(g)四種物質,此溫度下發生反應的平衡常數表達式為: ,有關該平衡體系的說法正確的是
,有關該平衡體系的說法正確的是
A.該反應可表示為X(g) + 2Y(g) 2Z(g) + 2W(g) 2Z(g) + 2W(g) |
| B.減小X濃度,平衡向逆反應方向移動,平衡常數K減小 |
| C.增大反應容器的壓強,該反應速率一定增大 |
| D.升高溫度,W(g)體積分數增加,則正反應是放熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在容積相同的A、B兩個密閉容器中,分別充入2molSO2和1molO2,使它們在相同溫度下發生反應:2SO2+O2 2SO3并達到平衡.在反應過程中,若A容器保持體積不變,B容器保持壓強不變,當 A 中的 SO2 的轉化率為 25% 時,則 B 容器中 SO2 的轉化率應是
2SO3并達到平衡.在反應過程中,若A容器保持體積不變,B容器保持壓強不變,當 A 中的 SO2 的轉化率為 25% 時,則 B 容器中 SO2 的轉化率應是
A.25% B.>25% C.<25% D.12.5%
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
100 mL濃度為2 mol·L-1的鹽酸跟過量的鋅片反應,為加快反應速率,又不影響生成氫氣的總量,可采用的方法是
| A.加入適量的6 mol·L-1的鹽酸 | B.加入數滴氯化銅溶液 |
| C.加入適量蒸餾水 | D.加入適量的氯化鈉溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
加熱N2O5時,發生以下兩個反應:N2O5 N2O3 + O2,N2O3
N2O3 + O2,N2O3 N2O + O2。在1L密閉容器中加熱4molN2O5,達到平衡時,c(O2)為4.5mol?L-1,c(N2O3) 為1.62mol?L-1,則c(N2O5) 為( )
N2O + O2。在1L密閉容器中加熱4molN2O5,達到平衡時,c(O2)為4.5mol?L-1,c(N2O3) 為1.62mol?L-1,則c(N2O5) 為( )
| A.1.44mol?L-1 | B.3.48mol?L-1 | C.0.94mol?L-1 | D.1.98mol?L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
溫度為T時,向2 L恒容密閉容器中充入1 mol PCl5,發生PCl5(g)  PCl3(g) + Cl2(g)反應。反應過程中c(Cl2) 隨時間變化的曲線如下圖所示,下列說法不正確的是
PCl3(g) + Cl2(g)反應。反應過程中c(Cl2) 隨時間變化的曲線如下圖所示,下列說法不正確的是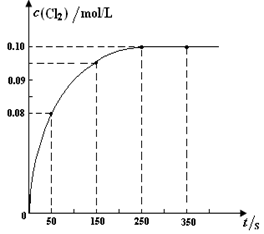
| A.反應在0 ~50 s 的平均速率v(Cl2) =1.6×10-3mol/(L·s) |
| B.該溫度下,反應的平衡常數K = 0.025 |
| C.保持其他條件不變,升高溫度,平衡時c(PCl3)=0.11mol/L,則該反應的ΔH <0 |
| D.反應達平衡后,再向容器中充入1 mol PCl5,該溫度下再達到平衡時,0.1 mol/L<c(Cl2)<0.2 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
現有下列各組溶液:
①10℃時10 mL 0.1 mol·L-1的Na2S2O3溶液和50 mL0.05 mol·L-1的H2SO4溶液;
②10℃時10 mL 0.05 mol·L-1的Na2S2O3溶液和10 mL 0.1 mol·L-1的H2SO4溶液;
③30℃時10 mL 0.05 mol·L-1的Na2S2O3溶液和10 mL 0.1 mol·L-1的H2SO4溶液。
若同時將它們混合發生反應:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,則出現渾濁的先后順序是( )
| A.①②③ | B.②①③ | C.③②① | D.①③② |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com