
A.1∶1 B.2∶1
C.1∶2 D.2∶2
 科學實驗活動冊系列答案
科學實驗活動冊系列答案科目:高中化學 來源: 題型:閱讀理解
| 資料:①H2S可溶于水(約1:2),其水溶液為二元弱酸. ②H2S可與許多金屬離子反應生成沉淀. ③H2S在空氣中燃燒,火焰呈淡藍色. |
| 實驗操作 | 實驗現象 | |
| 實驗1 | 將等濃度的Na2S和Na2SO3溶液按體積比2:1混合 | 無明顯現象 |
| 實驗2 | 將H2S通入Na2SO3溶液中 | 未見明顯沉淀,再加入少量稀硫酸,立即產生大量淺黃色沉淀 |
| 實驗3 | 將SO2通入Na2S溶液中 | 有淺黃色沉淀產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2012-2013學年北京市海淀區高三下學期期末練習理綜化學試卷(解析版) 題型:填空題
硫化氫(H2S)是一種具有臭雞蛋氣味的無色氣體,有劇毒;存在于多種生產過程以及自然界中。在人體的很多生理過程中也起著重要作用。
|
資料:① H2S可溶于水(約1:2),其水溶液為二元弱酸。 ② H2S可與許多金屬離子反應生成沉淀。 ③ H2S在空氣中燃燒,火焰呈淡藍色。 |
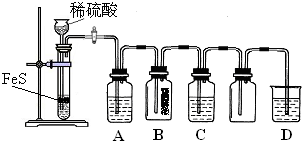
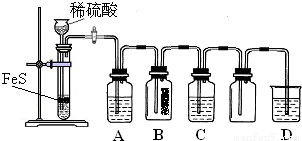
(1)某化學小組設計了制取H2S并驗證其性質的實驗,如下圖所示。A中是CuSO4溶液,B中放有濕潤的藍色石蕊試紙,C中是FeCl3溶液。

回答下列問題:
① A中有黑色沉淀(CuS)產生,A中發生反應的化學方程式為_________________。
② B中的現象是_________。
③ C中只有淺黃色沉淀產生,且溶液變淺綠色。則C中發生反應的離子方程式為_____。
④ D中盛放的試劑可以是____________(填標號)。
a. 水 b. 鹽酸 c. NaCl溶液 d. NaOH溶液
(2)為進一步探究-2價硫的化合物與+4價硫的化合物反應條件,小組同學又設計了下列實驗。
|
|
實驗操作 |
實驗現象 |
|
實驗1 |
將等濃度的Na2S和Na2SO3溶液按體積比2∶1混合 |
無明顯現象 |
|
實驗2 |
將H2S通入Na2SO3溶液中 |
未見明顯沉淀,再加入少量稀硫酸,立即產生大量淺黃色沉淀 |
|
實驗3 |
將SO2通入Na2S溶液中 |
有淺黃色沉淀產生 |
已知:電離平衡常數:H2S Ka1 =1.3×10-7;Ka2 = 7.1×10-15
H2SO3 Ka1 =1.7×10-2;Ka2 = 5.6×10-8
① 根據上述實驗,可以得出結論:在_________條件下,+4價硫的化合物可以氧化-2價硫的化合物。
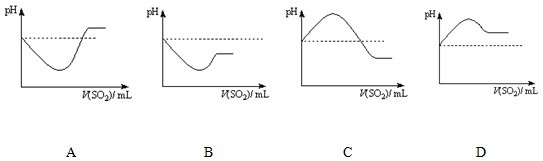
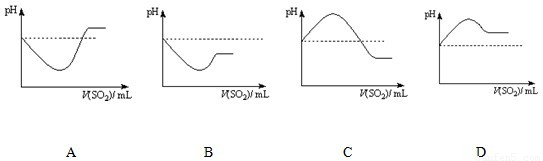
②將SO2氣體通入H2S水溶液中直至過量,下列表示溶液pH隨SO2氣體體積變化關系示意圖正確的是______(填序號)。




A B C D
(3)文獻記載,常溫下H2S可與Ag發生置換反應生成H2。現將H2S氣體通過裝有銀粉的玻璃管,請設計簡單實驗,通過檢驗反應產物證明H2S與Ag發生了置換反應_______。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 資料:①H2S可溶于水(約1:2),其水溶液為二元弱酸. ②H2S可與許多金屬離子反應生成沉淀. ③H2S在空氣中燃燒,火焰呈淡藍色. |

| 實驗操作 | 實驗現象 | |
| 實驗1 | 將等濃度的Na2S和Na2SO3溶液按體積比2:1混合 | 無明顯現象 |
| 實驗2 | 將H2S通入Na2SO3溶液中 | 未見明顯沉淀,再加入少量稀硫酸,立即產生大量淺黃色沉淀 |
| 實驗3 | 將SO2通入Na2S溶液中 | 有淺黃色沉淀產生 |

查看答案和解析>>
科目:高中化學 來源:2013年北京市海淀區高考化學二模試卷(解析版) 題型:填空題
| 資料:①H2S可溶于水(約1:2),其水溶液為二元弱酸. ②H2S可與許多金屬離子反應生成沉淀. ③H2S在空氣中燃燒,火焰呈淡藍色. |
| 實驗操作 | 實驗現象 | |
| 實驗1 | 將等濃度的Na2S和Na2SO3溶液按體積比2:1混合 | 無明顯現象 |
| 實驗2 | 將H2S通入Na2SO3溶液中 | 未見明顯沉淀,再加入少量稀硫酸,立即產生大量淺黃色沉淀 |
| 實驗3 | 將SO2通入Na2S溶液中 | 有淺黃色沉淀產生 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com