
(1)在一定的溫度下,向甲中通入3 mol N2和4 mol H2,反應達到平衡時,生成NH3的物質的量為a mol。?
①相同的溫度下,向乙中通入2 mol NH3,且保持容積與甲相同,當反應達到平衡時,各物質的濃度與甲中平衡時相同。起始時乙中通入 mol N2和 mol H2。?
②相同溫度下,若乙中通入6 mol N2和8 mol H2,且保持壓強與甲相同,當反應達到平衡時,生成NH3的物質的量為b mol,則![]()
![]() ;若乙與甲的容積始終相等,達到平衡時,生成的NH3的物質的量為c mol,則
;若乙與甲的容積始終相等,達到平衡時,生成的NH3的物質的量為c mol,則![]()
![]() (選填“>”“<”“=”)。?
(選填“>”“<”“=”)。?
(2)相同的溫度下,向甲和乙兩容器中分別通入2 mol NH3,甲保持體積不變,乙保持壓強不變。?
①達到平衡時,甲容器速率比乙容器速率 ,甲容器中NH3的轉化率比乙容器 。?
②達到①所述平衡后,若向兩容器中通入數量不多的等量氬氣,甲容器內的化學平衡________移動,乙容器內的化學平衡 移動(選填“向正反應方向”“向逆反應方向”或“不”)。③達到①所述平衡后,測得甲容器平衡體系的平均相對分子質量為M,則此條件下NH3的分解率為 (用M的代數式表示)。?
(1)①2 1 ②= <?
(2)①快 小
②不 向正反應方向
③(![]() -1)×100%
-1)×100%
解析:(1)①根據氮原子和氫原子守恒,得n(N2)=2 mol,n(H2) =1 mol。②在恒溫恒壓下,由于起始時,n(N2)∶n(H2)=3∶4=6∶8,則兩平衡等效,平衡時反應混合物對應各組分的物質的量分數相等,且n(乙)=2n(甲),得b=2a;由于上述平衡時,v(乙)=2v(甲),將乙的容器體積縮小一半,平衡向正反應方向移動,則平衡時c>b=2a。(2)①由于反應2NH3(g)![]() N2(g)+3H2(g)是氣體體積增大的反應,因此達到平衡時,甲容器內的壓強比乙容器內的大,其反應速l;,率快,又增大壓強,平衡向逆反應方向移動,則甲容器中NH3的轉化率比乙容器小。②向兩容器中通入數量不多的等量氬氣,甲容器體積不變,濃度不變,所以平衡不移動;乙容器壓強不變,體積增大,反應混合物濃度減小,則平衡向正反應方向移動。③根據反應的特點,反應前后氣體的物質的量的增加量就是分解的氨氣的物質的量,設有x mol的氨氣發生分解,則M=
N2(g)+3H2(g)是氣體體積增大的反應,因此達到平衡時,甲容器內的壓強比乙容器內的大,其反應速l;,率快,又增大壓強,平衡向逆反應方向移動,則甲容器中NH3的轉化率比乙容器小。②向兩容器中通入數量不多的等量氬氣,甲容器體積不變,濃度不變,所以平衡不移動;乙容器壓強不變,體積增大,反應混合物濃度減小,則平衡向正反應方向移動。③根據反應的特點,反應前后氣體的物質的量的增加量就是分解的氨氣的物質的量,設有x mol的氨氣發生分解,則M=![]() ,x=(
,x=(![]() -2) mol,則NH3的分解率為
-2) mol,則NH3的分解率為![]() ×100%=(
×100%=(![]() -1)×100%。
-1)×100%。


科目:高中化學 來源: 題型:
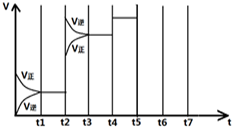 在一定條件下發生化學反應:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.現有容積均為1L的甲、乙兩個容器,在上述條件下分別充入氣體,到達平衡時,反應放出的熱(Q),及平衡時的轉化率(X)如下表所示:
在一定條件下發生化學反應:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.現有容積均為1L的甲、乙兩個容器,在上述條件下分別充入氣體,到達平衡時,反應放出的熱(Q),及平衡時的轉化率(X)如下表所示:| 容器 | 起始時各物質的量 | 到達平衡時放出的熱量(QkJ) | 平衡時SO2轉化率 (X) | |||
| SO2 | O2 | SO3 | N2 | |||
| 甲 | 2 | 1 | 0 | 0 | Q1 | X1 |
| 乙 | 1 | 0.5 | 0 | 1 | Q2= 39.4 |
X2 |
| t 1-t 2 | t 3-t 4 | t 4-t 5 | t 6-t 7 |
| K1 | K2 | K3 | K4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 容積均為1L的甲、乙兩個恒容容器中,分別充入2mol A、2mol B和1mol A、1mol B,相同條件下,發生下列反應:A(g)+B(g)?xC(g)△H<0.測得兩容器中c(A)隨時間t的變化如圖所示,下列說法正確的是( )
容積均為1L的甲、乙兩個恒容容器中,分別充入2mol A、2mol B和1mol A、1mol B,相同條件下,發生下列反應:A(g)+B(g)?xC(g)△H<0.測得兩容器中c(A)隨時間t的變化如圖所示,下列說法正確的是( )| A、該反應的x=3 | B、此條件下,該反應的平衡常數K=4 | C、給乙容器升溫可縮短反應達平衡的時間也能提高平衡轉化率 | D、其他條件不變,向甲容器中再充入0.2mol C,平衡時A的體積分數增大 |
查看答案和解析>>
科目:高中化學 來源:志鴻系列訓練必修一化學人教版 人教版 題型:022
A、B、C、D為中學化學中常見的四種氣體單質.
(1)已知在空氣中A約占21%、C約占78%(均為體積分數);D在標準狀況下的密度為3.170 g·L-1.分別寫出A、C、D的化學式:A________、C________、D________.SO2通入D的水溶液中,可以發生氧化還原反應,其化學方程式為:________.
(2)在一定條件下B與A、C、D化合分別生成甲、乙、丙.已知甲、乙分子中含有的電子數均與Na+相同;乙與丙可化合生成一種離子化合物.
甲、乙的化學式是:甲________、乙________;丙的電子式是:________.
(3)乙可以發生如下圖所示一系列轉化(無關物質及反應條件已略去):
單質A與化合物乙反應的化學方程式為________.
Z的稀溶液與過量鐵粉反應,當反應中有1.806×1023個電子轉移時,被還原的Z物質的量是________mol.
(4)將B、C按體積比為3∶1混合分別裝入盛有催化劑的密閉容器Ⅰ和Ⅱ中(容積相同),若反應過程中容器Ⅰ保持溫度和壓強不變,容器Ⅱ保持溫度和容積不變,當反應達平衡時,容器Ⅰ內氣體的密度________容器Ⅱ內氣體的密度(填“大小”“小于”或“等于”),理由是________.在容器Ⅰ中,當反應達平衡時容積變為起始時的![]() ,則C的轉化率為________.
,則C的轉化率為________.
查看答案和解析>>
科目:高中化學 來源:2010-2011學年黑龍江省高三上學期期末考試化學試卷 題型:填空題
(15分)化學學科中的平衡理論主要包括:化學平衡、電離平衡、水解平衡和溶解平衡四種,且均符合勒夏特列原理。請回答下列問題:
Ⅰ.有甲、乙兩個容積相等的恒容密閉容器,
發生反應3A(g)+B(g)  xC(g)
△H = QKJ/mol
xC(g)
△H = QKJ/mol
回答下列問題:
(1)下列各項能作為判斷該反應達到化學平衡狀態的依據是 (填序號)
① 化學反應速率:v(A)=3v(B) ② 混合氣體的密度保持不變
③ 有3molA消耗的同時有1molB生成 ④ C的濃度保持不變
(2)根據試驗測得的數據可知,溫度越高該反應的化學平衡常數越大,則Q 0(填“大于”或“小于”)
(3)向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC,將兩容器的溫度恒定在770K,使反應3A(g)+B(g)  xc(g)達到平衡,此時測得甲、乙兩容器中C的體積分數均為0.2 。
xc(g)達到平衡,此時測得甲、乙兩容器中C的體積分數均為0.2 。
① 若平衡時,甲、乙兩容器中A的物質的量相等,則x= ;
② 平衡時甲中A的體積分數為 ;
③ 若平衡時兩容器的壓強不相等,則兩容器中壓強之比為
Ⅱ.(1)pH=3的鹽酸a L,分別與下列3種溶液混合,充分反應后溶液呈中性:
①pH=11的氨水b L; ②物質的量濃度為1×10-3 mol/L 氨水c L;
③c(OH-)=1×10-3 mol/L的Ba(OH)2溶液d L;
試判斷a、b、c、d的大小關系正確的是
A.a=b>c>d B.b>a=d>c C.c>a>d>b D.c>a=d>b
(2)已知室溫的條件下,pH均為5的H2SO4溶液和NH4Cl溶液, 兩溶液中c(H+) • c(OH-)=___________;各取5mL上述溶液,分別加水稀釋至50mL,pH較大的是________溶液;各取5mL上述溶液,分別加熱到90℃,pH較小的是________溶液。
(3)同濃度的下列溶液:①NH4Al(SO4)2;②NH4Cl;③NH3·H2O;④CH3COONH4,其中c(NH4+) 由大到小的順序是: (填編號)。
Ⅲ.一定溫度下的難溶電解質AmBn在水溶液中達到沉淀溶解平衡時,其平衡常數Ksp=cm(An+)×cn(Bm—),稱為難溶電解質的溶度積。
(1)在25℃,AgCl的白色懸濁液中,依次加入等濃度的KI溶液和Na2S溶液,觀察到的現象是 ;
(2) 下列敘述不正確的是 (填字母)
A.溶度積小的沉淀可以轉化為溶度積更小的沉淀
B.25℃時,AgCl固體在等物質的量濃度NaCl、CaCl2溶液中的溶度積相同。
C.25℃時,飽和AgCl、AgI、Ag2S溶液中所含Ag+的濃度相同
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com