
【題目】下列離子方程式中正確的是
A. 向沸水中滴加FeCl3溶液制備Fe(OH)3膠體:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B. 小蘇打與氫氧化鈉溶液混合:HCO3-+OH-=CO2↑+H2O
C. NaHSO4溶液與Ba(OH)2溶液混合后呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D. 二氧化錳和濃鹽酸共熱:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
【答案】D
【解析】
A項,向沸水中滴加FeCl3溶液制備Fe(OH)3膠體,離子方程式為:Fe3++3H2O![]() Fe(OH)3(膠體)+3H+,故A錯誤;B項,小蘇打與氫氧化鈉溶液混合,反應離子方程式為:HCO3-+OH-=CO32-+H2O,故B錯誤;C項,NaHSO4溶液與Ba(OH)2溶液混合后呈中性,反應離子方程式為:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故C錯誤;D項,二氧化錳和濃鹽酸共熱,生成氯化錳、氯氣和水,書寫離子方程式時,可溶性的強電解質拆成離子形式,所以離子方程式為:MnO2+4H++2Cl-
Fe(OH)3(膠體)+3H+,故A錯誤;B項,小蘇打與氫氧化鈉溶液混合,反應離子方程式為:HCO3-+OH-=CO32-+H2O,故B錯誤;C項,NaHSO4溶液與Ba(OH)2溶液混合后呈中性,反應離子方程式為:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故C錯誤;D項,二氧化錳和濃鹽酸共熱,生成氯化錳、氯氣和水,書寫離子方程式時,可溶性的強電解質拆成離子形式,所以離子方程式為:MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O,故D正確。
Mn2++Cl2↑+2H2O,故D正確。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】汽車尾氣中通常含有NxOy和CO等大氣污染物,科學家尋找高效催化劑實現了汽車尾氣的轉化進而減少汽車尾氣對大氣的污染。
(1)己知:①CO的燃燒熱△H1=-283kJ·mol-1 ②N2(g)+O2(g) =2NO(g) △H2 =+183kJ·mol-1
由此寫出NO和CO反應的熱化學反應方程式________________________________。
(2)一定溫度下,向2L密閉容器中充入4.0mo1NO2和4.0molCO,在催化劑作用下發生反應 4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H<0,測得相關數據如下:
N2(g)+4CO2(g) △H<0,測得相關數據如下:
0 min | 5 min | 10 min | 15 min | 20 min | |
c(NO2)/ mol·L-1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
C(N2)/ mol·L-1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①5l0min,用N2的濃度變化表示的反應速率為__________________。
②以下表述能說明該反應己達到平衡狀態的是________。
A.氣體顏色不再變化 B.氣體密度不再變化 C.氣體平均相對分子質量不再變化
③20 min時,保持溫度不變,繼續向容器中加入1.0mol NO2和1.0molCO,在t1時刻反應再次達到平衡,則NO2的轉化率比原平衡 ______________(填“增大”、“減小”或“不變)。
④該溫度下反應的化學平衡常數K= __________ (保留兩位有效數字)。
(3)CO、空氣與過量KOH溶液可構成燃料電池(石墨為電極):
①寫出該電池的負極反應式____________________________;
②常溫下,用該燃料電池電解(惰性電極)1L飽和食鹽水(足量),當兩極共生成4.48L (折算為標準狀況)氣體時電解池溶液的pH=__________。(忽略溶液的體積變化,己知1g2=0.3,lg5=0.7)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)用系統命名法命名下列有機物
①CH3CH(C2H5)CH(CH3)2 ________________________________________
②![]() ______________________________________________________
______________________________________________________
(2)寫出下列物質的結構簡式
①對二甲苯________________________________________
②2-甲基-1,3-丁二烯________________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. FeCl3溶液可用于銅質印刷線路板的制作,該反應是置換反應
B. 向純堿溶液中滴加醋酸,將生成的氣體通入澄清的苯酚鈉溶液中,觀察是否出現沉淀,由此證明醋酸、碳酸、苯酚酸性強弱
C. 反應A(g)![]() B(g) △H,若正反應的活化能為EakJ/mol,逆反應的活化能為EbkJ/mol,則△H=-(Ea-Eb)kJ/mol
B(g) △H,若正反應的活化能為EakJ/mol,逆反應的活化能為EbkJ/mol,則△H=-(Ea-Eb)kJ/mol
D. 3x%的A物質的溶液與x%的A物質的溶液等體積混合后,溶液的質量分數小于2x%,則A物質可能為乙醇
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉆(Co)及其化合物在工業上有廣泛應用。為從某工業廢料中回收鈷,某學生設計流程如圖(廢料中含有Al、Li、Co2O3和Fe2O3等物質)。
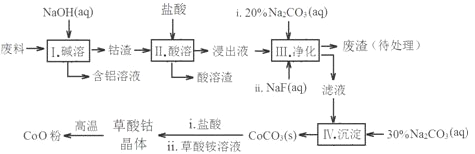
已知:LiF難溶于水,Li2CO3微溶于水。
請回答:
(1)寫出I中發生反應的化學方程式并用單線橋標記電子轉移的方向和數目________。
(2)寫出步驟中Co2O3與鹽酸反應生成Cl2的離子方程式_______________。
(3)步驟II所得廢渣的主要成分除了LiF外,還有________________。
(4)NaF與溶液中的Li+形成LiF沉淀,此反應對步驟IV所起的作用是___________。
(5)在空氣中加熱10.98g草酸鈷晶體(CoC2O42H2O)樣品,受熱過程中不同溫度范圍內分別得到一種固體物質,其質量如下表。己知:M(CoC2O42H2O)=183g/mol。
溫度范圍/℃ | 固體質量/g |
150--210 | 8.82 |
290--320 | 4.82 |
890--920 | 4.5 |
經測定,加熱到210℃時,固體物質的化學式為_____。加熱到210--290℃過程中產生的氣體只有CO2,此過程發生反應的化學方程式是_________。溫度高于890℃時,固體產物發生分解反應,固體產物為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A是一種重要的化工原料,A的產量可以用來衡量一個國家的石油化工水平,E是具有果香氣味的烴的衍生物。A、B、C、D、E在一定條件下存在如下轉化關系(部分反應條件、產物被省略)。
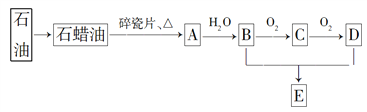
(已知乙醛在一定條件下可被氧化生成乙酸)
(1)丁烷是由石蠟油獲得A的過程中的中間產物之一,它的一種同分異構體中含有三個甲基,則這種同分異構體的結構簡式為________。
(2)B、D分子中官能團的名稱分別是________、________,A→B的反應類型是________。
(3)寫出反應A→B 、B→C的化學方程式:____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關周期表的說法正確的是( )
A.短周期是第一、二、三、四周期B.元素周期表有18個族
C.第IA族的元素全部是金屬元素D.元素周期表含元素最多的族是副族
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com