
一定條件下,在一個具有活塞的密閉容器中充入NH3和Cl2,反應恰好完成,若生成物只有N2和HCl,則反應前后體積之比為( )
A.5∶7 B.7∶5 C.7∶11 D.11∶7
科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
(16分)應用化學反應需要研究化學反應的條件、限度和速率。
(1)已知反應:Br2+2Fe2+=2Br-+2Fe3+ ,向10mL 0.1 mol·L-1的FeBr2溶液中通入0.001 mol Cl2,反應后,溶液中除含有Cl-外,還一定有 (填序號)。
①含Fe2+,不含Fe3+② 含Fe3+,不含Br-③ 含Fe3+,還含有Br-
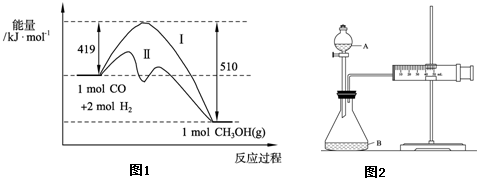
(2)773 K、固定體積的容器中,反應CO(g)+2H2(g)CH3OH(g)過程中能量變化如下圖。曲線Ⅱ表示使用催化劑時的能量變化。若投入amol CO、2a mol H2,平衡時能生成0.1a mol CH3OH,反應就具工業應用價值。
①若按上述投料比使該反應具有工業應用價值,CO的平衡轉化率最小為 ;
②在容器容積不變的前提下,欲提高H2的轉化率,可采取的措施(答兩項即可) 、 ;
③下列與催化劑有關的說法中,正確的是 (填字母序號)。
a. 使用催化劑,使反應CO(g)+2H2(g)CH3OH(g) ΔH>-91kJ·mol-1
b. 使用催化劑, 能夠提高反應物轉化率
c. 使用催化劑,不能改變反應的平衡常數K
(3)高鐵酸鹽在能源環保領域有廣泛用途。我國學者提出用鎳(Ni)、鐵作電極電解濃NaOH溶液制備高鐵酸鹽Na2FeO4的方案,裝置如右圖所示。
① Ni作 (填“陰”或“陽”)極;
②Ni電極的電極反應式為: 。
(4)氧化還原反應中實際上包含氧化和還原兩個過程。下面是HNO3發生的一個還原過程的反應式:NO-3+4H++3e-→NO+2H2O
①KMnO4、HCl、Fe(NO3)2、CuO、KI五種物質中的 (填化學式)能使上述還原過程發生。
②欲用下圖裝置通過測定氣體生成量測算硝酸被還原的速率,當反應物的濃度、用量及其他影響速率的條件確定之后,可以通過測定 推(計)算反應速率。
查看答案和解析>>
科目:高中化學 來源:2010年福建省廈門外國語學校高三模擬考試(理綜)化學部分 題型:填空題
(16分)應用化學反應需要研究化學反應的條件、限度和速率。
(1)已知反應:Br2+2Fe2+=2Br-+2Fe3+,向10 mL 0.1 mol·L-1的FeBr2溶液中通入0.001 mol Cl2,反應后,溶液中除含有Cl-外,還一定有 (填序號)。
①含Fe2+,不含Fe3+②含Fe3+,不含Br-③含Fe3+,還含有Br-
(2)773 K、固定體積的容器中,反應CO(g)+2H2(g) CH3OH(g)過程中能量變化如下圖。曲線Ⅱ表示使用催化劑時的能量變化。若投入a mol CO、2a mol H2,平衡時能生成0.1a mol CH3OH,反應就具工業應用價值。
CH3OH(g)過程中能量變化如下圖。曲線Ⅱ表示使用催化劑時的能量變化。若投入a mol CO、2a mol H2,平衡時能生成0.1a mol CH3OH,反應就具工業應用價值。
①若按上述投料比使該反應具有工業應用價值,CO的平衡轉化率最小為 ;
②在容器容積不變的前提下,欲提高H2的轉化率,可采取的措施(答兩項即可) 、 ;
③下列與催化劑有關的說法中,正確的是 (填字母序號)。
a. 使用催化劑,使反應CO(g)+2H2(g) CH3OH(g) ΔH>-91 kJ·mol-1
CH3OH(g) ΔH>-91 kJ·mol-1
b. 使用催化劑, 能夠提高反應物轉化率
c. 使用催化劑,不能改變反應的平衡常數K
(3)高鐵酸鹽在能源環保領域有廣泛用途。我國學者提出用鎳(Ni)、鐵作電極電解濃NaOH溶液制備高鐵酸鹽Na2FeO4的方案,裝置如右圖所示。
① Ni作 (填“陰”或“陽”) 極;
②Ni電極的電極反應式為: 。
。
(4)氧化還原反應中實際上包含氧化和還原兩個過程。下面是HNO3發生的一個還原過程的反應式:NO-3+4H++3e-→NO+2H2O
①KMnO4、HCl、Fe(NO3)2、CuO、KI五種物質中的 (填化學式)能使上述還原過程發生。
②欲用下圖裝置通過測定氣體生成量測算硝酸被還原的速率,當反應物的濃度、用量及其他影響速率的條件確定之后,可以通過測定 推(計)算反應速率。
查看答案和解析>>
科目:高中化學 來源:2010年福建省高三模擬考試(理綜)化學部分 題型:填空題
(16分)應用化學反應需要研究化學反應的條件、限度和速率。
(1)已知反應:Br2+2Fe2+=2Br-+2Fe3+ ,向10 mL 0.1 mol·L-1的FeBr2溶液中通入0.001 mol Cl2,反應后,溶液中除含有Cl-外,還一定有 (填序號)。
①含Fe2+,不含Fe3+② 含Fe3+,不含Br-③ 含Fe3+,還含有Br-
(2)773 K、固定體積的容器中,反應CO(g)+2H2(g) CH3OH(g)過程中能量變化如下圖。曲線Ⅱ表示使用催化劑時的能量變化。若投入a
mol CO、2a mol H2,平衡時能生成0.1a mol CH3OH,反應就具工業應用價值。
CH3OH(g)過程中能量變化如下圖。曲線Ⅱ表示使用催化劑時的能量變化。若投入a
mol CO、2a mol H2,平衡時能生成0.1a mol CH3OH,反應就具工業應用價值。

①若按上述投料比使該反應具有工業應用價值,CO的平衡轉化率最小為 ;
②在容器容積不變的前提下,欲提高H2的轉化率,可采取的措施(答兩項即可) 、 ;
③下列與催化劑有關的說法中,正確的是 (填字母序號)。
a. 使用催化劑,使反應CO(g)+2H2(g) CH3OH(g) ΔH>-91
kJ·mol-1
CH3OH(g) ΔH>-91
kJ·mol-1
b. 使用催化劑, 能夠提高反應物轉化率
c. 使用催化劑,不能改變反應的平衡常數K
(3)高鐵酸鹽在能源環保領域有廣泛用途。我國學者提出用鎳(Ni)、鐵作電極電解濃NaOH溶液制備高鐵酸鹽Na2FeO4的方案,裝置如右圖所示。

① Ni作 (填“陰”或“陽”) 極;
②Ni電極的電極反應式為: 。
(4)氧化還原反應中實際上包含氧化和還原兩個過程。下面是HNO3發生的一個還原過程的反應式:NO-3+4H++3e-→NO+2H2O
①KMnO4、HCl、Fe(NO3)2、CuO、KI五種物質中的 (填化學式)能使上述還原過程發生。
②欲用下圖裝置通過測定氣體生成量測算硝酸被還原的速率,當反應物的濃度、用量及其他影響速率的條件確定之后,可以通過測定 推(計)算反應速率。

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
應用化學反應需要研究化學反應的條件、限度和速率。
(1)已知反應:Br2+2Fe2+=2Br-+2Fe3+ ,向10 mL 0.1 mol·L-1的FeBr2溶液中通入0.001 mol Cl2,反應后,溶液中除含有Cl-外,還一定有 (填序號)。
①含Fe2+,不含Fe3+② 含Fe3+,不含Br-③ 含Fe3+,還含有Br-
(2)773 K、固定體積的容器中,反應CO(g)+2H2(g)![]() CH3OH(g)過程中能量變化如下圖。曲線Ⅱ表示使用催化劑時的能量變化。若投入a mol CO、2a mol H2,平衡時能生成0.1a mol CH3OH,反應就具工業應用價值。
CH3OH(g)過程中能量變化如下圖。曲線Ⅱ表示使用催化劑時的能量變化。若投入a mol CO、2a mol H2,平衡時能生成0.1a mol CH3OH,反應就具工業應用價值。
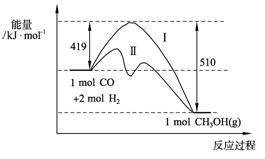
①若按上述投料比使該反應具有工業應用價值,CO的平衡轉化率最小為 ;
②在容器容積不變的前提下,欲提高H2的轉化率,可采取的措施(答兩項即可) 、 ;
③下列與催化劑有關的說法中,正確的是 (填字母序號)。
a. 使用催化劑,使反應CO(g)+2H2(g)![]() CH3OH(g) ΔH>-91 kJ·mol-1
CH3OH(g) ΔH>-91 kJ·mol-1
b. 使用催化劑, 能夠提高反應物轉化率
c. 使用催化劑,不能改變反應的平衡常數K
(3)高鐵酸鹽在能源環保領域有廣泛用途。我國學者提出用鎳(Ni)、鐵作電極電解濃NaOH溶液制備高鐵酸鹽Na2FeO4的方案,裝置如右圖所示。
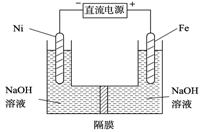
① Ni作 (填“陰”或“陽”) 極;
②Ni電極的電極反應式為: 。
(4)氧化還原反應中實際上包含氧化和還原兩個過程。下面是HNO3發生的一個還原過程的反應式:NO-3+4H++3e-→NO+2H2O
①KMnO4、HCl、Fe(NO3)2、CuO、KI五種物質中的 (填化學式)能使上述還原過程發生。
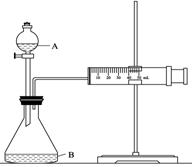
②欲用下圖裝置通過測定氣體生成量測算硝酸被還原的速率,當反應物的濃度、用量及其他影響速率的條件確定之后,可以通過測定 推(計)算反應速率。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com