
【題目】【化學---選修3:物質結構與性質】原子序數小于36的X、Y、Z、W四種元素,其中X是半徑最小的元素,Y原子基態時最外層電子數是其內層電子總數的2倍,Z原子基態時2p原子軌道上有3個未成對的電子,W原子4s原子軌道上有1個電子,M能層為全充滿的飽和結構。回答下列問題:

(1)W基態原子的價電子排布式____________;Y2X2分子中Y原子軌道的雜化類型為______。
(2)化合物ZX3的沸點比化合物YX4的高,其主要原因是_____________。
(3)元素Y的一種氧化物與元素Z的一種氧化物互為等電子體,元素Z的這種氧化物的分子式是____________。Y60用做比金屬及其合金更為有效的新型吸氫材料,其分子結構為球形32面體,它是由60個Y原子以20個六元環和12個五元環連接而成的具有30個Y=Y鍵的足球狀空心對稱分子。則該分子中σ鍵和π鍵的個數比_____;36gY60最多可以吸收標準狀況下的氫氣_____L。
(4)元素W的一種氯化物晶體的晶胞結構如右圖所示,該氯化物的化學式是___________,該晶體中W的配位數為___________。它可與濃鹽酸發生非氧化還原反應,生成配合物HnWCl3,反應的化學方程式為_________。
【答案】(1)3d104s1 sp雜化(2)NH3分子間存在氫鍵(3)N2O 3:1 33.6L
(4)CuCl 4 CuCl+2HCl=H2CuCl3(或CuCl+2HCl=H2[CuCl3])
【解析】
試題分析:原子序數小于36的X、Y、Z、W四種元素,其中X是半徑最小的元素,則X是H;Y原子基態時最外層電子數是其內層電子總數的2倍,則Y是C;Z原子基態時2p原子軌道上有3個未成對的電子,所以Z是N;W原子4s原子軌道上有1個電子,M能層為全充滿的飽和結構,則W是Cu。
(1)銅基態原子的價電子排布式3d104s1;Y2X2分子是乙炔,乙炔是直線形結構,則分子中碳原子軌道的雜化類型為sp雜化。
(2) NH3分子間存在氫鍵,其沸點高于甲烷。
(3)元素Y的一種氧化物與元素Z的一種氧化物互為等電子體,由于互為等電子體的原子數和價電子數分別均相等,則元素Z的這種氧化物的分子式是N2O。C60分子構型為一個32面體,其中有12個五元環,20個六元環,每個碳周圍有一個碳碳雙鍵和兩個碳碳單鍵,均為兩個碳共用,所以每個碳實際占有的碳碳單鍵是1個,碳碳雙鍵數為0.5個,而每個雙鍵中有一個π鍵和σ鍵,而單鍵都是σ鍵,則該分子中σ鍵和π鍵的個數比![]() ;C60分子中含有的碳碳雙鍵個數是30,一個碳碳雙鍵需要1分子氫氣加成,因此36gC60最多可以吸收標準狀況下的氫氣
;C60分子中含有的碳碳雙鍵個數是30,一個碳碳雙鍵需要1分子氫氣加成,因此36gC60最多可以吸收標準狀況下的氫氣![]() 。
。
(4)根據晶胞結構可知晶胞中銅原子的個數是8×1/8+6×1/2=4,氯原子全部在晶胞內,共計4個,因此該氯化物的化學式是CuCl,該晶體中W的配位數為4。它可與濃鹽酸發生非氧化還原反應,生成配合物HnWCl3,反應的化學方程式為CuCl+2HCl=H2CuCl3(或CuCl+2HCl=H2[CuCl3])。


科目:高中化學 來源: 題型:
【題目】回答下列問題:
(1)下圖為四種粒子的結構示意圖,完成以下填空:
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
屬于陽離子結構的粒子是________(填字母序號,下同);A粒子的半徑________B粒子的半徑(填“>”、“<”或“=”)。
(2)有機物M經過太陽光光照可轉化成N,轉化過程如下:

![]()
 ΔH = +88.6 kJ·mol-1
ΔH = +88.6 kJ·mol-1
則M、N相比,較穩定的是____________。
(3) 由氫氣和氧氣反應生成1 mol水蒸氣放出熱量241.8 kJ,寫出該反應的熱化學方程式為:_____________________________________________________。
(4)一定溫度下在某定容容器中發生反應:2A(g)+3B(g)![]() 2C(g),開始時,A的濃度為2 mol·L-1,B的濃度為4 mol·L-1,2 min后,A的濃度減少0.8 mol·L-1,則
2C(g),開始時,A的濃度為2 mol·L-1,B的濃度為4 mol·L-1,2 min后,A的濃度減少0.8 mol·L-1,則
① v(B)=____________,v(C)=__________。
② 在2 min末,C的濃度是__________,B的濃度是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計下列實驗,來研究硫酸和硝酸的性質。

實驗一:在一支試管中放入一塊很小的銅片,再加入2 mL濃硫酸,然后把試管固定在鐵架臺上。把一小條蘸有品紅溶液的濾紙放入帶有單孔橡皮塞的玻璃管中。塞緊試管口,在玻璃管口處纏放一團蘸有Na2CO3溶液的棉花。給試管加熱,觀察現象。當試管中的液體逐漸透明時,停止加熱。待試管中的液體冷卻后,將試管中的液體慢慢倒入另一支盛有少量水的試管中,觀察現象。
回答下列問題:
(1)a處反應的化學方程式為________________________________,計算放出112 mL氣體(標準狀況),轉移電子的物質的量為________________。
(2)試管中的液體反應一段時間后,b處濾紙條的變化為________________________。
待試管中反應停止后,給玻璃管放有蘸過品紅溶液的濾紙處微微加熱,濾紙條的變化為__________________________________________________________________。
實驗二:為了證明銅與稀硝酸反應產生一氧化氮,某同學設計了一個實驗,其裝置如下圖所示(加熱裝置和固定裝置均已略去)。A為注射器,B為兩端長短不等的U形管,C是裝有NaOH溶液的燒杯,D處是繞成螺旋狀的銅絲,K1、K2是止水夾。

(1)實驗時,為在D處收集到NO,以便觀察顏色,必須事先在A中吸入一定量的空氣。然后__________K1(“關閉”或“打開”),從U形管左端注入稀硝酸,當看到________________________現象可以確定U形管中空氣已被趕盡。
(2)然后給裝置B微微加熱,在裝置D處產生無色氣體,其反應的離子方程式為:
________________________________________________________________________。
(3)如何證明D處聚集的是NO而不是H2?
________________________________________________________________________。
(4)實驗現象觀察完畢,關閉止水夾K1,打開止水夾K2,在重力作用下,U形管右端的紅棕色混合氣體被酸液壓入NaOH溶液中吸收,消除了環境污染。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】IA、B、C、D四種元素的核電荷數均小于18,A元素原子核外只有1個電子;B是地殼中含量最多的元素;B、C可形成兩種化合物CB和CB2,C的最高正價與最低負價絕對值相等,CB有毒,CB2可用于滅火;D+具有與Ne原子相同的電子層結構。

(1)試判斷A、B、C、D四種元素的名稱。A______,B_____,C______,D______。
(2)C在周期表中的位置是 。
(3)由B、D兩種元素組成的D2B2型化合物的電子式為_______,CB2的電子式 為________。
(4)如右圖所示,在燒瓶中收集滿CB2氣體,用帶導管(導管一端事先綁好一個氣球)的膠塞緊,當打開膠塞迅速倒入濃的A、B、D三種元素組成的化合物的溶液后,立即塞緊膠塞振蕩,可觀察到_____,原因是_____________。
II(9分)下表是元素周期表的一部分, 針對表中的①~⑩種元素,填寫下列空白:
主族K] | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | [m] | ⑩ |
(1)在最高價氧化物的水化物中,酸性最強的化合物的分子式是: ,堿性最強的化合物的電子式是: 。
(2)最高價氧化物是兩性氧化物的元素是 ;寫出它的氧化物與氫氧化鈉反應的離子方程式 。
(3)用電子式表示元素④與⑥的化合物的形成過程:
(4)表示①與⑦的化合物的電子式 ,該化合物是由 (填“極性”“非極性”)鍵形成的。
(5)③、⑥、⑦三種元素形成的離子,離子半徑由大到小的順序是______(要求用離子符號表示)。
(6)元素③的氫化物常溫下和元素⑦的單質反應的離子方程式為: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(化學—選修3:物質結構與性質)
氮化硼(BN)被稱為一種“宇宙時代的材料”,具有很大的硬度。
(1)基態硼原子有__________個未成對電子,氮離子的電子排布式為__________。
(2)部分硼的化合物有以下轉化:![]()
則下列敘述正確的是__________(填序號);
A.B3N3H6俗稱無機苯,但不是平面分子
B.BNH6與乙烷是等電子體
C.HB≡NH中的硼原子、氮原子韻雜化類型相同
D.硼、氮、氧三元素的第一電離能比較:B<N<O
(3)下圖的晶體結構中,黑球白球分別代表不同的原子、離子或分子,則圖1的晶胞中含有的粒子總數為__________;圖2中的白球的配位數是__________。

(4)已知圖3、4均表示BN晶體的結構,制備氮化硼的原理為:BCl3+2NH3=BN+2HCl+NH4Cl,當該反應中有1mol BN生成時,則反應中可形成__________mol配位鍵,比較氮化硼晶體與晶體硅的沸點高低并解釋原因____________________。
(5)X射線的衍射實驗可獲取晶體的結構,包括晶胞形狀、大小及原子的分布等參數,從而提供了又一種實驗測定阿伏加德羅常數和元素的相對質量的方法。若圖4晶胞的棱長為a nm,密度為ρ g·cm-3,則阿伏加德羅常數為__________(要求化為最簡關系)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將57.6克的銅投入200毫升的硝酸溶液中恰好反應完全,產生標準狀況下的NO2 、NO共1.4 mol。
(1)寫出剛開始反應的化學方程式
(2)求硝酸的濃度 mol·L-1
(3)將生成的氣體收集在大試管中,然后倒扣在水中,寫出二氧化氮與水反應的化學方程式 ,若反應完全,則最后試管中NO的物質的量 mol。若往試管中通入氧氣讓液體充滿試管問通入氧氣的物質的量 mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【選修3:物質結構與性質】
在電解冶練鋁的過程中加入冰晶石,可起到降低Al2O3熔點的作用。冰晶石的生產原理為2Al(OH)3+12HF+3Na2CO3═2Na3AlF6+3CO2↑+9H2O.根據題意完成下列填空:
(1)冰晶石的晶體不導電,但熔融時能導電,則在冰晶石晶體中存在__________(填序號).
a.離子鍵 b.極性鍵 c.配位鍵 d.范德華力
(2)CO2分子的空間構型為__________,中心原子的雜化方式為__________,和CO2 互為等電子體的氧化物是__________;
(3)反應物中電負性最大的元素為_________(填元素符號),寫出其原子最外層的電子排布圖__________;
(4)冰晶石由兩種微粒構成,冰晶石的晶胞結構如圖甲所示,●位于大立方體的頂點和面心,○位于大立方體的12條棱的中點和8個小立方體的體心,那么大立方體的體心處所代表的微粒是______(填具體的微粒符號).
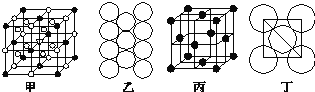
(5)Al單質的晶體中原子的堆積方式如圖乙所示,其晶胞特征如圖丙所示,原子之間相互位置關系的平面圖如圖丁所示:
若已知Al的原子半徑為d cm,NA代表阿伏伽德羅常數,Al的相對原子質量為M,則一個晶胞中Al原子的數目為_________個;Al晶體的密度為__________(用字母表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素X、Y、Z、W、Q在元素周期表中的相對位置如圖。下列說法正確的是( )

A. Y、Z的常見氧化物可通過加入過量的NaOH溶液來分離
B. 其氫化物的穩定性由弱到強的順序是Q、W、Z
C. 元素Y、Z、W、Q的原子半徑依次增大
D. Y單質做的容器可盛裝W的最高價氧化物對應的水化物的濃溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,向某密閉容器中加入1molN2和4molH2,使之反應合成NH3,平衡后測得NH3的體積分數為m。若T不變,只改變起始加入的物質的量,使之反應平衡后NH3的體積分數仍為m,若N2、H2、NH3的加入量用X、Y、Z表示應滿足:
(1)恒定T、V:
[1]若X=0,Y=1,則Z= 。
[2]若X=0.75,Y= ,Z=0.5。
[3]X、Y、Z應滿足的一般條件是(分別用只含X、Z和只含Y、Z寫兩個方程式表示) 。
(2)恒定T、P:
[1]若X=1、Y= ,則Z=2。
[2]若X=2,則Y=10,Z= 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com