
分析 (1)熱化學方程式要標明物質的聚集狀態,并且焓變的符號和單位要正確,根據熱化學方程式的書寫方法來回答;
(2)結合化學反應④⑤,利用蓋斯定律來回答;
(3)燃燒熱是指在25℃,101kPa時,1mol可燃物完全燃燒生成穩定的氧化物時所放出的熱量,中和熱是指稀的強酸和強堿反應生成1mol水所放出的熱量,據此分析.
解答 解:(1)根據熱化學方程式的書寫方法,②C(s)+H2O(g)═CO(g)+H2(g)是吸熱反應,△H應該大于0,即△H=+131.3KJ/mol;
故答案為:②;該反應為吸熱反應,△H應該大于0;
(2)已知④C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
⑤2CO(g)+O2(g)═2CO2(g)△H=-564kJ/mol
利用蓋斯定律,④-⑤×$\frac{1}{2}$得到反應C(s)+$\frac{1}{2}$O2(g)=CO(g),所以焓變△H=-111.5KJ/mol,則C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-111.5KJ/mol;
故答案為:C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-111.5KJ/mol;
(3)上述反應中,④分別是表示C的燃燒熱的熱化學方程式,⑥表示的是中和熱的熱化學方程式,
故答案為:④;⑥.
點評 本題考查學生熱化學方程式的書寫方法以及蓋斯定律計算化學反應的焓變等知識,注意知識的歸納和整理是解題關鍵,難度不大,側重于考查學生對基礎知識的應用能力和計算能力.


 能力評價系列答案
能力評價系列答案 唐印文化課時測評系列答案
唐印文化課時測評系列答案 導學與測試系列答案
導學與測試系列答案科目:高中化學 來源: 題型:解答題
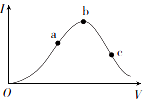 一定溫度下,在向冰醋酸(無水醋酸)加水稀釋的過程中,溶液的導電能力(I)隨著加入水的體積V變化的曲線如圖所示.
一定溫度下,在向冰醋酸(無水醋酸)加水稀釋的過程中,溶液的導電能力(I)隨著加入水的體積V變化的曲線如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 陽離子 | 陰離子 | ||
| OH- | SO42- | SO32- | |
| Ca2+ | ① | 微 | 不 |
| Fe3+ | 不 | 溶 | ② |
| Cu2+ | 不 | ③ | 不 |
| A. | ①處物質屬于可溶性堿 | |
| B. | ②處物質組成為Fe2(SO3)3 | |
| C. | ③處物質為硫酸鹽或者銅鹽 | |
| D. | ①、③處物質在溶液中發生的反應一定是Cu2++2OH-═Cu(OH)2↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 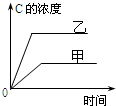 研究的是溫度對反應的影響,且乙的溫度較高 | |
| B. | 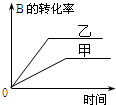 研究的是壓強對反應的影響,且甲的壓強較高 | |
| C. | 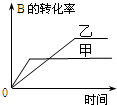 研究的是溫度對反應的影響,且乙的溫度較高 | |
| D. | 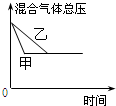 研究的是不同催化劑對反應的影響,且甲使用的催化劑效率較高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 通入氦氣使密閉容器中壓強增大,平衡向正反應方向移動 | |
| B. | 增加X的物質的量,混合氣體的密度減小 | |
| C. | X的正反應速率是Y的逆反應速率的$\frac{m}{n}$倍 | |
| D. | 降低溫度,混合氣體的平均相對分子質量增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ksp的數值只與溫度有關 | |
| B. | Ksp的數值只與難溶電解質的性質和溫度有關 | |
| C. | Ksp的大小與沉淀量有多少和溶液中離子濃度的大小有關 | |
| D. | Ksp的數值越大,電解質在水中的溶解能力越強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
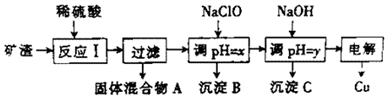
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 開始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
| 沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com