
在一定溫度下,反應A2(g)+B2(g) ![]() 2AB(g)達到平衡狀態的標志是______
2AB(g)達到平衡狀態的標志是______
A.單位時間內生成n mol A2的同時生成n mol AB
B.容器內的總壓強不隨時間變化
C.單位時間內生成2n mol AB的同時生成n mol B2
D.單位時間內生成n mol A2的同時生成n mol B2
E.容器內A2、B2、AB的物質的量之比是1∶1∶2時的狀態
F.容器中[A2]=[B2]=[AB]時的狀態
解析:化學平衡狀態的根本標志是v(正)=v(逆),或平衡混合物中各組分的濃度或質量分數、體積分數等保持不變。只要具備上述兩點之一,便一定是平衡狀態;否則,不能確定為平衡狀態。A項,根據化學方程式中的化學計量數之比,可知生成n mol AB必消耗![]() mol A2,即單位時間內生成
mol A2,即單位時間內生成![]() mol A2的同時生成n mol AB,顯然反應未達到平衡狀態。B項,是從壓強方面來敘述的。由于此反應是反應前后氣體分子數不變的反應,達到平衡或未達到平衡時壓強都不隨時間變化,因此不能用壓強來說明反應是否達到平衡狀態。C項,由題意可知當單位時間內生成2n mol AB時,也就消耗了n mol A2和n mol B2,這樣同一時刻相同容積的容器中消耗的A2和生成的A2都是n mol,說明反應處于平衡狀態。D項,只知道單位時間生成n mol A2和n mol B2,卻不知道同時消耗多少A2和多少B2,故無法確定反應是否達到平衡。E、F兩項是以混合物成分的含量來敘述的。由于達到化學平衡狀態時,反應混合物中各物質的濃度保持不變,并不是相等,也不是它們的分子數之比一定等于其化學方程式中各物質的化學計量數之比,所以E、F兩項不符合題意。
mol A2的同時生成n mol AB,顯然反應未達到平衡狀態。B項,是從壓強方面來敘述的。由于此反應是反應前后氣體分子數不變的反應,達到平衡或未達到平衡時壓強都不隨時間變化,因此不能用壓強來說明反應是否達到平衡狀態。C項,由題意可知當單位時間內生成2n mol AB時,也就消耗了n mol A2和n mol B2,這樣同一時刻相同容積的容器中消耗的A2和生成的A2都是n mol,說明反應處于平衡狀態。D項,只知道單位時間生成n mol A2和n mol B2,卻不知道同時消耗多少A2和多少B2,故無法確定反應是否達到平衡。E、F兩項是以混合物成分的含量來敘述的。由于達到化學平衡狀態時,反應混合物中各物質的濃度保持不變,并不是相等,也不是它們的分子數之比一定等于其化學方程式中各物質的化學計量數之比,所以E、F兩項不符合題意。
答案:C


 優翼小幫手同步口算系列答案
優翼小幫手同步口算系列答案科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
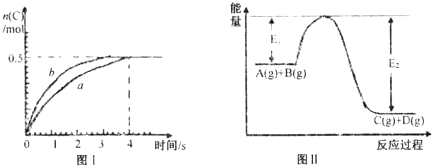
| A、此反應過程中的能量變化可用上圖II表示 | B、此溫度下,該反應的平衡常數的值為1 | C、該反應4s內平均速率v(A)=0.125mol?L-1?s-1 | D、若在恒溫加大反應容器的容積條件下,該反應將按b曲線進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:021
在一定溫度下,反應
A(氣)+B(氣)[ ]
A.正反應速率增大時,平衡將向右移動B.升高溫度平衡向左移動,則正反應肯定是放熱反應
C.使用催化劑時,正、逆反應速率同等加快,平衡不會發生移動
D.增大壓強,將會使平衡向正反應方向移動
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com