
【題目】下列實驗或操作方法正確的是
A. 用蘸有待測液的鐵絲,檢驗K+ 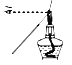
B. 從食鹽水中提取氯化鈉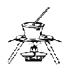
C. 驗證NaHCO3和Na2CO3的熱穩定性 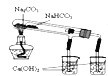
D. 分離水與乙醇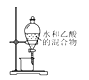
科目:高中化學 來源: 題型:
【題目】設NA表示阿伏加德羅常數,下列說法正確的是
A. 標準狀況下,22.4L氦氣與lmol氫氣所含原子數均為NA
B. 1L0.l mol/LNaHCO3溶液中含有 0.1NA個 HCO3-
C. 己知可將0.lmolNaCl溶于乙醇中制成膠體,其中含有的膠體粒子數目為0.1NA
D. 6molCl2通入足量熱 NaOH 溶液發生反應:3Cl2+6NaOH![]() NaC1O3+5NaCl+3H2O,轉移電子數目為10NA
NaC1O3+5NaCl+3H2O,轉移電子數目為10NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將物質X逐漸加入(或滴入)Y溶液中,其生成沉淀的物質的量與加入X的物質的量關系如圖所示,符合圖示情況的是( )
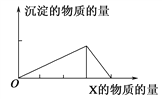
A | B | C | D | |
X | NaOH | HCl | CO2 | AlCl3 |
Y | AlCl3 | NaAlO2 | Ca(OH)2 | NaOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質與水反應生成強堿的是( )
A. NH3 B. Na2O C. CO2 D. NO2
【答案】B
【解析】
A. NH3溶于水生成一水合氨,屬于弱堿,A錯誤;B. Na2O溶于水生成氫氧化鈉,是強堿,B正確;C. CO2溶于水生成碳酸,屬于弱酸,C錯誤;D. NO2溶于水生成硝酸和NO,硝酸是強酸,D錯誤,答案選B。
【題型】單選題
【結束】
19
【題目】利用下列裝置可以完成的實驗組合是
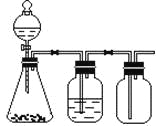
選項 | 制氣裝置 | 洗氣瓶中試劑 | 瓶中氣體 |
A | 氯酸鉀 MnO2 | 濃硫酸 | O2 |
B | 石灰石 稀鹽酸 | NaHCO3溶液 | CO2 |
C | Zn 稀硫酸 | 濃硫酸 | H2 |
D | MnO2 濃鹽酸 | 濃硫酸 | Cl2 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列各組離子在指定溶液中一定能大量共存的是( )
A. 0.1 mol·L-1NaNO3溶液:H+、Fe2+、Cl-、SO42-、K+
B. ![]() =10-13mol·L-1的溶液:Na+、AlO2-、OH-、NO3-
=10-13mol·L-1的溶液:Na+、AlO2-、OH-、NO3-
C. 0.1 mol·L-1NH3·H2O溶液:K+、Na+、NO3-、Cl-
D. 加入鋁粉能產生大量H2的溶液:Na+、K+、Cl-、HCO3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某試液中只可能含有K+、NH4+、Fe2+、Al3+、Cl﹣、SO42﹣、CO32﹣、AlO2﹣ 中的若干種離子,離子濃度均為 0.1molL﹣1.某同學進行了如下實驗:

下列說法正確的是( )
A. 無法確定原試液中是否含有 Al3+、 Cl﹣
B. 濾液 X 中大量存在的陽離子有 NH4+、 Fe2+和 Ba2+
C. 無法確定沉淀 C 的成分
D. 原溶液中存在的離子為 NH4+、 Fe2+、 Cl﹣、 SO42﹣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】無水MgBr2可用作催化劑。實驗室采用鎂屑與液溴為原料制備無水MgBr2,裝置如圖,主要步驟如下:
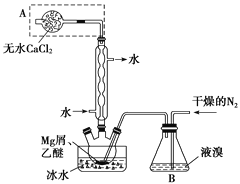
步驟1 三頸瓶中裝入10 g鎂屑和150 mL無水乙醚;裝置B中加入15 mL液溴。
步驟2 緩慢通入干燥的氮氣,直至溴完全導入三頸瓶中。
步驟3 反應完畢后恢復至常溫,過濾,濾液轉移至另一干燥的燒瓶中,冷卻至0 ℃,析出晶體,再過濾得三乙醚合溴化鎂粗品。
步驟4 室溫下用苯溶解粗品,冷卻至0 ℃,析出晶體,過濾,洗滌得三乙醚合溴化鎂,加熱至160 ℃分解得無水MgBr2產品。
已知:
①Mg與Br2反應劇烈放熱;MgBr2具有強吸水性;
②MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5。
MgBr2·3C2H5OC2H5。
請回答:
(1)儀器A的名稱是________。實驗中不能用干燥空氣代替干燥N2,原因是__________。
(2)如將裝置B改為裝置C(如圖),可能會導致的后果是______________________。
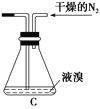
(3)步驟3中,第一次過濾除去的物質是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組利用下圖所列裝置進行“鐵與水蒸氣反應”的實驗,并利用產物進一步制取FeCl36H2O晶體(圖中夾持及尾氣處理裝置均已略去)。請回答下列問題:
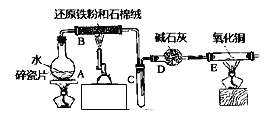
(1)裝置B中發生反應的化學方程式是______________________________.
(2)E中出現的現象是______________________.
(3)該小組把B中反應后的產物加入到足量的鹽酸中,用該溶液制取FeCl36H2O晶體.
①欲檢驗溶液中含有Fe3+,選用的試劑為________________,現象是_______________.
②該實驗小組同學用上述試劑沒有檢測到Fe3+,用離子方程式解釋濾液中不存在Fe3+可能的原因:_______________________.
③將此濾液中FeCl2完全氧化為FeCl3最好選擇下列物質中的_______.
A.酸性KMnO4溶液 B.Cl2 C.Na2O2 D.FeCl3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com