
常溫下,向含2 mol NaClO的稀溶液中通入1 mol CO2二氧化碳,充分反應后,生成1 mol HClO和1 mol NaHCO3,
經檢驗溶液![]() .有關反應后該混合溶液的敘述正確的是
.有關反應后該混合溶液的敘述正確的是
A.上述反應對應的離子方程式為2ClO-+CO2+H2O=2HClO+CO32-
B.上述溶液中:c(ClO-)>c(HCO3-)>c(CO32-)
C.上述溶液中:c(ClO-)+c(HClO)=c(HCO3-)+c(CO32-)+c(H2CO3)
D.上述溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(ClO-)
B
從題干信息可看出,電離H+能力:H2CO3>HClO>HCO3-,離子方程式為ClO-+CO2+H2O=HClO+HCO3-,A選項錯誤;反應后的溶液中含有1 mol NaClO、1mol HClO、1mol NaHCO3,由![]()
得c(H+)=1×10-6 mol·L-1,溶液呈酸性,說明次氯酸電離程度大于次氯酸鈉、碳酸氫鈉水解能力,故有c(ClO-)>c(HCO3-),而HCO3-電離程度很小,則有c(HCO3-)>c(CO32-),B選項正確;氯的物質的量是碳的物質的量2倍,該溶液的物料守恒式有:c(ClO-)+c(HClO)=2c(HCO3-)+2c(CO32-)+2c(H2CO3),C選項錯誤;該溶液的電荷守恒式為c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(ClO-)+2c(CO32-),D選項錯誤。


 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案 名校名師培優作業本加核心試卷系列答案
名校名師培優作業本加核心試卷系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2012-2013學年河南省鄭州市高三第三次測驗預測理綜化學試卷(解析版) 題型:填空題
銅是一種與人類關系非常密切的有色金屬。常溫下,Cu2+在溶液中穩定, Cu+在酸性條件下易發生歧化反應:2Cu+=Cu2++Cu;大多數 +1價銅的化合物是難溶 物,如:Cu20、Cul、CuCl、CuH 等。
(1)在CuCl2溶液中逐滴加入過量KI溶液,可能發生的反應有:
2Cu2++4I-=2CuI↓(白色)+I2; 2Cu2++4I-+2Cl-=CuCl↓(白色)+I2
已知:常溫下Ksp(CuCl)=1.20×10-6(mol/L)2; Ksp(CuI)=5.06×10-12(mol/L)2。 由此推斷上述反應生成主要沉淀物的化學式是______。
(2)向CuH中加入過量稀HC1,有氣體生成,該反應的離子方程式為______。
(3)將 冰 銅(由Cu2S和FeS熔合成含Cu 18%—20%的一種物質)加入熔劑,在髙溫下 吹入空氣,冰銅中的Cu2S被氧化為Cu2O,生 成 的Cu2O與Cu2S反應生成粗銅。上述兩個反應的化學方程式分別是______、______。
(4)常溫下,向0.20 mol • L-1硫酸銅溶液中加入氫氧化鈉溶液,生成淺藍色氫氧化銅 沉淀,當溶液的pH = 6時,c(Cu2+)=______mol.L‑1。[已知:Ksp(CuI)=2.2×10-20(mol/L)3]
(5)將0.80 gCuSO4 • 5H2O樣品加熱分解,其脫水過程中固體質量隨溫度的變化如下圖所示。
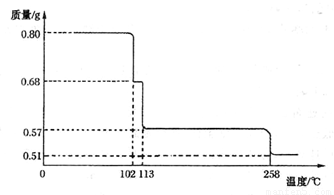
請 確定110°C時固體物質的化學式____________。(要求寫出推斷過程)
查看答案和解析>>
科目:高中化學 來源:遼寧省期末題 題型:推斷題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com