
如圖所示,下列敘述正確的是( ) 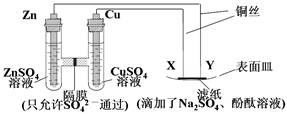
| A.隔膜左側溶液的質量增加,隔膜右側溶液的液面升高 |
| B.ZnSO4溶液與CuSO4溶液可以互換 |
| C.X與濾紙接觸處有氧氣生成 |
| D.Y與濾紙接觸處有氣泡產生,溶液逐漸變紅 |
科目:高中化學 來源: 題型:實驗題
實驗測定酸堿中和滴定曲線是高中化學的重要定量實驗。下表是用0.10 mol/L的鹽酸滴定 0.10 mol/L 20.00 mL NaOH 溶液時獲得的一些相關數據。請回答下列問題:
(1)填寫表中①②對應的 pH (結果保留兩位小數)
(2)下圖是本實驗的滴定曲線圖。請根據該圖,說明強酸溶液滴定強堿溶液時,為什么既可以使用甲基橙作為指示劑,又可以使用酚酞試液作指示劑來指示滴定終點?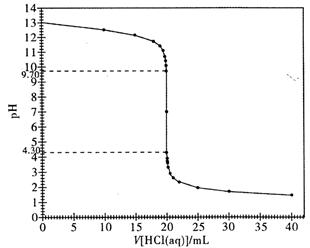
(3)若在滴定終點時俯視讀數,最終測得的氫氧化鈉溶液的濃度會 (填“偏大”、“偏小”或“沒有影響”,下同);若滴定結束時,滴定管尖嘴懸有半滴標準鹽酸,最終測得的氫氧化鈉溶液的濃度會;若盛裝待測液的錐形瓶洗滌干凈后,未干燥即盛裝待測液,最終測得的氫氧化鈉溶液的濃度會 。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
結合下圖判斷,下列敘述正確的是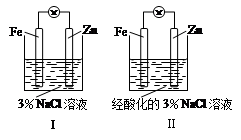
| A.Ⅰ和Ⅱ中正極均被保護 |
| B.Ⅰ和Ⅱ中負極反應均是:Fe-2e-===Fe2+ |
| C.Ⅰ正極反應是:O2 + 2H2O + 4e-===4OH- |
| D.Ⅰ和Ⅱ中分別加入少量KSCN溶液,溶液均變紅 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
原電池的電極名稱不僅與電極材料的性質有關,也與電解質溶液有關,下列說法中不正確的是
| A.由Al、Cu、稀H2SO4組成原電池,放電時SO42-向Al電極移動 |
| B.由Mg、Al、NaOH溶液組成原電池,其負極反應式為:Al-3e-+4OH-===AlO2-+2H2O |
| C.由Fe、Cu、FeCl3溶液組成原電池,其負極反應式為:Cu-2e-===Cu2+ |
| D.由Al、Cu、濃硝酸組成原電池作電源,用石墨電極來電解硝酸銀溶液,當析出1 mol Ag時,消耗銅電極32 g |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
堿性電池具有容量大、放電電流大的特點,因而得到廣泛應用。鋅—錳堿性電池以氫氧化鉀溶液為電解液,電池總反應式為: Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s) ,下列說法錯誤的是( )
| A.電池工作時,鋅失去電子 |
| B.電池正極的電極反應式為:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH—(aq) |
| C.電池工作時,電子由正極通過外電路流向負極 |
| D.外電路中每通過0.2mol電子,鋅的質量理論上減小6.5g |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
如圖所示,a、b是多孔石墨電極,某同學按圖示裝置進行如下實驗: 斷開K2,閉合K1一段時間,觀察到兩支玻璃管內都有氣泡將電極包圍,此時斷開K1,閉合K2,觀察到電流計A的指針有偏轉。下列說法不正確的是
| A.斷開K2,閉合K1一段時間,溶液的pH變大 |
| B.斷開K1,閉合K2時,b極上的電極反應式為:2H++2e-====H2↑ |
| C.斷開K2,閉合K1時,a極上的電極反應式為:4OH--4e-====O2↑+2H2O |
| D.斷開K1,閉合K2時,OH-向b極移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
把鋅片和銅片用導線相連后插入稀硫酸溶液中構成原電池。對該電池的描述合理的是①溶液中硫酸的物質的量濃度保持不變;②Cu極上有氣泡產生,發生還原反應;③Cu為負極,Zn為正極;④原電池在工作時電子由負極通過溶液流向正極;⑤該裝置將化學能轉變為電能( )
| A.④⑤ | B.③⑤ | C.①② | D.②⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
我們生活中離不開各種各樣的電池,下列關于電池的說法錯誤的是( )
| A.用后不能再生的電池稱為一次電池,如鋅錳干電池(電解質溶液中含氯化銨等) |
| B.放電后通過充電可反復使用的電池稱為二次電池,如鎳鎘電池、鉛蓄電池等 |
| C.手機、電腦、數碼相機中的可充電電池使用壽命長,對環境無害,不用進行回收 |
| D.目前我國生產的無汞干電池,對環境和人體健康沒有明顯危害,可以不進行特殊處理,和普通垃圾混放 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com