
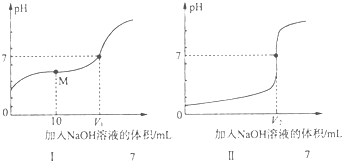
 室溫下,用0.10mol•L-1鹽酸分別滴定20.00mL 0.10mol•L-1氫氧化鈉溶液和氨水,滴定過程中溶液pH隨加入鹽酸體積[V(HCl)]的變化關系如圖所示.下列說法不正確的是( )
室溫下,用0.10mol•L-1鹽酸分別滴定20.00mL 0.10mol•L-1氫氧化鈉溶液和氨水,滴定過程中溶液pH隨加入鹽酸體積[V(HCl)]的變化關系如圖所示.下列說法不正確的是( )| A. | Ⅱ表示的是滴定氨水的曲線,當V(HCI)=20 mL時,有:c(Cl-)>c(N${{H}_{4}}^{+}$)>c(H+)>c(OH-) | |
| B. | 當pH=7時,滴定氨水消耗的V(HCl)=20 mL,且c(N${{H}_{4}}^{+}$)=c(Cl-) | |
| C. | 滴定氫氧化鈉溶液時,若V(HCl)>20 mL,則一定有:c(Cl-)>c(Na+)>c(H+)>c(OH-) | |
| D. | 當滴定氨水消耗V(HCl)=10 mL時,有:2[c(OH-)-c(H+)]=c(N${{H}_{4}}^{+}$)-c(NH3•H2O) |
分析 A.根據氨水和NaOH在滴定開始時的pH來判斷;
B.鹽酸與氨水恰好反應生成氯化銨,溶液顯酸性;
C.滴定氫氧化鈉溶液時,若V(HCl)>20 mL,氫離子濃度可能大于鈉離子;
D.當滴定氨水消耗V(HCl)=10 mL時,溶液中溶質為等物質的量的NH3•H2O和NH4Cl.
解答 解:A.一水合氨是弱堿,在溶液中部分電離,則開始時氨水的pH小于13,所以Ⅱ表示的是滴定氨水的曲線,當V(HCl)=20 mL時,恰好反應生成氯化銨,溶液顯酸性,則c(Cl-)>c(NH4+)>c(H+)>c(OH-),故A正確;
B.滴定氨水消耗的V(HCl)=20 mL,鹽酸與氨水恰好反應生成氯化銨,溶液顯酸性,當pH=7時,滴定氨水消耗的V(HCl)<20 mL,故B錯誤;
C.滴定氫氧化鈉溶液時,若V(HCl)>20 mL,氫離子濃度可能大于鈉離子,則溶液中離子濃度關系可能為:c(Cl-)>c(H+)>c(Na+)>c(OH-),故C錯誤;
D.當滴定氨水消耗V(HCl)=10 mL時,溶液中溶質為等物質的量的NH3•H2O和NH4Cl,電荷守恒為c(Cl-)+c(OH-)=c(NH4+)+c(H+),物料守恒為:2c(Cl-)=c(NH3•H2O)+c(NH4+),則2[c(OH-)-c(H+)]=c(NH4+)-c(NH3•H2O),故D正確.
故選BC.
點評 本題考查酸堿混合的定性判斷和計算,題目難度中等,本題注意把握弱電解質的電離特點以及電荷守恒、物料守恒的應用.


科目:高中化學 來源: 題型:解答題

| 離子 | 開始沉淀時的pH | 完全沉淀時的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
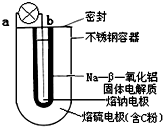 鈉-硫($\frac{Na}{{S}_{8}}$)電池是由固體電解質將兩個液體電極隔開(如圖),一個由鈉-β-氧化鋁固體電解質做成的中心管,將內室的熔融鈉(熔點98℃)和外室的熔融硫(熔點119℃)隔開,并允許Na+通過.下列有關說法錯誤的是( )
鈉-硫($\frac{Na}{{S}_{8}}$)電池是由固體電解質將兩個液體電極隔開(如圖),一個由鈉-β-氧化鋁固體電解質做成的中心管,將內室的熔融鈉(熔點98℃)和外室的熔融硫(熔點119℃)隔開,并允許Na+通過.下列有關說法錯誤的是( )| A. | 放電時b為電池的負極 | |
| B. | 充電時陰極反應式為:Na++e-=Na | |
| C. | 充電時,陽極處發生還原反應 | |
| D. | 放電時Na+可以穿過固體電解質流向a電極 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 常溫下0.1 mol•L-1的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,c(N${{H}_{4}}^{+}$)由大到小的順序為②>①>③ | |
| B. | 常溫下0.4 mol•L-1CH3COOH溶液和0.2 mol•L-1 NaOH溶液等體積混合后溶液顯酸性,則溶液中粒子濃度由大到小的順序為c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液與0.2 mol•L-1 NaHCO3溶液等體積混合所得溶液中:c(C${{O}_{3}}^{2-}$)+2c(OH-)=c(HC${{O}_{3}}^{-}$)+3c(H2CO3)+2c(H+) | |
| D. | 0.1 mol•L-1的氨水與0.05 mol•L-1 H2C2O4溶液等體積混合所得溶液中:c(N${{H}_{4}}^{+}$)+c(NH3•H2O)=2c(C2${{O}_{4}}^{2-}$)+2c(HC2${{O}_{4}}^{-}$)+2c(H2C2O4) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑的大小順序:r(W)>r(Z)>r(Y) | |
| B. | 元素Z、M的簡單離子的電子層結構相同 | |
| C. | W的簡單氣態氫化物的熱穩定性比M的差 | |
| D. | 元素X和Y形成的化合物只有一種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 操作步驟 | 現象 |
| 步驟1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1KSCN溶液,靜置. | 出現白色沉淀. |
| 步驟2:取1mL上層清液于試管中,滴加1滴2mol•L-1 Fe(NO3)3溶液. | 溶液變紅色. |
| 步驟3:向步驟2的溶液中,繼續加入5滴3mol•L-1AgNO3溶液. | 出現白色沉淀,溶液紅色變淺. |
| 步驟4:向步驟1余下的濁液中加入5滴3mol•L-1KI溶液. | 出現黃色沉淀. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗操作 | 現象 | 實驗結論 | |
| ① | 將某氣體通入品紅溶液中 | 品紅溶液褪色 | 該氣體一定是SO2 |
| ② | 將無色氣體通入溴水中 | 溴水的黃色褪去 | 該氣體可能是乙烯 |
| ③ | 向某溶液中滴入兩滴KSCN溶液 | 溶液不顯紅色 | 該溶液一定含有Fe2+ |
| 另取該溶液少許,先滴入氯水,再 滴入KSCN溶液 | 溶液為紅色 | ||
| ④ | 向某溶液中加入鹽酸酸化的氯化鋇 溶液 | 有白色沉淀產生 | 該溶液中可能含有SO42- |
| ⑤ | 將木炭和濃硫酸反應生成的氣體通入 澄清石灰水中 | 有白色沉淀生成 | 該氣體一定是CO2 |
| A. | ②④ | B. | ②③④ | C. | ①③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將Ca(ClO)2、Na2SO3、FeCl3溶液蒸干可得到原溶質 | |
| B. | 因Cl2的氧化性強于I2的氧化性,所以置換反應I2+2NaClO3═2NaIO3+Cl2不能發生 | |
| C. | 在新制氯水中各微粒濃度的關系為:2c(Cl2)=c(ClO?)+c(Cl?)+c(HClO) | |
| D. | 用1L 0.2 mol•L-1NaOH溶液分別吸收0.1molSO2、0.1mol CO2,所得的兩種溶液中酸根離子濃度大小關系是:c(SO32- )>c(CO32-)>c(HCO3-)>c(HSO3-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com