
下列事實不能用電化學原理解釋的是
A. 可將地下輸油鋼管與外加直流電源的負極相連以保護鋼管不受腐蝕
B. 常溫條件下,鋁在空氣中不易被腐蝕
C. 鍍層破壞后,白鐵(鍍鋅的鐵)比馬口鐵(鍍錫的鐵)更耐腐蝕
D. 用鋅與稀硫酸刮氫氣時,往稀硫酸中滴少量硫酸銅溶液能加快反應速率
科目:高中化學 來源:2017屆河南省安陽市高三第二次模擬考試理綜化學試卷(解析版) 題型:選擇題
化學與生活、科技關系密切。下列說法正確的是
A. 液氨可用作制冷劑是因為其氣化時可放出大量的熱
B. 將青蒿在乙醚中浸取,通過分餾可提取治療瘧疾的青蒿素
C. 鋼制品、鋁制品在日常生活中被廣泛應用是因為鐵、鋁為活潑金屬
D. 久置的漂白粉變質是因為漂白粉與空氣中的O2反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省高一下學期第一次月考化學試卷(解析版) 題型:簡答題
實驗室需配制4.6 mol·L-1的H2SO4溶液0.5 L。
⑴ 需要濃度為18.4 mol·L-1的濃硫酸_______________ mL;
⑵ 需要用的玻璃儀器除玻璃棒、量筒外還有___________________________;
⑶ 配制過程中下列操作導致溶液濃度偏高的是____________________。
( A)移液時未充分洗滌燒杯和玻棒
( B)移液時未用玻棒引流而使少量液體外溢
( C)定容俯視刻度線
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省邯鄲市高二上學期期末考試化學試卷(解析版) 題型:實驗題
已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
某化學小組根據上述反應原理進行下列實驗:
Ⅰ.測定H2C2O4溶液的物質的量濃度
實驗步驟如下:
①取待測H2C2O4溶液25.00mL放入錐形瓶中,再加入適量的稀硫酸;
②用0.1mol·L-1KMnO4溶液滴定至終點,記錄數據;
③重復滴定2次,平均消耗KMnO4溶液20.00mL。
請回答:
(1)滴定時,將KMnO4溶液裝在________(填“酸式”或“堿式”)滴定管中。
(2)若在步驟①操作之前,先用待測H2C2O4溶液潤洗錐形瓶,則測得H2C2O4溶液的濃度會________(填“偏大”“偏小”或“無影響”)。
(3)步驟②中到達滴定終點時的現象為________。
(4)計算H2C2O4溶液的物質的量濃度為________mol·L-1。
Ⅱ.探究反應物濃度對化學反應速率的影響設計如下實驗方案(實驗溫度均為25℃):
實驗序號 | 體積V/mL | |||
0.1mol·L-1KMnO4溶液 | 0.1mol·L-1H2C2 O4溶液 | 0.1mol·L-1H2SO4溶液 | H2O | |
① | 2.0 | 5.0 | 6.0 | 7.0 |
② | 2.0 | 8.0 | 6.0 | V1 |
③ | 2.0 | V2 | 6.0 | 2.0 |
請回答:
(5)表中V1=________,V2=________。
(6)實驗中需要測量的數據是________。
(7)實驗中________(填“能”或“不能”)用0.2mol·L-1鹽酸代替0.1mol·L-1H2SO4溶液,理由是________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省邯鄲市高二上學期期末考試化學試卷(解析版) 題型:選擇題
已知室溫下,0.1mol·L-1的NaHSO3溶液的pH=4。該溶液中各粒子的濃度關系正確的是
A. C(Na+)>c(HSO3-)>C(H+)>c(OH-)
B. c(H2SO3)>c(SO32-)
C. c(H+)+C(Na+)=c(OH-)+c(SO32-)+c(HSO3-)
D. c(Na+)=C(HSO3-)+c(H2SO3)+2c(SO32-)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省邯鄲市高二上學期期末考試化學試卷(解析版) 題型:選擇題
對下列現象或事實的解釋正確的是
選項 | 現象或事實 | 解釋 |
A | 用熱的純堿溶液洗去油污 | Na2CO3可直接與油污反應 |
B | 漂白粉在空氣中久置變質 | 漂白粉中的CaCl2與空氣中的CO2反應生成CaCO3 |
C | 向Mg(OH)2懸濁液中滴加CuSO4溶液,生成藍色沉淀 | Cu(OH)2的溶度積比Mg(OH)2的小,Mg(OH)2轉化為Cu(OH)2 |
D | 施肥時,草木灰(有效成分為K2CO3)不能與NH4Cl混合使用 | K2CO3與NH4Cl反應會損失鉀肥 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省邯鄲市高二上學期期末考試化學試卷(解析版) 題型:選擇題
化學與人類生產、生活密切相關。下列說法正確的是
A. 減少CO2的排放,可以減少酸雨的產生
B. 減少SO2的排放,可以從根本上消除霧霾
C. 用電鍍廠的廢水直接灌溉農田,可提高水的利用率
D. 用CO2合成聚碳酸酯可降解塑料,可以實現“碳”的循環利用
查看答案和解析>>
科目:高中化學 來源:2017屆河南省濮陽市高三第一次模擬考試理綜化學試卷(解析版) 題型:實驗題
某研究性學習小組的同學通過查閱資料得到如下信息:草酸晶體(H2C2O4·2H2O)無色,熔點為101℃,受熱脫水、升華,易溶于水,170℃以上分解可得到CO、CO2、H2O,H2C2O4難溶于水。他們欲利用如下裝置驗證上述產物(加熱儀器、夾持儀器省略)。
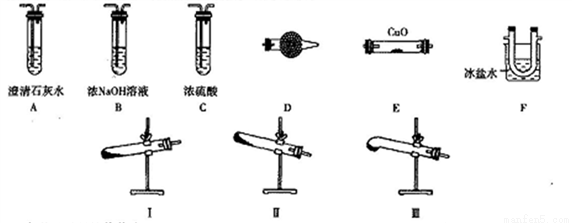
(1)加熱草酸晶體使其分解的裝置是________(從I、II、III中選取),驗證其分解產物的裝置依次是______→A→尾氣處理裝置(用裝置字母作答,裝置可重復使用)。
(2)D中試劑是_________,證明有CO生成的現象是_______。
(3)實驗中有兩處需要加熱,加熱的順序是_________,寫出一種處理尾氣的方法:_____________。
(4)若上述實驗均產生了預期的現象,寫出草酸分解的化學方程式:_________________。
(5)設計一種方案證明草酸是弱酸_________。
查看答案和解析>>
科目:高中化學 來源:2017屆海南省瓊海市高三下學期第一次月考化學試卷(解析版) 題型:填空題
鎂化合物具有廣泛用途。請回答有關鎂的下列問題:
(1)單質鎂在空氣中燃燒的主要產物是白色的____,還生成少量的______(填化學式);
(2)CH3MgCl是一種重要的有機合成試劑,其中鎂的化合價是___________,該化合物水解的化學方程式為____________;
(3)下圖是金屬鎂和鹵素反應的能量變化圖(反應物和產物均為298K時的穩定狀態)。
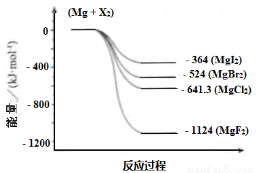
下列選項中正確的是_____________(填序號)。
① MgI2中Mg2+ 與I- 間的作用力小于MgF2中Mg2+ 與F- 間的作用力
② Mg與F2的反應是吸熱反應
③ MgBr2與Cl2 反應的△H > 0
④ 化合物的熱穩定性順序為MgI2 < MgBr2 < MgCl2 < MgF2
⑤ MgF2(s) + Br2(l) = MgBr2(s) + F2(g) △H = +600 kJ · mol-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com