
分析 (1)根據稱量、溶解、配制一定物質的量濃度的溶液、準確量取溶液等操作確定所需儀器;
(2)根據氯水能將FeCl2氧化生成FeCl3;
(3)根據溶液中含有氨水、氯化銨來確定離子;根據洗滌沉淀的方法;
(4)因為沉淀中含有Cl-,據此檢驗沉淀是否洗滌干凈;
(5)氫氧化鐵加熱灼燒后生成氧化鐵,坩堝質量是W1,坩堝與加熱后固體總質量是W2,則氧化鐵的質量為(W2-W1)g.氧化鐵中鐵元素的質量等于樣品中鐵元素的質量,進而計算鐵元素的質量分數;
(6)根據FeCl3、FeCl2溶液中加入過量氨水,生成Fe(OH)3和Fe(OH)2沉淀,在操作過程中Fe(OH)2會被空氣進一步氧化生成Fe(OH)3,最后所得生成物只有Fe2O3.
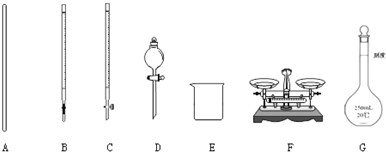
解答 解:(1)稱量時需要天平、鑰匙;溶解時需要燒杯、玻璃棒;配制一定物質的量濃度的溶液時需要量筒、燒杯、玻璃棒、膠頭滴管、一定規格的容量瓶;
準確量取溶液需要酸式滴定管、洗耳球,
故答案為:A、C、F、G;
(2)氯水能將FeCl2氧化生成FeCl3,離子方程式為:2Fe2++Cl2=2Fe3++2Cl-,故答案為:2Fe2++Cl2=2Fe3++2Cl-;
(3)溶液中含有氨水、氯化銨,所以離子有:NH4+、Cl-、OH-;洗滌沉淀的方法是向漏斗里注入蒸餾水,使水面沒過濾渣,等水自然流完后,重復操作2~3次,
故答案為:NH4+、Cl-、OH-;向漏斗里注入蒸餾水,使水面沒過濾渣,等水自然流完后,重復操作2~3次;
(4)因為沉淀中含有Cl-,確定沉淀是否洗滌干凈的操作是:取最后一滴洗滌液,加入硝酸銀溶液,如果沒有沉淀生成,則證明洗滌干凈,
故答案為:取最后一滴洗滌液,加入硝酸銀溶液,如果沒有沉淀生成,則證明洗滌干凈;
(5)鐵元素質量守恒,即紅棕色固體中的鐵就是樣品中鐵,Fe2O3中鐵元素的質量為(W2-W1)g×$\frac{112}{160}$,樣品中鐵元素的質量(W2-W1)g×$\frac{112}{160}$×$\frac{250}{25}$,樣品中鐵元素的質量分數$\frac{({W}_{2}-{W}_{1})g×\frac{112}{160}×\frac{250}{25}}{ag}$×100%,
故答案為:$\frac{({W}_{2}-{W}_{1})g×\frac{112}{160}×\frac{250}{25}}{ag}$×100%.
(6)因FeCl3、FeCl2溶液中加入過量氨水,生成Fe(OH)3和Fe(OH)2沉淀,在操作過程中Fe(OH)2會被空氣進一步氧化生成Fe(OH)3,最后所得生成物只有Fe2O3,仍可達到實驗目的,故甲同學的觀點正確,
故答案為:正確;FeCl3、FeCl2溶液中加入過量氨水,生成Fe(OH)3和Fe(OH)2沉淀,在操作過程中Fe(OH)2會被空氣進一步氧化生成Fe(OH)3,最后所得生成物只有Fe2O3,對實驗結果無影響,故甲同學的觀點正確.
點評 本題主要考查學生溶液的配制、對實驗原理理解、對實驗操作的評價、物質含量的測定、化學計算等,題目難度中等,需要學生具備扎實的基礎知識與分析問題、解決問題能力.


科目:高中化學 來源: 題型:選擇題

| A. | X與Y組成的兩種化合物中陰、陽離子的個數比均為1:2 | |
| B. | W、R兩種元素對應的簡單離子都能影響水的電離平衡 | |
| C. | 由X、Y、Z三種元素組成的化合物,其水溶液顯堿性 | |
| D. | 工業上用電解熔融的Z和X組成的化合物來制取Z的單質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH4+Cl2 $\stackrel{光照}{→}$CH2Cl2+H2 | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化劑}$2CH3CHO+H2O | |
| C. | CH3CH2OH+CH3COOH $\stackrel{濃硫酸}{→}$CH3COOCH2CH3 | |
| D. | H2C═CH2+Br2→CH3CHBr2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AgCl沉淀的生成和溶解不斷進行,但速率相等 | |
| B. | AgCl難溶于水,溶液中沒有Ag +和Cl - | |
| C. | 升高溫度,AgCl的溶解度不變 | |
| D. | 向AgCl沉淀的溶解平衡體系中加入NaCl固體,AgCl的溶解度不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
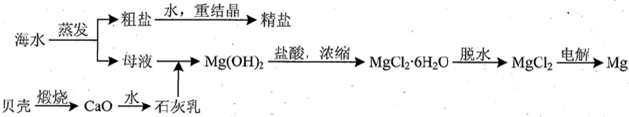
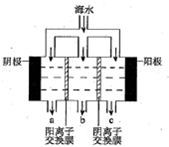 海水中主要離子的含量如下:
海水中主要離子的含量如下:| 成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 氧化還原反應在生產、生活中具有廣泛的用途,貫穿古今.
氧化還原反應在生產、生活中具有廣泛的用途,貫穿古今.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
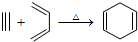 ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )| A. | 2-甲基-1,3-丁二烯和2-丁炔 | B. | 1,3-戊二烯和2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯和乙炔 | D. | 2,3-二甲基-1,3-丁二烯和1-丁炔 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

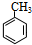 ;
;查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com