
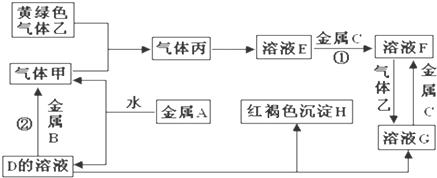
分析 金屬A焰色反應為黃色,故A為金屬Na,與水反應生成NaOH與氫氣,則D為NaOH,氣體甲為H2;NaOH與金屬B反應生成氫氣,故金屬B為Al.黃綠色氣體乙為Cl2,與H2反應生成丙為HCl,HCl溶于水得物質E為鹽酸;NaOH與物質G反應生成紅褐色沉淀H是Fe(OH)3,故物質G中含有Fe3+,由轉化關系HCl生成F、F生成G知,可知金屬C為Fe,物質F為FeCl2,物質G為FeCl3,據此分析解答.
解答 解:金屬A焰色反應為黃色,故A為金屬Na,與水反應生成NaOH與氫氣,則D為NaOH,氣體甲為H2;NaOH與金屬B反應生成氫氣,故金屬B為Al.黃綠色氣體乙為Cl2,與H2反應生成丙為HCl,HCl溶于水得物質E為鹽酸;NaOH與物質G反應生成紅褐色沉淀H是Fe(OH)3,故物質G中含有Fe3+,由轉化關系HCl生成F、F生成G知,可知金屬C為Fe,物質F為FeCl2,物質G為FeCl3,
(1)通過以上分析知,A、H、G、乙分別為Na、Fe(OH)3、FeCl3、Cl2,
故答案為:Na;Fe(OH)3;FeCl3;Cl2;
(2)反應①是Fe與鹽酸反應生成氯化亞鐵與氫氣,反應方程式為:Fe+2HCl═FeCl2+H2↑;
反應②是Al與NaOH溶液反應生成偏鋁酸鈉與氫氣,反應方程式為:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
故答案為:Fe+2HCl═FeCl2+H2↑;2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(3)氯化亞鐵和氯氣反應生成氯化鐵,該反應離子方程式為2Fe 2++Cl2=2Fe 3++2Cl-,
故答案為:2Fe 2++Cl2=2Fe 3++2Cl-.
點評 本題以鈉、鋁和鐵為載體考查無機物推斷,為高頻考點,明確物質性質及物質之間轉化是解本題關鍵,以物質特殊顏色為突破口進行推斷,需要學生熟練掌握元素化合物知識,題目難度不大.


 捷徑訓練檢測卷系列答案
捷徑訓練檢測卷系列答案 小夫子全能檢測系列答案
小夫子全能檢測系列答案科目:高中化學 來源: 題型:解答題
| 元素代號 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | Al14和稀鹽酸反應的化學方程式可表示為Al14+2HCl→Al14Cl2+H2↑ | |
| B. | Al13超原子中Al原子間是通過共價鍵結合的 | |
| C. | Al14、Al13性質與Al相似,都具有較強的還原性 | |
| D. | Al13和Al14互為同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
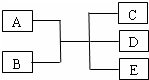 已知A、B、C、D、E是化學中常見的物質,常溫下,E是一種無色無味的液體,它們之間有如下反應關系.
已知A、B、C、D、E是化學中常見的物質,常溫下,E是一種無色無味的液體,它們之間有如下反應關系.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 150mL 1mol•L-1NaCl溶液 | B. | 75mL 1mol•L-1 CaCl2溶液 | ||
| C. | 150mL 1mol•L-1 KCl溶液 | D. | 75mL 1mol•L-1 AlCl3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 生成物都屬于電解質 | |
| B. | HCl全部發生氧化反應 | |
| C. | 該反應表明氧化性KClO3比Cl2強 | |
| D. | 1 mol KClO3在反應中得到6 mol e- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 在測定中和反應的反應熱實驗中,只要讀一次溫度 | |
| B. | 可用pH試紙測定新制氯水的pH | |
| C. | 中和滴定實驗中,洗凈后的錐形瓶不需要干燥 | |
| D. | 向CH3COONa溶液中滴入石蕊試液,溶液變藍 | |
| E. | 向白色ZnS沉淀上滴加CuSO4溶液,沉淀變為黑色,說明Ksp(ZnS)<Ksp(CuS) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com