
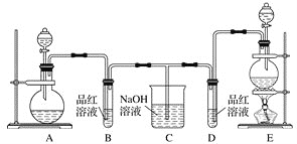
【題目】某化學小組為了證明二氧化硫和氯氣的漂白性,設計了如下圖所示的實驗裝置:
他們制備二氧化硫和氯氣所依據的原理分別是:
Na2SO3+H2SO4===Na2SO4+H2O+SO2↑
MnO2+4HCl(濃)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用來制取氯氣的裝置是________(填字母),反應中濃鹽酸所表現出的化學性質是________________和________________。
(2)反應開始一段時間后,B、D試管中的品紅溶液均褪色。停止通氣后,再給B、D兩個試管分別加熱,__________(填“B”或“D”)試管中無明顯現象。
(3)裝置C的作用是____________________。
(4)若裝置D中的品紅溶液換成紫色的石蕊溶液,則出現的現象是__________________。
(5)該小組同學將兩種氣體混合后通入品紅溶液,一段時間后,品紅溶液幾乎不褪色。查閱資料得知:兩種氣體按體積比1∶1混合,再與水反應可生成兩種常見的酸,因而失去漂白作用,該反應的化學方程式是____________________________。
【答案】E 還原性 酸性 D 吸收多余的二氧化硫和氯氣 先變紅,后褪色 SO2+Cl2+2H2O===2HCl+H2SO4
【解析】
(1)根據反應物的狀態和反應條件選擇反應裝置,根據氯元素的化合價變化和生成物分析濃鹽酸的性質;
(2)根據二氧化硫和次氯酸的漂白原理分析;
(3)根據二氧化硫和氯氣均是大氣污染物分析;
(4)根據氯水的性質分析;
(5)根據氯氣能和二氧化硫在溶液中反應生成鹽酸和硫酸解答。
(1)根據題給信息知,實驗室制取氯氣所用藥品是固體和液體,反應條件是加熱,所以應選用固液加熱型裝置,選E;實驗室制取氯氣的反應方程式為:MnO2+4HCl(濃)![]() MnCl2+Cl2↑+2H2O,由HCl生成MnCl2,氯元素化合價不變,由HCl生成Cl2,氯元素化合價降低,所以濃鹽酸所表現出的性質是酸性和還原性;
MnCl2+Cl2↑+2H2O,由HCl生成MnCl2,氯元素化合價不變,由HCl生成Cl2,氯元素化合價降低,所以濃鹽酸所表現出的性質是酸性和還原性;
(2)氯氣通入品紅溶液中紅色褪去,是利用次氯酸的強氧化性,生成的無色物質穩定,加熱不復原;二氧化硫的漂白性是利用二氧化硫和有色物質化合生成無色物質,生成的無色物質不穩定,加熱復原,因此D試管中無明顯現象;
(3)氯氣和二氧化硫均有毒不能直接排放到空氣中,需進行尾氣處理,裝置C的作用是吸收多余的SO2和Cl2防止污染環境;
(4)氯氣溶于水生成鹽酸和次氯酸,氯水顯酸性和強氧化性,因此若裝置D中的品紅溶液換成紫色的石蕊溶液,則出現的現象是先變紅,后褪色;
(5)氯氣有強氧化性,二氧化硫有還原性,二者能按1:1發生氧化還原反應生成鹽酸和硫酸而使氣體失去漂白性,反應方程式為Cl2+SO2+2H2O=H2SO4+2HCl。


科目:高中化學 來源: 題型:
【題目】C、N、O、Na、Mg、Al、S、Cl是常見的八種元素,根據元素及其化合物性質,回答下列問題:
(1)S在周期表中的位置為______;CO2的電子式是_______。
(2)比較O、Na元素常見離子的半徑大小(用化學式表示,下同)____>____;__________比較S、Cl元素的最高價氧化物對應水化物的酸性強弱:____>____ 。_______________
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
類型 | 離子化合物 | 離子化合物 | 離子化合物 | 共價化合物 |
熔點/℃ | 2800 | 2050 | 714 | 191 |
工業制鎂時,電解MgCl2而不電解MgO的原因是___________;制鋁時,電解Al2O3而不電解AlCl3的原因是___________ 。
(4)碳與鎂形成的1mol化合物Q與水反應,生成2molMg(OH)2和1mol烴,該烴分子中碳氫質量比為9:1,烴的結構簡式為______;Q的化學式為_______ 。
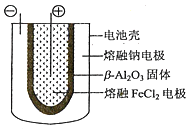
(5)熔融狀態下,鈉和FeCl2能組成可充電電池(裝置示意圖如下),反應原理為:2Na+FeCl2![]() Fe+2NaCl.放電時,電池的正極反應式為___________;充電時,_______(寫物質名稱)電極接電源的負極;該電池的電解質為_______。
Fe+2NaCl.放電時,電池的正極反應式為___________;充電時,_______(寫物質名稱)電極接電源的負極;該電池的電解質為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀鹽酸,CO2的生成量與加入鹽酸的體積(V)的關系如圖所示。下列判斷正確的是( )

A. 在0-a范圍內,只發生中和反應
B. ab段發生反應的離子方程式為:CO32-+2H+=H2O+CO2↑
C. a=0.3
D. 原混合溶液中NaOH與Na2CO3的物質的量之比為1:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定質量的鎂和鋁分別與等濃度、等體積的過量稀硫酸反應,產生氣體的體積(V)與時間(t)關系如右圖。下列關于反應的說法錯誤的是
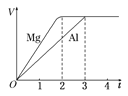
A.鎂和鋁的物質的量之比為3∶2
B.鎂和鋁轉移電子數之比為1∶1
C.鎂和鋁的摩爾質量之比為8∶9
D.鎂和鋁反應所用時間之比為3∶2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室里需要純凈的NaCl溶液,但手邊只有混有Na2SO4、NaHCO3的NaCl。某學生設計了如圖所示方案提取純凈的NaCl溶液。
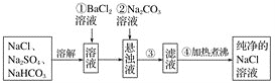
如果此方案正確,那么:
(1)操作①為什么不用硝酸鋇溶液,其理由是___________________________________。
(2)進行操作①后,如何判斷SO![]() 已除盡,方法是___________________________。
已除盡,方法是___________________________。
(3)操作②的目的是________,為什么不先過濾后加碳酸鈉溶液?理由是________________________________________________________________________。
(4)操作③用到的玻璃儀器除燒杯、玻璃棒外,還需要____________________。
(5)操作④的目的是______________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實不能用勒夏特列原理解釋的是
A. 加壓有利于SO2與O2反應生成SO3 B. 500度左右比常溫下更有利于合成氨
C. 將氨氣液化,有利于合成氨的反應 D. 用過量空氣煅燒硫鐵礦可以提高原料利用率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】大氣中CO2含量的增加會加劇溫室效應,秉承“低碳環保,綠色出行”的生活理念,CO2的綜合利用也成為熱門研究領域。
I.CO2可用于生產乙烯。
(1)依據圖1寫出CO2和H2生成C2H4和H2O(l)的熱化學方程式________。
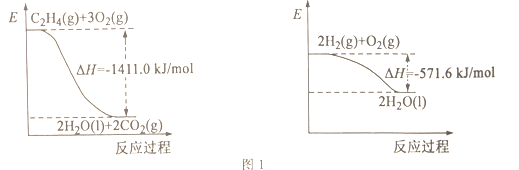
(2)以稀硫酸作電解質溶液,利用電解法將CO2轉化為乙烯的裝置如圖2所示。M電極的電極反應式為_____,工作一段時間后,陽極室中溶液的pH_____(填“增大”“不變”或“減小”)。
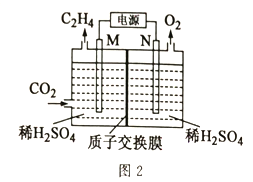
Ⅱ.CO2與H2在一定條件下可生產二甲醚:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)Δ H<0
CH3OCH3(g)+3H2O(g)Δ H<0
(3)在2.0L恒容密閉容器中,加入2.0molCO2和6.0molH2,恒溫條件下經過5min達到平衡狀態,此時的壓強是起始壓強的2/3
①0~5min內反應的平均速率v(H2)=____,此溫度下的平衡常數K=______.
②平衡常數K(800K)______K(900K)(填“>”“=”或“<”)
(4)分別以Cat.1和Cat.2作催化劑發生該反應,反應進行相同的時間后,測得CO2的轉化率a(CO2)隨反應溫度T的變化情況如圖3所示(忽略溫度對催化劑活性的影響)。
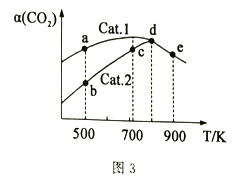
①該反應的活化能Ea(Cat.1)________Ea(Cat.2)(填“>”或“<”)。
②a、b、c、d、e五個狀態中一定是平衡狀態的是_______(填字母)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素W、X、Y、Z,原子半徑依次增大。W、X在同一主族,Y元素在第三周期中離子半徑最小,Y和Z的原子序數之和是W的3倍。下列說法正確的是
A. X的簡單氫化物的熱穩定性比W的強 B. X的氧化物對應的水化物是強酸
C. Z和W形成的化合物可能含有非極性鍵 D. Z、Y的氧化物是常用的耐火材料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈦及其化合物在化工、醫藥、材料等領域有著廣泛的應用。
(1)基態鈦原子的價電子排布式為_____________,與鈦同周期的元素中,基態原子的未成對電子數與鈦相同的有____________種。
(2)鈦比鋼輕、比鋁硬,是一種新興的結構材料,鈦的硬度比鋁大的原因是_________。
(3)在濃的TiCl3的鹽酸溶液中加入乙醚,并通入HCl至飽和,可得到配位數為6、組成為TiCl3·6H2O的綠色晶體,該晶體中兩種配體的物質的量之比為1:5,則該配合離子的化學式為___________。
(4)半夾心結構催化劑M能催化乙烯、丙烯、苯乙烯的聚合,其結構如下圖所示。
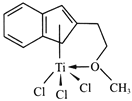
①組成M的元素中,電負性最大的是_________(填名稱)。
②M中碳原子的雜化方式為____________。
③M中不含________(填代號)。
a.π鍵 b.σ鍵 c.離子鍵 d.配位鍵
(5)金紅石(TiO2)是含鈦的主要礦物之一。其晶胞結構(晶胞中相同位置的原子相同)如圖所示。

①A、B、C、D 4種微粒,其中氧原子是________(填代號)。
②若A、B、C的原子坐標分別為A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),則D的原子坐標為D(0.19a,____,___);鈦氧鍵的鍵長d=______(用代數式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com