
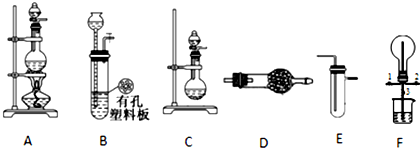
分析 (1)C裝置是不需要加熱制備氨氣的裝置,利用濃氨水滴入生石灰產生氨氣,與制取干燥氨氣可以用堿石灰干燥氨氣;
(2)二氧化錳和濃鹽酸加熱反應制備氯氣,濃鹽酸易揮發,所以生成的氯氣中含有氯化氫和水蒸氣,通過飽和食鹽水除去氯化氫,通過濃硫酸除去水蒸氣;
(3)實驗時打開開關1、3,關閉2向燒瓶中通入氯氣,然后關閉1、3,打開2,向燒瓶中緩慢通入一定量的氨氣,實驗一段時間后燒瓶內出現濃厚的白煙并在容器內壁凝結,反應生成氯化銨,可根據銨根離子與堿反應生成氨氣的方法檢驗;
(4)氯氣的氧化性強于溴,可根據溴水的顏色判斷;
(5)乙烯和溴水發生加成反應生成1,2-二溴乙烷;
(6)二氧化硫和硫化氫發生氧化還原反應生成硫,二氧化硫和硫化氫都可與堿液反應,防止污染空氣.
解答 解:(1)C裝置是不需要加熱制備氨氣的裝置,利用濃氨水滴入生石灰產生氨氣,制取干燥氨氣可以用堿石灰干燥氨氣;為制取干燥氨氣,可將裝置C連接D點的干燥的氨氣,裝置C中的燒瓶內固體宜選用濃氨水和生石灰或堿石灰,
故答案為:D;ad;
(2)二氧化錳和濃鹽酸加熱反應制備氯氣,濃鹽酸易揮發,所以生成的氯氣中含有氯化氫和水蒸氣,通過飽和食鹽水除去氯化氫,通過濃硫酸除去水蒸氣,
故答案為:飽和食鹽水、濃硫酸;
(3)實驗時打開開關1、3,關閉2向燒瓶中通入氯氣,然后關閉1、3,打開2,向燒瓶中緩慢通入一定量的氨氣,實驗一段時間后燒瓶內出現濃厚的白煙并在容器內壁凝結,依據反應化學方程式判斷是生成的氯化氫和氨氣反應生成的氯化銨,檢驗銨根離子,可取少量固體于試管中,加入適量濃NaOH溶液并加熱,在管口用濕潤的紅色石蕊試紙檢驗產生的氣體,若濕潤的紅色石蕊試紙變藍,[或用蘸有濃鹽酸(或濃硝酸)的玻璃棒放在試管口,若有白煙生成],證明固體中有NH4+,
故答案為:氯氣;取少量固體于試管中,加入適量濃NaOH溶液并加熱,在管口用濕潤的紅色石蕊試紙檢驗產生的氣體,若濕潤的紅色石蕊試紙變藍,[或用蘸有濃鹽酸(或濃硝酸)的玻璃棒放在試管口,若有白煙生成],證明固體中有NH4+;
(4)氯氣氧化性強于溴,能夠與溴離子發生氧化還原反應置換出溴,溴單質溶液水呈橙紅色,故答案為:裝置E中的NaBr溶液變橙紅色;
(5)乙烯和溴水發生加成反應生成1,2-二溴乙烷,方程式為CH2═CH2+Br2→Br-CH2-CH2-Br,
故答案為:CH2═CH2+Br2→Br-CH2-CH2-Br;
(6)二氧化硫和硫化氫發生氧化還原反應生成硫,方程式為SO2+2H2S═3S↓+2H2O,二氧化硫和硫化氫都可與堿液反應,防止污染空氣,
故答案為:SO2+2H2S═3S↓+2H2O;吸收尾氣.
點評 本題考查綜合考查物質的性質,為高考常見題型,側重于學生的分析能力和實驗能力的考查,題目涉及氨氣、氯氣、乙烯氣體的制備及性質的檢驗,熟悉制備原理和物質的性質是解題關鍵,題目難度中等.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:實驗題
| 實驗編號 | 加入試劑 | 實驗現象 |
| Ⅰ | 2滴 0.1mol/L FeCl3 溶液 | ①白色沉淀轉化為紅褐色沉淀 |
| Ⅱ | 4mL2mol/LNH4Cl溶液 | ②白色沉淀溶解,得無色溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.6 g鐵粉在0.1mol氯氣中充分燃燒,轉移電子數為0.3NA | |
| B. | 2.5mL 16mol•L-1濃硫酸與足量銅反應,轉移電子數為0.04NA | |
| C. | 7.8g Na2S和Na2O2的固體混合物中含有的陰離子數等于0.1NA | |
| D. | 常溫下,5.6 g 鐵釘與足量濃硝酸反應,轉移的電子數為0.3 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲苯(苯酚):氫氧化鈉,蒸餾 | B. | 乙酸丁酯(乙酸):碳酸鈉,分液 | ||
| C. | 乙醇(苯酚):氫氧化鈉,分液 | D. | 乙醇(乙酸):堿石灰,分液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸和氫氧化銅 | B. | 硫酸和氫氧化鈉溶液 | ||
| C. | 醋酸和氫氧化鋇溶液 | D. | 稀硝酸和氨水混合 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分散質粒子能做不停的,無規則的運動 | |
| B. | 是否有丁達爾現象 | |
| C. | 靜置后既不分層,也無沉淀產生 | |
| D. | 分散質粒子直徑在10-7-10-9m之間 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com